INVESTIGATING THE STOICHIOMETRIC COUPLING BETWEEN MESOZOOPLANKTON ASSEMBLAGE AND SESTON IN FRESHWATERS
-
摘要: 通过对湖北省13个湖库悬浮物和中型浮游动物群体碳氮磷比的分析, 探讨了浮游动物与食物之间的元素耦联和不平衡性是如何随食物质量的改变而变化, 以及这种不平衡性对生态系统浮游动植物间能量传递效率的影响。结果显示: 中型浮游动物C﹕N比和C﹕P比分别随悬浮物C﹕N比和C﹕P比的增加而变大。悬浮物-中型浮游动物之间的元素不平衡性不仅与悬浮物C﹕N比显著正相关(r=0.97, P<0.001), 且与悬浮物C﹕P比也显著正相关(r=0.81, P=0.001)。浮游动植物之间的能量传递效率与悬浮物-中型浮游动物C﹕P比差值呈显著负相关(r= –0.58, P=0.037), 但与其C﹕N比差值关系不显著(P>0.05)。此外, 中型浮游动物生物量也随其与悬浮物之间C﹕P比差值的增大而下降(r= –0.59, P=0.033)。这些结果表明, 悬浮物碳氮磷比能显著影响中型浮游动物群体的碳氮磷比组成, 两者之间的元素不平衡性随前者的增加而变大并进而降低能量向后者的传递。Abstract: Food quality can significantly affect the phosphorus content, growth, reproduction, as well as physiological behavior of zooplankton, leading to regulate the energy transfer efficiency at the primary producer-consumer interface. However, the elemental coupling between zooplankton and food is scarcely observed at the community level. In this study, the elemental coupling and the elemental imbalances between seston and mesozooplankton assemblage in addition to the ecological impacts of such imbalances on zooplankton-phytoplankton interaction were detailed by analyzing the compositions of carbon, nitrogen, and phosphorus in seston and mesozooplankton assemblage derived from 13 samples containing water bodies in the Hubei province, China. The achieved results showed that both C﹕N and C﹕P ratios in mesozooplankton were positively correlated with the corresponding ratios in seston. Besides, the elemental imbalances between seston and mesozooplankton were positively correlated with the corresponding seston ratio (C﹕N,r=0.97, P<0.001; C﹕P,r=0.81, P=0.001). Further analysis also revealed that the energy transfer efficiency between zooplankton and phytoplankton declined with the increase of elemental imbalance in C﹕P ratio (r= –0.58, P=0.037). Moreover, a similar decline in zooplankton biomass was found as well as increase of imbalance in C﹕P ratio (r= –0.59, P=0.033). These results indicated that seston stoichiometry could remarkably impact the elemental stoichiometry of mesozooplankton assemblage, and the elemental imbalances tended to be greater with the increase of seston stoichiometry; consequently, the energy transferred to mesozooplankton was decreased as well.
-
Keywords:
- Seston /
- Food quality /
- Ecological stoichiometry /
- Energy transfer efficiency
-
生物与环境之间的物质耦联在自然界中广泛存在。研究发现, 异养细菌和浮游植物体内磷(P)元素含量随供应水平而变化[1, 2]; 湖泊营养水平能极大地影响沉水植被组织中宏量元素的含量[3]; 即使同一种螺, 它们体内的碳氮磷比也与环境中营养物质的含量密切相关[4]; 浮游植物组织中的不饱和脂肪酸含量还能显著影响浮游动物体内的不饱和脂肪酸含量[5]。
生态化学计量学(Ecological stoichiometry)理论为理解水生态系统生物之间的相互作用提供了一种有效手段。多样的光照、营养输入和环境介质特点造就了悬浮物较大的C﹕P比变化范围[1], 沿着这一环境梯度浮游动物优势物种也从高磷需求的溞类(Daphnia)向低磷需求的桡足类转变[6, 7]。浮游动物体内的元素含量相对稳定, 当面对多变的食物资源时, 其可能遭遇营养限制, 引起生长、繁殖、生理代谢的改变, 进而影响元素循环甚至能量在食物链中的传递效率[7, 8]。对于浮游动物群落而言, 优势物种组成不仅受食物数量影响, 还受食物质量影响。有研究发现哲水蚤在生长发育的不同阶段对食物中N、P的需求比例是不一样的[9], 肉食性桡足类的元素组成也有可能受食物元素比的影响[10], 对P需求更高的网纹溞(Ceriodaphnia)还可能在食物质量较差的低营养高光照的环境中通过对高P食物资源细菌的利用而形成竞争优势[2]。虽然Daphnia体内P含量随食物C﹕P比的增加而减小, 但其组织C﹕P比随食物C﹕P比的增加而增大[11]。自然水体中的浮游动物群落在物种、食性、大小组成上呈现多样化, 其群落碳氮磷比又是如何响应悬浮物质量变化的呢?从食物质量促进不同营养需求优势种群建立的现象出发, 我们推测, 浮游动物群落的元素组成比例也与食物质量密切相关, 有研究证实了它们两者C﹕P比呈显著正相关[12, 13]。
虽然作为个体存在的浮游动物会因食物质量或鱼类捕食而影响其在群落中的优势性, 但作为整体存在的浮游动物群落, 它们和悬浮物之间碳氮磷比耦联的相关报道还很少。另外, 浮游动物的元素调节能力有限, 食物质量如何影响两者元素之间的不平衡性(Imbalance)?这种不平衡程度如何影响生态系统营养关系?目前认识尚不明确。本文通过对湖北省境内13个湖库悬浮物、中型浮游动物群体碳氮磷比组成的分析, 旨在探讨两者之间的元素耦联和不平衡性是如何随食物质量的改变而变化, 以及这种不平衡性对生态系统浮游动植物间能量传递效率的影响。
1. 材料与方法
1.1 野外采样
本研究选取湖北省内13个水体进行采样, 其中湖泊3个、水库10个(表 1)。野外采样分别在2014年和2015年的4月20日—5月9日进行。每一水体设置3个采样点, 用5 L采水器按照间隔1 m的方式从水面往下采集15—20 L水样, 充分混匀后取2.5 L水样带回实验室用于营养盐、叶绿素a (Chl. a)和悬浮物碳氮磷比测定; 现场用透明度盘测定透明度(SD)。浮游甲壳动物样品的定量采集通过64 μm浮游生物网的垂直拖曳来实现, 上提速度约为 0.5 m/s, 采样深度为沉积物界面之上0.5 m到水面。采集的样品用福尔马林保存, 最终浓度为5%。中型浮游动物(200—2000 μm)样品的采集通过直径40 cm、孔径200 μm浮游生物网的垂直拖曳来实现, 采集的样品装入盛有湖水的2.5 L塑料壶, 带回室内处理。
1.2 室内分析
浮游植物生物量用Chl. a表示, 取200—800 mL的混合水样用GF/C膜过滤, 冰箱冷冻保存24h后放入装有10 mL 90%丙酮的塑料管, 在冰箱保温室抽提16h后离心, 取上清液在分光光度计上测定吸光度, 所用波长分别为630、645、663和750 nm。浮游甲壳动物组成和密度通过显微镜进行鉴定和计数, 大部分的浮游动物鉴定到种, 只有数量较少的小型物种鉴定到属, 枝角类和桡足类的鉴定参考工具书[14, 15]。每一样品计数完毕后对优势物种随机选取30个进行体长测定, 数量少的物种则尽可能多地测量体长, 然后利用体长-体重方程估算浮游动物湿重[16], 无节幼体未计入到总生物量。本文用浮游甲壳动物生物量和Chl. a含量的比值(Z/P)来表征浮游动植物之间的能量传递效率[17]。营养盐分析包括总溶解性氮(TDN)、总溶解性磷(TDP), 具体分析方法参考黄祥飞等[16]。
1.3 样品碳氮磷比测定
在测定悬浮物碳氮磷比之前, 混合水样先经64 μm筛绢过滤, 去除中型浮游动物难于摄食的粗粒径颗粒物, 然后用提前灼烧好的GF/F玻璃纤维滤膜(500℃, 3h)过滤尽可能多的水样, 之后用1 mol/L盐酸润洗去除无机碳的影响。滤膜经50℃干燥至恒重后在坩埚中碾磨成粉末用于元素测定。中型浮游动物样品在室内经2000和200 μm筛网过滤, 然后用蒸馏水冲洗至500 mL烧杯, 用胶头吸管去掉肉眼可见的杂质, 如此反复3次。最后将烧杯中的浮游动物用提前灼烧好的GF/C玻璃纤维滤膜(500℃, 3h)收集, 烘干、碾磨程序同悬浮物。碳、氮含量用Carlo Erba NC2500元素分析仪测定; 磷含量的测定同水样, 先取一定重量滤膜粉末经过硫酸钾氧化, 然后再离心取上清液测定。元素计量特征的不平衡性按下式计算:
ΔC﹕N=C﹕Nseston – C﹕Nzooplankton; ΔC﹕P=C﹕Pseston – C﹕Pzooplankton。
1.4 统计分析
悬浮物与中型浮游动物碳氮磷比的差异用单因素方差分析来检验(one way ANOVA), Pearson相关分析用软件SPSS 17.0完成, 显著性水平设置为P<0.05。
2. 结果
Chl. a含量的变化范围是1.05—52.8 μg/L, 平均值11.5 μg/L, 最小值和最大值分别出现在王英水库和高坝洲水库。浮游甲壳动物生物量均值0.93 mg/L, 最大值出现在2015年的惠亭水库(8.97 mg/L), 最小值出现在牛山湖(0.09 mg/L)(表 1)。
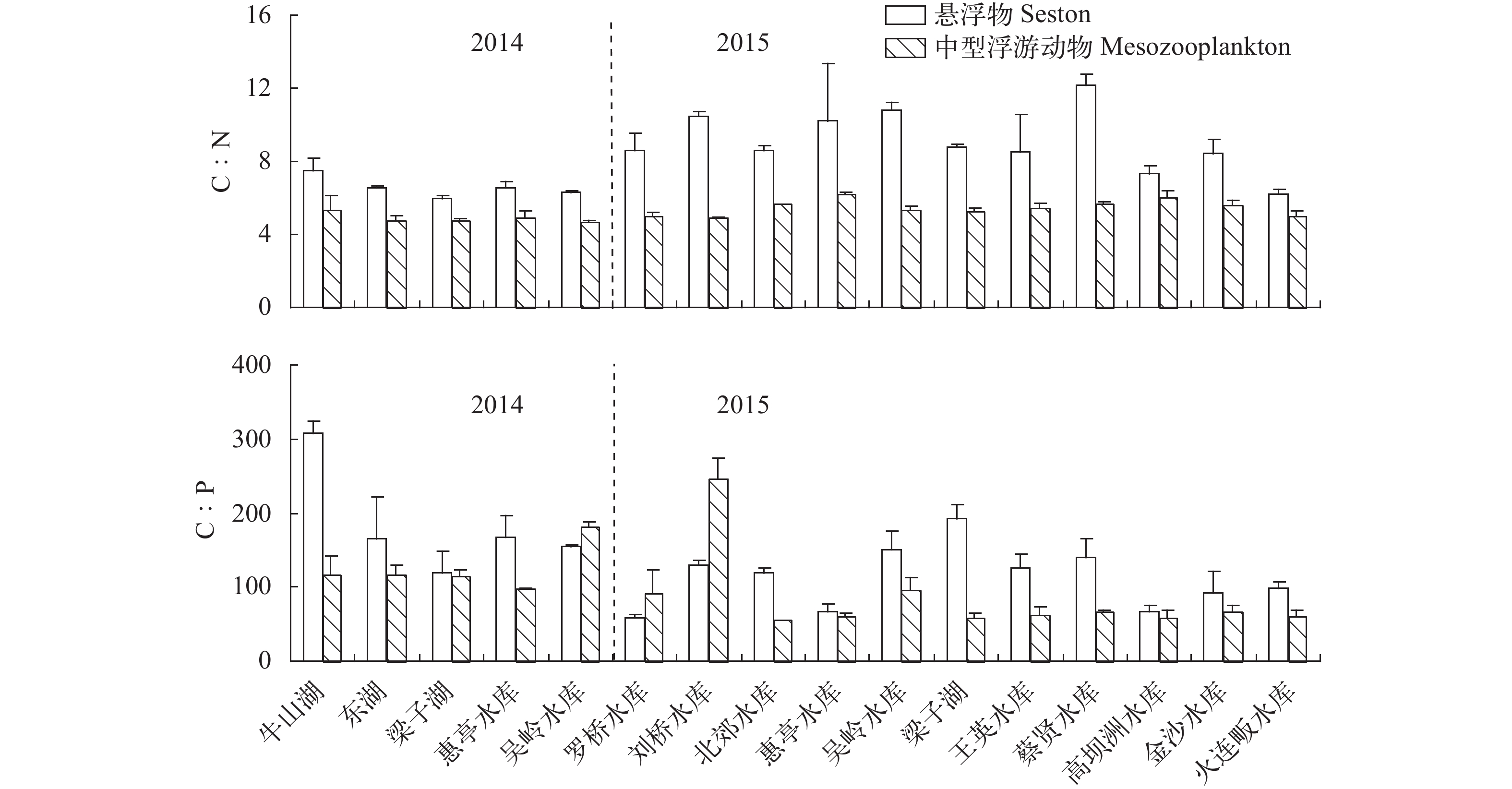
表 1 采样水体湖沼学特征Table 1. Limnological characteristics of the samples containing water bodies地点Site 经度Longitude 纬度Latitude SD (m) TDN (mg/L) TDP (mg/L) Chl. a (μg/L) Zbiomass (mg/L) 牛山湖1 114°34′40" 30°18′15" 0.70 0.58 0.03 5.70 0.09 东湖1 114°23′48" 30°33′57" 0.96 0.94 0.06 18.20 0.10 梁子湖1 114°32′47" 30°14′53" 1.06 0.55 0.04 5.40 1.05 惠亭水库1 113°05′24" 31°00′37" 2.51 0.63 0.02 5.00 0.20 吴岭水库1 113°05′37" 30°53′21" 1.58 1.04 0.03 5.50 0.35 罗桥水库 112°41′21" 32°13′11" 0.58 1.59 0.13 16.40 0.13 刘桥水库 112°41′33" 32°11′22" 0.61 1.44 0.08 10.00 0.16 北郊水库 112°46′40" 32°10′24" 0.80 1.47 0.11 8.60 0.30 惠亭水库 113°05′24" 31°00′37" 7.40 1.19 0.08 1.94 8.97 吴岭水库 113°05′37" 30°53′21" 1.55 0.96 0.07 4.40 0.67 梁子湖 114°32′47" 30°14′53" 1.32 1.83 0.07 9.80 0.60 王英水库 114°49′41" 29°47′13" 7.35 1.65 0.07 1.10 0.40 蔡贤水库 114°46′20" 29°51′01" 3.62 1.86 0.07 18.10 0.45 高坝洲水库 111°20′40" 30°23′33" 1.18 3.24 0.08 52.80 0.91 金沙水库 114°35′37" 31°17′45" 4.91 1.82 0.08 1.90 0.46 火连畈水库 114°40′47" 31°23′25" 1.22 1.32 0.11 19.20 0.12 注: SD. 透明度; TDN. 总溶解性氮; TDP. 总溶解性磷; Zbiomass. 浮游甲壳动物生物量; 有上标1的表示该水体在2014年采样, 没有的则表示其在2015年采样 Note: SD. Secchi depth; TDN. total dissolved nitrogen; TDP. total dissolved phosphorus; Zbiomass, crustacean zooplankton biomass. Sites with 1 superscripts indicate that the water bodies were sampled in 2014, whereas those without numbers were sampled in 2015 悬浮物C﹕N比变化范围为5.95—12.2, 均值8.06, 变异系数为22.4%; 中型浮游动物C﹕N比变化范围为4.68—6.17, 均值5.30, 变异系数为8.7%。单因素方差分析显示悬浮物C﹕N比要显著大于中型浮游动物(F1, 30=39.6, P<0.001)。悬浮物C﹕P比最大值出现在牛山湖(307), 最小值出现在罗桥水库(59), 均值139, 变异系数为44.6%; 中型浮游动物C﹕P比最大值出现在刘桥水库(246), 最小值出现在北郊水库(56), 均值97, 变异系数为53.6% (图 1), 单因素方差分析显示悬浮物C﹕P比与中型浮游动物差异不显著(F1, 30=3.56, P=0.069)。
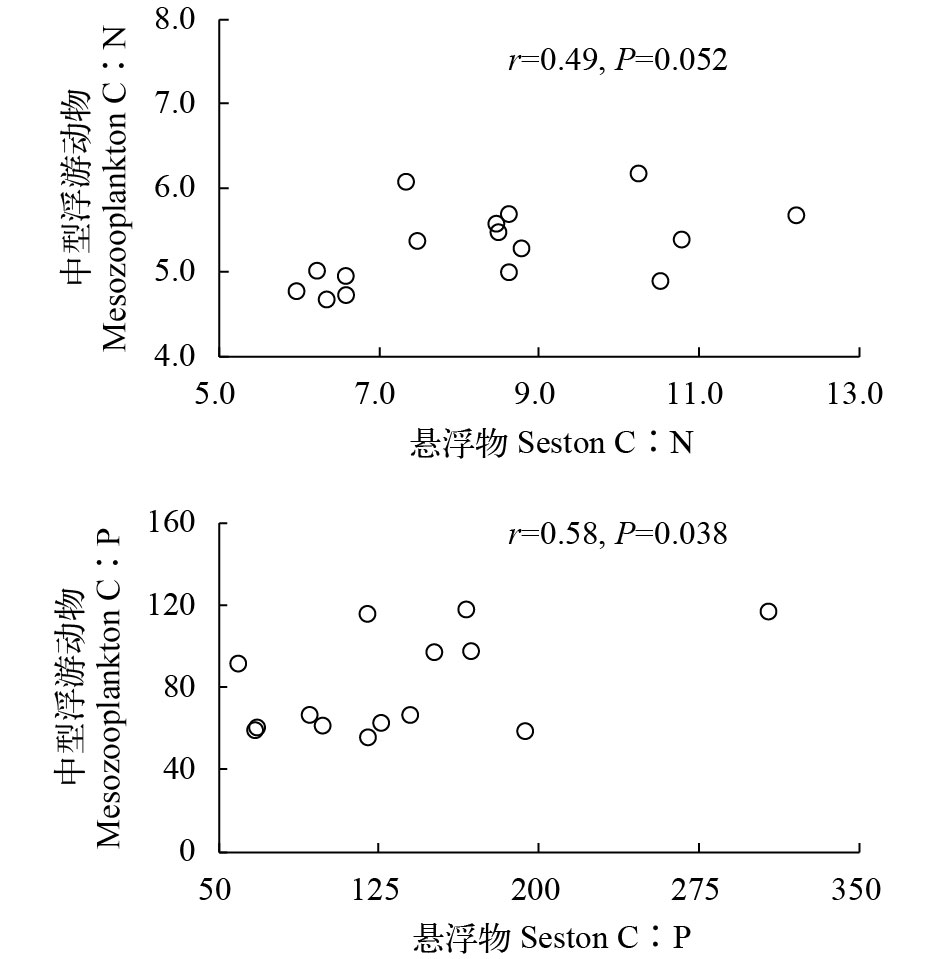
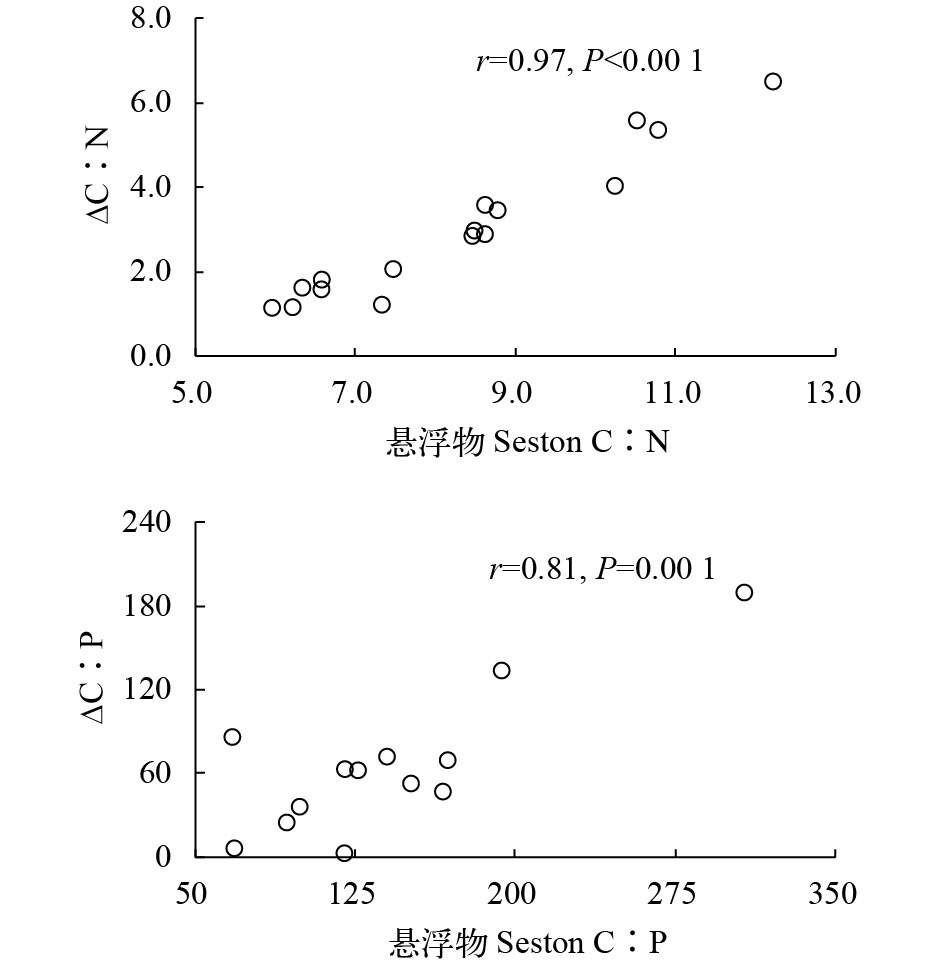
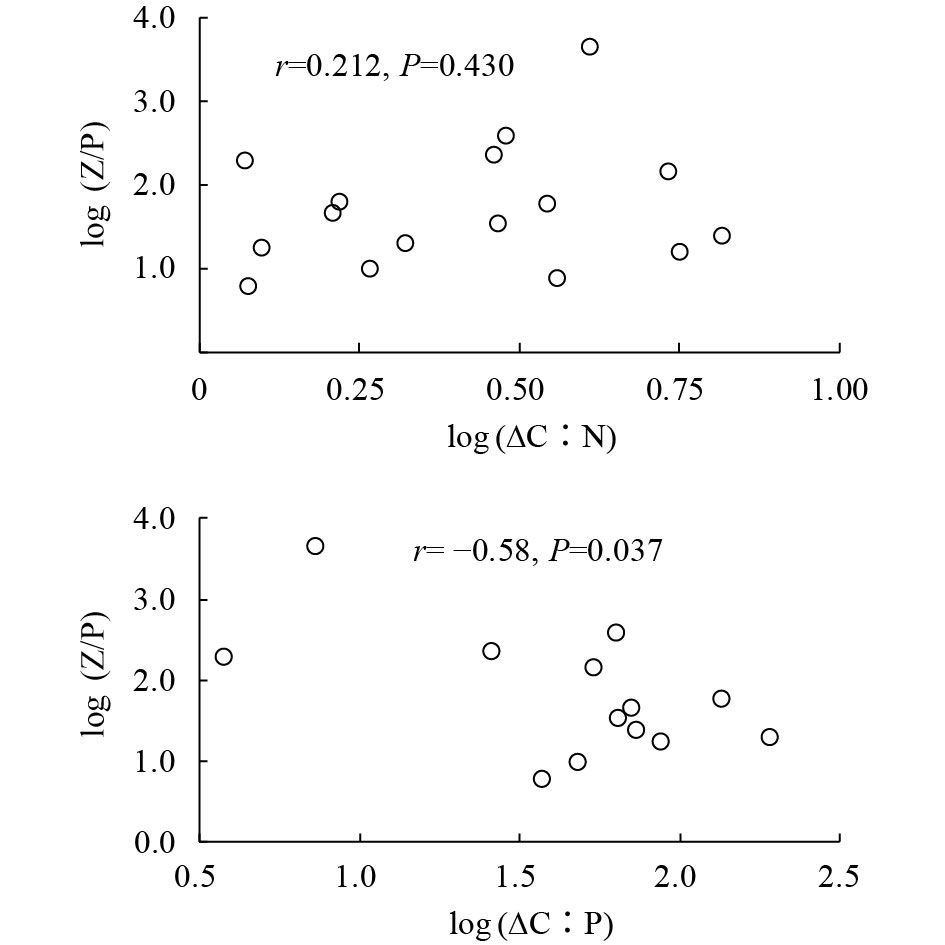
相关分析显示, 中型浮游动物C﹕N比与悬浮物C﹕N比呈正相关(r=0.49, P=0.052)。81%的采样点的悬浮物C﹕P比大于中型浮游动物, 我们剔除了与此结果相反的3个异常点后两者C﹕P比也显著正相关(r=0.58, P=0.038)(图 2)。悬浮物-中型浮游动物C﹕N比差值与悬浮物C﹕N比显著正相关(r=0.97, P<0.001)。类似地, 其C﹕P比差值与悬浮物C﹕P比显著正相关(r=0.81, P=0.001)(图 3)。此外, 随着C﹕P比不平衡性加大, 中型浮游动物生物量也随之降低(r=–0.59, P=0.033)。浮游动植物之间的能量传递效率随C﹕P比不平衡性的增大而显著下降(r=–0.58, P=0.037), 但与C﹕N比不平衡性的关系不显著(P=0.430)(图 4)。
3. 讨论
3.1 中型浮游动物与悬浮物碳氮磷比耦联
环境的选择作用通常导致物种沿着一定的环境梯度分布, 从适合度(Fitness)的角度看, 物种将尽力调整以使自身不被环境淘汰。食物C﹕P比和C﹕N比对浮游甲壳动物群落结构的影响已在上一文[18]中详细讨论, 在此不再赘述。在本文中, 中型浮游动物群落碳氮磷比与食物资源碳氮磷比呈正相关。据我们所知, 目前有4篇文献报道了浮游动物群落C﹕P比与悬浮物C﹕P比的关系, 其中两篇显著正相关[12, 13], 一篇未发现相关性[19]; 另一篇发现两者关系呈抛物线型[20]。这种消费者-食物之间的元素耦联在其他生物中也有类似报道, 如鱼类、陆生昆虫[21]和蚌[22], 它们体内的碳氮磷比也与食物资源碳氮磷比密切相关。浮游动物体内的碳氮磷含量一般被认为是相对稳定的(Homeostasis), 当食物C﹕P比增加时, 高P需求的Daphnia 会被低磷需求的桡足类取代[6], 从而使浮游动物群体的碳氮磷水平适应环境改变。Hassett等[23]研究发现悬浮物C﹕P比与Daphnia生物量百分比显著负相关, 而与哲水蚤生物量百分比显著正相关。进一步分析发现, 中型浮游动物与悬浮物碳氮磷比组成上的不平衡性随悬浮物碳氮磷比的增加而增大, 表明中型浮游动物内在的元素调节能力有限。Teurlincx等[20]研究发现, 当悬浮物C﹕P比低于270时, 浮游动物群落C﹕P比与之正相关, 然而当悬浮物C﹕P比从500增加到1000时, 浮游动物群落C﹕P比基本维持在100左右, 物种配置(Species sorting)和其C﹕P比可塑性共同决定浮游动物群落的C﹕P比。另外, 浮游动物C﹕P比变化范围约为30—300, 而悬浮物的变化范围可达40—1000, 这种不匹配的变化幅度决定了两者的不平衡性可随悬浮物C﹕P比的增加而不断变大。整体来看, 在一定悬浮物C﹕P比范围内, 浮游动物群落C﹕P比与之显著正相关。Persson等[21]通过大数据分析认为: 不仅自养生物, 还包括许多异养生物, 其体内碳氮磷比并不是严格一成不变的, 稳定的程度取决于外部(如环境)和内部(如生理状态和生长)因子的共同作用。
3.2 碳氮磷比不平衡性对生态系统过程的影响
初级生产者与植食性消费者之间的元素不平衡无所不在, 了解这种不平衡对生物相互关系以及食物链能量传递效率的影响是生态学研究的一项重要任务[7]。在本文中, 浮游动植物之间的能量传递效率随两者C﹕P比不平衡性的加大而降低, 表明食物元素供应与浮游动物需求之间的不平衡会影响C向浮游动物的流动。Sterner等[24]发现, 高光照时藻类固定的大量碳并没有有效转化成浮游动物生物量, 导致其净生产量近乎为零。在1个P限制的湖泊, 遮荫处理增加了低P处理中植食性浮游动物的生物量, 因为食物质量的提高(低C﹕P比)超越了光照不足引起的初级生产量降低[7]。因此, 当食物C﹕P比偏离浮游动物群体需求时, 意味着多余的C进入了浮游动物体内, 可能导致同化效率降低或呼吸作用增强[25], 从而对群体生长、繁殖产生抑制作用, 引起其生物量降低。本文发现随着C﹕P比不平衡性加大, 中型浮游动物生物量也随之降低。另一方面, 浮游动物营养需求与食物供应不平衡性的加大意味着两者耦联性降低, 此时可能引起浮游动物群落中优势物种的转换和食性改变, 比如从植食性向杂食性甚至肉食性转变[26], 从而引起食物链长度增加, 降低C在食物链中的传递效率。同时, 模型研究发现: 当悬浮物C﹕P比较大可能导致浮游动物受到P限制时, 食物链的传递效率就会降低; 而当悬浮物元素供应与浮游动物需求完全匹配时, 此时食物链传递效率最高[27]。另外, 当浮游动物受到营养限制时, 会导致相应限制性元素在其体内累积, 影响元素循环并进一步加强初级生产者的营养限制[28]。所以, 光照和营养输入的平衡将直接决定悬浮物化学计量组成, 进而影响物质和能量在食物链中的传递效率。
-
表 1 采样水体湖沼学特征
Table 1 Limnological characteristics of the samples containing water bodies
地点Site 经度Longitude 纬度Latitude SD (m) TDN (mg/L) TDP (mg/L) Chl. a (μg/L) Zbiomass (mg/L) 牛山湖1 114°34′40" 30°18′15" 0.70 0.58 0.03 5.70 0.09 东湖1 114°23′48" 30°33′57" 0.96 0.94 0.06 18.20 0.10 梁子湖1 114°32′47" 30°14′53" 1.06 0.55 0.04 5.40 1.05 惠亭水库1 113°05′24" 31°00′37" 2.51 0.63 0.02 5.00 0.20 吴岭水库1 113°05′37" 30°53′21" 1.58 1.04 0.03 5.50 0.35 罗桥水库 112°41′21" 32°13′11" 0.58 1.59 0.13 16.40 0.13 刘桥水库 112°41′33" 32°11′22" 0.61 1.44 0.08 10.00 0.16 北郊水库 112°46′40" 32°10′24" 0.80 1.47 0.11 8.60 0.30 惠亭水库 113°05′24" 31°00′37" 7.40 1.19 0.08 1.94 8.97 吴岭水库 113°05′37" 30°53′21" 1.55 0.96 0.07 4.40 0.67 梁子湖 114°32′47" 30°14′53" 1.32 1.83 0.07 9.80 0.60 王英水库 114°49′41" 29°47′13" 7.35 1.65 0.07 1.10 0.40 蔡贤水库 114°46′20" 29°51′01" 3.62 1.86 0.07 18.10 0.45 高坝洲水库 111°20′40" 30°23′33" 1.18 3.24 0.08 52.80 0.91 金沙水库 114°35′37" 31°17′45" 4.91 1.82 0.08 1.90 0.46 火连畈水库 114°40′47" 31°23′25" 1.22 1.32 0.11 19.20 0.12 注: SD. 透明度; TDN. 总溶解性氮; TDP. 总溶解性磷; Zbiomass. 浮游甲壳动物生物量; 有上标1的表示该水体在2014年采样, 没有的则表示其在2015年采样 Note: SD. Secchi depth; TDN. total dissolved nitrogen; TDP. total dissolved phosphorus; Zbiomass, crustacean zooplankton biomass. Sites with 1 superscripts indicate that the water bodies were sampled in 2014, whereas those without numbers were sampled in 2015 -
[1] Godwin G M, Cotner J B. Aquatic heterotrophic bacteria have highly flexible phosphorus content and biomass stoichiometry [J]. The ISME Journal, 2015, 9(10): 2324–2327
[2] Hall S P, Leibold M A, Lytle D A, et al. Stoichiometry and planktonic grazer composition over gradients of light, nutrients, and predation risk [J]. Ecology, 2004, 85(8): 2291–2301
[3] Xing W, Wu H, Shi Q, et al. Multielement stoichiometry of submerged macrophytes across Yunnan plateau lakes (China) [J]. Scientific Reports, 2015, 5: 10186
[4] Cai Y, Xue Q, Xu J, et al. Widespread natural intraspecific variation in tissue stoichiometry of two freshwater molluscs: Effect of nutrient enrichment [J]. Ecological Indicators, 2016, 66: 583–591
[5] Brett M T, Müller-Navarra D C, Ballantyne A P, et al. Daphnia fatty acid composition reflects that of their diet [J]. Limnology and Oceanography, 2006, 51(5): 2428–2437
[6] Laspoumaderes C, Modenutti B, Souza M S, et al. Glacier melting and stoichiometric implications for lake community structure: zooplankton species distributions across a natural light gradient [J]. Global Change Biology, 2013, 19(1): 316–326
[7] Urabe J, Kyle M, Makino W, et al. Reduced light increases herbivore production due to stoichiometric effects of light/nutrient balance [J]. Ecology, 2002, 83(3): 619–627
[8] Hessen D O, Elser J J, Sterner R W, et al. Ecological stoichiometry: an elementary approach using basic principles [J]. Limnology and Oceanography, 2013, 58(6): 2219–2236
[9] Meunier C L, Boersma M, Wiltshire K H, et al. Zooplankton eat what they need: copepod selective feeding and potential consequences for marine systems [J]. Oikos, 2016, 125(1): 50–58
[10] Laspoumaderes C, Modenutti B, Elser J J, et al. Does the stoichiometric carbon:phosphorus knife edge apply for predaceous copepods [J] Oecologia, 2015, 178(2): 557–569
[11] DeMott W R, Gulati R D, Siewertsen K. Effects of phosphorus-deficient diets on the carbon and phosphorus balance of Daphnia magna [J]. Limnology and Oceanography, 1998, 43(6): 1147–1161
[12] Hessen D O, van Donk E, Gulati R. Seasonal seston stoichiometry: effects on zooplankton in cyanobacteria-dominated lakes [J]. Journal of Plankton Research, 2005, 27(5): 449–460
[13] McCarthy V, Irvine K. A test of stoichiometry across six Irish lakes of low-moderate nutrient status and contrasting hardness [J]. Journal of Plankton Research, 2010, 32(1): 15–29
[14] 蒋燮治, 堵南山. 中国动物志: 淡水枝角类. 北京: 科学出版社. 1979, 79-273 Jiang X Z, Du N S. Fauna Sinica, Crustacea: Freshwater Cladocera [M]. Beijing: Science Press. 1979, 79-273
蒋燮治, 堵南山. 中国动物志: 淡水枝角类. 北京: 科学出版社. 1979, 79-273[15] 沈嘉瑞. 中国动物志: 淡水桡足类. 北京: 科学出版社. 1979, 53-420 Shen J R. Fauna Sinica, Crustacea: Freshwater Copepoda [M]. Beijing: Science Press. 1979, 53-420
沈嘉瑞. 中国动物志: 淡水桡足类. 北京: 科学出版社. 1979, 53-420[16] 黄祥飞, 陈伟民, 蔡启铭. 湖泊生态调查观测与分析. 北京: 中国标准出版社. 1999, 90-91 Huang X F, Chen W M, Cai Q M. Survey, Observation and Analysis of Lake Ecology [M]. Beijing: Standards Press of China. 1999, 90-91
黄祥飞, 陈伟民, 蔡启铭. 湖泊生态调查观测与分析. 北京: 中国标准出版社. 1999, 90-91[17] Havens K E, Beaver J R. Zooplankton to phytoplankton biomass ratios in shallow Florida lakes: an evaluation of seasonality and hypotheses about factors controlling variability [J]. Hydrobiologia, 2013, 703(1): 177−187
[18] 王松波, 耿红, 吴来燕, 等. 食物和理化因子对浮游甲壳动物群落结构的影响. 湖泊科学, 2018, 30(3): 723-731 Wang S B, Geng H, Wu L Y, et al. Effects of food and physicochemical factors on crustacean zooplankton community structure [J]. Journal of Lake Sciences, 2018, 30(3): 723-731
王松波, 耿红, 吴来燕, 等. 食物和理化因子对浮游甲壳动物群落结构的影响. 湖泊科学, 2018, 30(3): 723-731[19] Dobberfuhl D R, Elser J J. Elemental stoichiometry of lower food web components in arctic and temperate lakes [J]. Journal of Plankton Research, 2000, 22(7): 1341–1354
[20] Teurlincx S, Velthuis M, Seroka D, et al. Species sorting and stoichiometric plasticity control community C: P ratio of first–order aquatic consumers [J]. Ecology Letters, 2017, 20(6): 751–760
[21] Persson J, Fink P, Goto A et al. To be or not to be what you eat: regulation of stoichiometric homeostasis among autotrophs and heterotrophs [J]. Oikos, 2010, 119(5): 741–751
[22] Vanderploeg H A, Sarnelle O, Liebig J R, et al. Seston quality drives feeding, stoichiometry and excretion of zebra mussels [J]. Freshwater Biology, 2017, 62(4): 664–680
[23] Hassett R P, Cardinale B, Stabler L B, et al. Ecological stoichiometry of N and P in pelagic ecosystems: comparison of lakes and oceans with emphasis on the zooplankton-phytoplankton interaction [J]. Limnology and Oceanography, 1997, 42(4): 648–662
[24] Sterner R W, Clasen J, Lampert W, et al. Carbon:phosphorus stoichiometry and food chain production [J]. Ecology Letters, 1998, 1(3): 146–150
[25] Andersen T, Elser J J, Hessen D O. Stoichiometry and population dynamics [J]. Ecology Letters, 2004, 7(9): 884–900
[26] Gaedke U, Hochstädter S, Straile D. Interplay between energy limitation and nutritional deficiency: empirical data and food web models [J]. Ecological Monographs, 2002, 72(2): 251–270
[27] Peace A. Effects of light, nutrients, and food chain length on trophic efficiencies in simple stoichiometric aquatic food chain models [J]. Ecological Modelling, 2015, 312: 125–135
[28] Elser J J, Urabe J. The stoichiometry of consumer-driven nutrient recycling: theory, observations, and consequences [J]. Ecology, 1999, 80(3): 735–751
-
期刊类型引用(0)
其他类型引用(1)



 下载:
下载: