ESTABLISHMENT ENDOPLASMIC RETICULUM STRESS MODEL INDUCED BY β-CONGLYCININ IN INTESTINAL EPITHELIAL CELLS OF HYBRID YELLOW CATFISH (PELTEOBAGRUS FULVIDRACO ♀ ×PELTEOBAGRUS VACHELLI ♂)
-
摘要:
实验旨在利用β-伴大豆球蛋白构建黄颡鱼上皮细胞内质网应激(Endoplasmic reticulum stress, ERS)模型。利用酶消化法分离得到黄颡鱼肠道上皮细胞, 通过细胞形态、角蛋白18 (Cytokeratin-18, CK-18)免疫荧光染色和碱性磷酸酶染色法鉴定。利用不同浓度β-伴大豆球蛋白刺激24h后, RT-qPCR检测相关基因转录表达水平, 筛选最合适刺激浓度。在此浓度下分别刺激黄颡鱼肠道上皮细胞0、12h、24h和36h, 使用RT-qPCR、CCK8、透射电镜和免疫荧光染色等方法检测相关指标, 筛选最适刺激时间。结果表明: (1)成功分离培养黄颡鱼肠道上皮细胞, 细胞呈铺路石状, CK-18和碱性磷酸酶染色呈阳性; (2)成功筛选到4 mg/mL β-伴大豆球蛋白为最佳刺激浓度。在该浓度下, 除grp78、jnk、il-10、atf6外, 内质网应激、自噬、凋亡、炎症等相关基因表达水平均显著最高(P<0.05); 成功筛选24h为最适刺激时间。4 mg/mL β-伴大豆球蛋白刺激细胞24h显著降低细胞活力, 同时引起内质网显著肿胀, GRP78、LC3、Caspase3蛋白表达和Tunel信号显著升高(P<0.01), perk、atf6、beclin1、lc3a、bcl2、caspase3、caspase9和il-12 mRNA表达水平显著最高(P<0.05)。综上, 实验成功分离得到黄颡鱼肠道上皮细胞, 构建了黄颡鱼肠道上皮细胞内质网应激模型。实验为进一步研究未折叠反应信号通路在黄颡鱼豆粕诱导肠炎发生发展中的作用奠定基础。
Abstract:The purpose of this study was to establish an endoplasmic reticulum stress model induced by β-conglycinin using intestinal epithelial cells from hybrid yellow catfish. The method involved isolating intestinal epithelial cells using an enzyme digestion method. Cells were identified through morphological assessment, cytokeratin-18 (CK-18) immunofluorescence, and alkaline phosphatase staining. Following isolation, well-grown cells were stimulated with different levels of β-conglycinin for 24h. RT-qPCR was employed to measure mRNA expression of relative indexes to determine the optimal stimulation concentration. Subsequently, cells were stimulated at the optimal concentration for 0, 12h, 24h and 36h. RT-qPCR, CCK8, transmission electron microscopy, and immunofluorescence were used for measuring the relative indexes to determine the suitable stimulation time. The results indicated that: (1) Successful isolation of intestinal epithelial cells from hybrid yellow catfish, characterized by paving stone-like cell morphology and positive CK-18 and alkaline phosphatase staining. (2) Identification of 4 mg/mL as the optimal stimulation concentration. Treatment with 4 mg/mL β-conglycinin significantly elevated mRNA levels of ERS, autophagy, apoptosis and inflammation related genes (P<0.05), except for grp78, jnk, il-10 and atf6 genes. (3) Determination of 24h as the optimal stimulation duration. Cell viability significantly decreased with prolonged stimulation time. Notably, after 24h of treatment, swellen endoplasmic reticulum, elevated levels of GRP78, LC3, Caspase3 protein, Tunle signal, and the mRNA expression of perk, atf6, beclin1, lc3a, bcl2, caspase3, caspase9 and il-12 were observed (P<0.01). In conclusion, this study successfully isolated intestinal epithelial cells from hybrid yellow catfish and established the endoplasmic reticulum stress model. These findings provides a foundation for understanding the effects of unfolded protein response on soybean meal-induced enteritis of hybrid yellow catfish.
-
肠道上皮细胞是肠道的主要功能细胞, 负责营养物质的消化、吸收、免疫和应激反应等[1]。因此, 肠道上皮细胞经常作为体外细胞模型用于营养学和病理学研究, 是探究外源性物质对肠道上皮细胞作用机制的重要技术手段。近年来, 快速发展的水产养殖业使得鱼粉需求量和鱼粉供给量出现极度不平衡, 鱼粉出现严重短缺, 价格不断攀升, 寻找能够部分或完全替代鱼粉的蛋白源成为水产饲料行业的研究热点[2]。植物蛋白源因来源广、价格低, 被认为是理想的鱼粉替代品。然而植物蛋白易引起鱼类不耐受, 导致食源性肠炎, 以豆粕诱导肠炎(Soybean meal-induced enteritis, SBMIE)最为典型。豆粕替代鱼粉对鱼类生长和生理状态的影响及其摄食机制具有物种特异性[3], 在肉食性鱼类最为高发, 降低鱼类生长性能, 引起肠道炎症, 损害肠道健康。以鱼类SBMIE为代表的食源性肠道炎症已经成为限制我国水产养殖业绿色可持续发展的重要问题。
β-伴大豆球蛋白是豆粕中主要的抗原蛋白, 分子质量为140—180 kD, 约占豆粕总蛋白质含量的40%[4]。β-伴大豆球蛋白主要在肠道部位被消化吸收, 是引起肠道消化吸收功能障碍、诱发肠炎的常见抗原蛋白, 被认为是影响鱼类肠道健康的主要抗营养因子之一[5], 可引起多种鱼类肠道炎症[6, 7]。因此, 使用β-伴大豆球蛋白构建SBMIE模型, 深入探索并解析β-伴大豆球蛋白对水生生物肠道的致敏机理及鱼类肠道对β-伴大豆球蛋白的响应规律, 可为寻求防治SBMIE的策略提供研究基础。
内质网是真核生物重要的细胞器, 是细胞内蛋白质合成和修饰的主要场所, 维护着细胞内环境稳态与平衡。当受到外界不良刺激或干扰时, 内质网易发生功能紊乱, 导致未折叠的蛋白及错误折叠的蛋白在内质网累积, 从而引起内质网应激(Endoplasmic reticulum stress, ERS), 诱发未折叠反应(Unfolded protein response, UPR)。UPR通过肌醇需求酶1α (Inositol-requiring enzyme 1, IRE1α)、蛋白激酶R样内质网激酶(Protein kinase r-like er kinase, PERK)和活化转录因子6 (Activating transcription factor 6, ATF6 α)三种内质网膜相关蛋白表达引起下游信号反应, 进而减缓蛋白合成、促使未折叠蛋白或错误折叠蛋白正确折叠、或者降解未折叠蛋白等, 恢复内质网稳态[8]。当内质网应激持续或重度发生时, 则诱发自噬或者凋亡, 引起疾病发生发展[9, 10]。在这一过程中, 主要分布于内质网中的热休克蛋白葡萄糖调节蛋白78 (Glucose-regulated protein 78, GRP78)被认为是发生内质网应激的标志物[11]。在正常生理状态, GRP78与UPR的三种跨膜感受蛋白紧密结合, 使其处于非活性状态。在内质网应激时, GRP78与上述3种感受器发生解离, 进而启动UPR和下游级联反应[12]。
肠道是生物消化和营养吸收的主要场所, 也是机体与外部环境接触的重要部位之一, 面临来自外界的各种刺激和压力, 极易发生内质网应激[13]。哺乳动物中已报道, 炎性肠病与肠上皮的内质网应激直接有关, 内质网应激通过影响免疫细胞的增殖、分化和炎性因子的释放等, 加重炎症性肠病[14, 15]。鱼类中已有研究发现, 饲料中鱼粉含量过低, 植物蛋白、碳水化合物或者脂肪含量过高等[16—18]营养因素均可导致鱼类肠道上皮细胞发生内质网应激, 引发肠道炎症发生。本实验室前期研究数据也表明, 饲料中豆粕替代鱼粉可引起黄颡鱼肠道发生内质网应激, 且UPR三条信号通路及其下游因子受饲料中豆粕添加量和投喂时间的调控(数据暂未发表), 推测UPR反应信号通路的作用在黄颡鱼SBMIE发生发展的不同阶段存在差异。
因此, 为进一步研究UPR信号通路在黄颡鱼SBMIE发生发展中的作用, 挖掘调控鱼类SBMIE肠道黏膜屏障功能的靶点, 本研究以黄颡鱼为研究对象, 通过鱼类细胞培养技术分离得到黄颡鱼肠道上皮细胞, 使用β-伴大豆球蛋白刺激构建内质网应激模型, 为体外研究UPR反应信号通路在鱼类SBMIE中的作用和机制提供模型。
1. 材料与方法
1.1 实验鱼
实验用黄颡鱼[规格: (3.00±0.50) g]取自河南省郑州市黄河特种鱼苗繁育中心, 运回后置于河南农业大学第一实验楼方形养殖缸内(长1.2 m, 宽0.4 m, 高0.6 m; 有效水体积0.24 m3), 使用本实验配置的以鱼粉为主要蛋白原的暂养料(蛋白水平: 43.22%; 脂肪水平: 8.88%)暂养7d, 选取表观健康的黄颡鱼用于实验。暂养条件: 自然光照, 循环水, 连续适量充气, 水体溶氧量>5 mg/L, 水温22—25℃, 氨氮含量<0.01 mg/L。每天表观饱食投喂两次(09:00和15:00)。
1.2 主要试剂
β-伴大豆球蛋白购自淮北富德莱博食品科技有限公司; 胎牛血清购自Biological Industries; L-15培养基、三抗(青霉素-链霉素-两性霉素B混合溶液)、胰岛素、表皮生长因子、胶原酶Ⅰ、胶原酶Ⅳ、中性蛋白酶Ⅱ、胰蛋白酶、D-Hanks缓冲溶均购自北京索莱宝科技有限公司; HiScript Ⅱ Q RT SuperMix、ChamQ-SYBR-qPCR Master Mix购自南京诺唯赞生物科技股份有限公司; 破膜液、DAPI染液、抗荧光淬灭封片剂、一抗Anti-CK-18 Rabbit pAb、Anti-GRP78 BiP Rabbit pAb、Anti-LC3 Rabbit pAb、Anti-Caspase-3 Rabbit pAb、二抗山羊抗兔IgG、牛血清白蛋白磷酸酶试剂盒购自武汉赛维尔生物科技有限公司。
1.3 黄颡鱼肠道上皮细胞的分离
黄颡鱼肠道上皮细胞分离方法参照王立改等[19]的方法。
具体操作步骤如下: 在无菌操作台中, 取禁食48h后的黄颡鱼于托盘中, 用剪刀断头致死后断尾放血, 置于75%酒精溶液中浸泡1min; 用无菌吸水纸擦净鱼体表粘液, 取出肠道, 放入盛有含有4%三抗的D-hanks清洗液的培养皿中, 去除肠系膜及脂肪组织, 纵向剖开肠道, 放入新的清洗液中清洗3次; 将清洗过的肠道组织置于干燥的无菌培养皿中, 用剪刀剪碎至1 mm3左右并转移至L-15培养基中清洗3次, 加入约三倍体积的混合消化液(胶原酶Ⅰ﹕胶原酶Ⅳ﹕中性酶Ⅱ=1﹕1﹕2)于50 mL离心管中, 在28℃恒温摇床中消化10min后静置1min, 弃掉上层悬浊液, 加入新的消化液, 消化至出现浑浊, 用细胞筛过滤至新的50 mL离心管中, 1500 r/min离心5min后弃上清, 加入适量L-15培养基清洗3次, 最后加入完全培养基重悬细胞。
1.4 黄颡鱼肠道上皮细胞的原代培养
显微镜计数重悬细胞的密度, 将其接种到六孔板中, 使细胞数量为1×105个/孔左右, 每孔加入2 mL完全培养基, 然后将六孔板置于CO2恒温培养箱中进行培养。90min后, 将未贴壁的细胞连同培养基一起转移到新的六孔板中, 24h后弃掉上层未贴壁的细胞加入新的培养基继续培养。培养期间, 每24h更换一次培养基。
1.5 黄颡鱼肠道上皮细胞的鉴定
细胞爬片的制作 将细胞接种在六孔板中的爬片上, 待细胞状态稳定后, 吸出培养基, 用PBS清洗爬片3次, 每次5min, 4%多聚甲醛固定30min, 用PBS清洗3次, 每次5min。
CK-18免疫荧光鉴定 将制作好的爬片加入100 μL破膜液, 室温孵育20min, PBS洗3次, 3% BSA室温封闭30min, 滴加1﹕50稀释的一抗, 并置于湿盒内4℃孵育过夜, PBS清洗3次后滴加二抗(稀释比例为1﹕500), 室温孵育50min后PBS清洗3次。爬片滴加DAPI染液, 避光室温孵育10min, PBS清洗3次后用抗荧光淬灭封片剂封片后置于荧光显微镜下观察并采集图像。
碱性磷酸酶染色 将制作好的细胞爬片置根据碱性磷酸酶试剂盒说明书进行染色, 中性树胶封片后, 使用显微镜镜检, 并进行图像采集。
1.6 模型构建
筛选β-伴大豆球蛋白浓度 使用L-15培养基将β-伴大豆球蛋白分别稀释为终浓度为0、2、4、8和12 mg/mL的处理液, 选取六孔板中生长良好的细胞, 用D-hanks清洗细胞后, 分别加入含不同浓度的β-伴大豆球蛋白的处理液, 每个浓度梯度3个重复孔, 每孔的最终体积为2 mL, 处理细胞24h后, 收细胞, 提取细胞总RNA, –80℃保存待测。
细胞活力的检测 使用4 mg/mL β-伴大豆球蛋白分别处理细胞12h、24h和36h, 以无处理组为对照组, 每个处理3个重复孔, 使用CCK8法测定细胞活力。
细胞免疫荧光染色 使用4 mg/mL β-伴大豆球蛋白处理细胞24h, 制作细胞爬片, 用于GRP78/LC3及Caspase3/Tunel蛋白的免疫荧光检测, 方法同上, 使用ImageJ软件进行荧光强度量化。
1.7 透射电镜观察细胞内质网形态
用2.5%戊二醛固定5min, 用细胞刮将细胞收集于离心管中, 1500 r/min离心2min, 弃掉上清后加入2.5%戊二醛室温避光固定50min, 然后用0.1 mmol/L的磷酸缓冲液(pH=7.4)漂洗3次, 每次10min, 将细胞团块置于1%锇酸溶液中固定2h后, 用同样的方法再次漂洗, 之后用梯度乙醇、丙酮脱水, 然后用丙酮、环氧树脂包埋剂包埋后60℃烤箱聚合48h, 70 nm切片、染色后用透射电镜仪(日立有限公司, HITACHI HT7800)观察内质网形态并采集图像。
1.8 引物设计、RNA提取和RT-qPCR
根据NCBI GenBank发布的黄颡鱼基因预测序列, 利用NCBI primer-BLAST软件设计引物, 并交由上海生工生物工程有限公司合成, 引物序列见表 1。
表 1 引物信息Table 1. Primers information基因
Gene登录号
Accession No.引物序列
Primer Sequence (5′—3′)产物长度
Product length (bp)β-actin XM_027148463 CCTTGACTTCGAGCAGGAGA 115 GGGACACCTGAACCTCTCATT ef1α XM_027175544 CTACAACCCTGCTGCCGTT 144 TCCAGGAGAGTAGTGCCGC grp78 KM114873 CATCGAGCGCATGGTAAACG 113 GGTTCTTGAGCGAGTAGGCA ire1 KP687345 TACCTCGGACGCACAGAGTA 108 GTCATCGTCTGGAAGGGTGG perk KP687344 TGAGCCCAGAACAGTTGTCAG 109 CTCTCCATCTGTGTGCGGAA atf6 KP687343 CAGATCGTGACTGTGCCGTA 198 CGGTCTGCTTCCTCTGTTGT xbp1 XM_027162925 TGCAGGTTCAGACGTTGGAG 196 TCCAGAATGCCGAGCAAGAG traf2 XM_027143648 CAACAAGGTGCGTCAGTTGG 138 CGACGGGTGAAATCGGAGAT jnk MH663998.1 CTACTACGCCTTCTGCCTGG 144 GCCTGCAGCACAGTGAGTAT eif2a XM_027143563 TCACCAGGGATGGCACTTTG 198 GAAGGTTCGCATCACCCTGA chop MG685920 CAGAGTTGGAGGCGTGGTAT 129 AGCAGCTCTCCAAGACATCC beclin1 KY062770 ATTACCCAGCGTTCCTGTGG 107 ATCTCTGAAAGCGCAGACCC atg1a KY404999 ACAGCCAATCCGTTCCTGTT 192 GAGATGGCTGGTGAGGTCTG atg3 KY062769 TTGGGCAGTGGAATTAGCGA 146 CTTGCCTCAGCCTTCCACTT lc3a KY062773 TCGACTGCAACTGAACCCTAC 142 CTGGGAGGCATAGACCATGT nf-κb KF572025 CGTGGGAAAGTAAAGGCTCG 120 GCTGCATCTTCACTCTCACG tnf-α NM_001200172 TATGAGCCACACCGTCTCTC 107 TCGACTGGTAGCCTTTGTGT il-12 XM_007231707 TCCACCTCACGAGATGCTTT 143 ATCGCCTGCTGATCTTCTGA il-10 XM_027144360 GCACTTCGTTCTTCATACGCC 161 GGCAACACGGTCTCCAAGTA bcl2 KY053838 GCGCTTTATTACCGCTGCAC 199 CCGAACTCGAGGAAGACCAC baxα KY072819 CACCTGGACTCTGGACTACC 144 ACGACAGTGGTGAGAACTCC caspase3a KY072821 GAATCAGCGCAATGGTACGG 143 TGTGGTCATCCTTGGCAACT caspase9 KY053837 CCAGAAGGAGGTGATGCTCC 155 ACTCCACATGGACTGGCTTC TRIzol法提取组织总RNA, 微量紫外分光光仪测定RNA的浓度和纯度, 1%琼脂糖凝胶电泳检测所提RNA的质量。使用HiScript Ⅱ Q RT SuperMix合成cDNA, 使用ChamQ-SYBR-qPCR Master Mix进行RT-qPCR。每个反应体系为10 μL: cDNA (200 ng/µL)2 μL、2×ChamQ SYBR qPCR 5 μL、上下游引物各0.2 μL、ddH2O 2.6 μL。使用CFX96tm实时系统进行RT-qPCR, 扩增程序: 95℃, 30s; 95℃, 10s, 60℃, 30s, 40次循环; 95℃, 15s。熔融曲线65—95℃, 0.5℃/s。
1.9 数据分析
实验数据采用SPSS 26.0 软件进行统计分析, 数据用平均值±标准差(mean±SD)表示。用Shapiro-Wilk检验分析数据的正态性, 利用One-way ANOVA进行单因素方差分析, Duncan’s多重比较检验, P<0.05表示差异显著, P<0.01表示差异极显著。使用GraphPad Prism 5进行图形绘制。
2. 结果
2.1 黄颡鱼肠道上皮细胞分离纯化
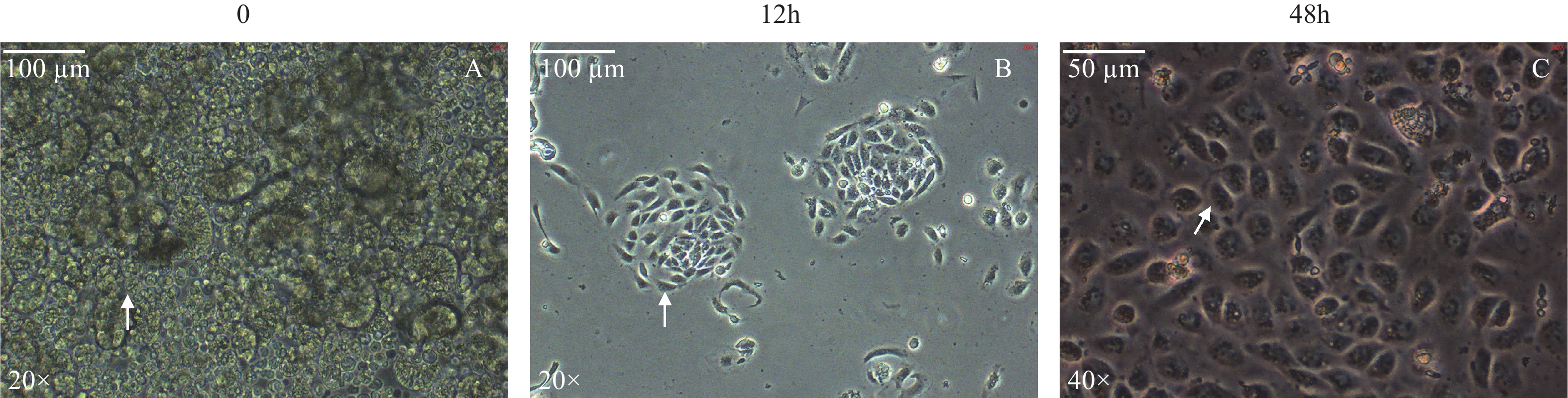
如图 1所示, 刚分离出来的细胞在显微镜下观察, 可见大量单细胞及细胞团(图 1A)。纯化后培养12h和48h, 去除未贴壁的细胞后在显微镜下观察, 可见贴壁的单细胞和细胞团, 且呈铺路石状(图 1B和图 1C)。未发现成纤维细胞。
![]() 图 1 分离得到的黄颡鱼肠道上皮细胞A. 培养0h, 放大倍数20×; B. 培养12h, 放大倍数20×; C. 培养48h, 放大倍数40×; 白色箭头: 分离得到的上皮细胞Figure 1. Isolated intestinal epithelial cells of hybrid yellow catfishA. Cells cultured for 0h, magnification 20×; B. Cells cultured for 12h, magnification 20×; C. Cells cultured for 48h, magnification 40×; White arrow: Isolated epithelial cells
图 1 分离得到的黄颡鱼肠道上皮细胞A. 培养0h, 放大倍数20×; B. 培养12h, 放大倍数20×; C. 培养48h, 放大倍数40×; 白色箭头: 分离得到的上皮细胞Figure 1. Isolated intestinal epithelial cells of hybrid yellow catfishA. Cells cultured for 0h, magnification 20×; B. Cells cultured for 12h, magnification 20×; C. Cells cultured for 48h, magnification 40×; White arrow: Isolated epithelial cells2.2 黄颡鱼肠道上皮细胞的鉴定
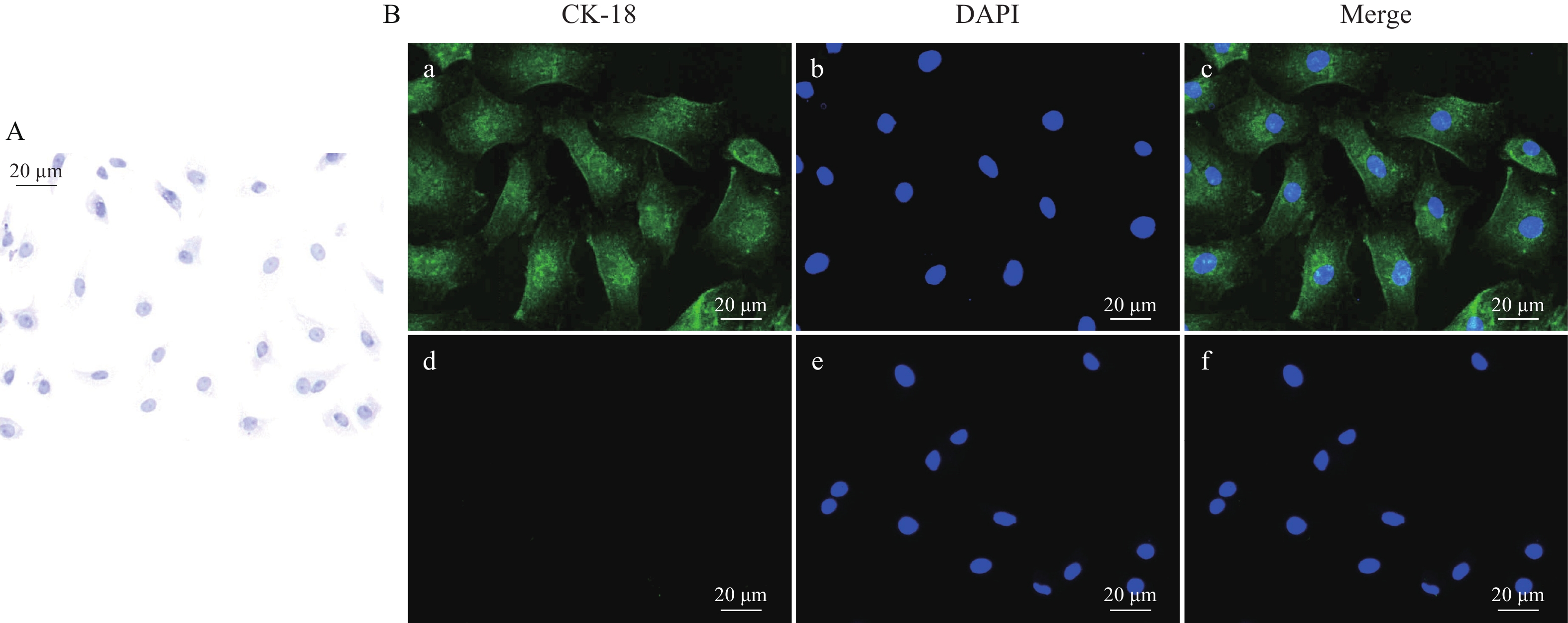
碱性磷酸酶染色和CK-18免疫荧光染色及结果如图 2所示, 结果表明碱性磷酸酶染色(图 2A)和CK-18 (图 2B)均呈阳性, 且CK-18染色中阴性对照无绿色荧光出现, 说明分离得到的细胞为黄颡鱼肠道上皮细胞。
![]() 图 2 黄颡鱼肠道上皮细胞鉴定A. 碱性磷酸酶染色; B. CK-18免疫荧光; a. 上皮细胞CK-18染色; b. 上皮细胞核染; c. 染色融合图; d. 阴性对照; e. 阴性对照核染; f. 阴性对照染色融合图Figure 2. Identification of intestinal epithelial cells of yellow catfishA. alkaline phosphatase staining; B. immunofluorescence of CK-18; a. epithelial cells with CK-18 staining; b. nuclear staining with DAPI; c. merged image; d. negative control; e. nuclear staining of negative control; f. merged image of negative control
图 2 黄颡鱼肠道上皮细胞鉴定A. 碱性磷酸酶染色; B. CK-18免疫荧光; a. 上皮细胞CK-18染色; b. 上皮细胞核染; c. 染色融合图; d. 阴性对照; e. 阴性对照核染; f. 阴性对照染色融合图Figure 2. Identification of intestinal epithelial cells of yellow catfishA. alkaline phosphatase staining; B. immunofluorescence of CK-18; a. epithelial cells with CK-18 staining; b. nuclear staining with DAPI; c. merged image; d. negative control; e. nuclear staining of negative control; f. merged image of negative control2.3 不同浓度β-伴大豆球蛋白对黄颡鱼肠道上皮细胞内质网、自噬、炎症和凋亡的影响
由图 3A 可知, 随着β-伴大豆球蛋白作用浓度的增加, 内质网应激标志蛋白GRP78的mRNA 表达水平显著上升(P<0.05), UPR信号通路起始因子ire1、perk的mRNA表达水平在4 mg/mL处理组显著上调(P<0.05), atf6 的mRNA表达水平则在2 mg/mL处理组达到最高后又显著下降至对照水平(P<0.05)。由图 3B可知, UPR通路关键因子traf2、eIF2A和chop基因mRNA表达均在4 mg/mL处理组显著最高(P<0.05)。xbp1基因mRNA表达水平在不同浓度β-伴大豆球蛋白处理组间无显著差异(P>0.05), 显著高于0组(P<0.05)。各处理组jnk基因mRNA表达水平在2 mg/mL处理组显著最高, 显著低于0组(P<0.05)。
![]() 图 3 不同浓度β-伴大豆球蛋白处理细胞24h后基因表达量A和B. 内质网应激相关基因, C. 自噬相关基因, D. 炎症相关基因, E. 凋亡相关基因; 柱上标注不同小写字母表示在不同处理间差异显著(P<0.05); 下同Figure 3. The expression of genes after 24h of treatment with different concentrations of β-conglycinin in cellsA and B. Genes related with endoplasmic reticulum stress, C. Genes related with autophagy, D. Genes related with inflammation, E. Genes related with apoptosis. Different lowercase letters indicate significant differences among treatments (P<0.05); The same applies below
图 3 不同浓度β-伴大豆球蛋白处理细胞24h后基因表达量A和B. 内质网应激相关基因, C. 自噬相关基因, D. 炎症相关基因, E. 凋亡相关基因; 柱上标注不同小写字母表示在不同处理间差异显著(P<0.05); 下同Figure 3. The expression of genes after 24h of treatment with different concentrations of β-conglycinin in cellsA and B. Genes related with endoplasmic reticulum stress, C. Genes related with autophagy, D. Genes related with inflammation, E. Genes related with apoptosis. Different lowercase letters indicate significant differences among treatments (P<0.05); The same applies below由图 3C可知, 自噬相关基因beclin1、atg1a、atg3和lc3a的mRNA表达量均随β-伴大豆球蛋白浓度的增加呈现显著上升后又显著下降的趋势(P<0.05)。其中beclin1、atg1a和atg3的mRNA表达量在2和4 mg/mL处理组显著最高, 显著高于其他处理组(P<0.05)。lc3a基因mRNA表达量则在4 mg/mL组显著最高(P<0.05)。β-伴大豆球蛋白浓度过高显著抑制lc3a和atg1a mRNA的表达(P<0.05)。
由图 3D和图 3E可知, 促炎因子nf-κb、tnf-α和il-12 mRNA表达量均随β-伴大豆球蛋白浓度升高呈先上升后下降趋势, 以4 mg/mL处理组最高, 显著高于0处理组(P<0.05), 凋亡相关基因baxα、bcl2和caspase9 mRNA表达量在4 mg/mL处理组最高(P<0.05)。il-10 mRNA的表达不受β-伴大豆球蛋白浓度的影响。
综合上述实验数据, 选取4 mg/mL β-伴大豆球蛋白浓度进行后续实验。
2.4 4 mg/mL β-伴大豆球蛋白对黄颡鱼肠道上皮细胞活性的影响
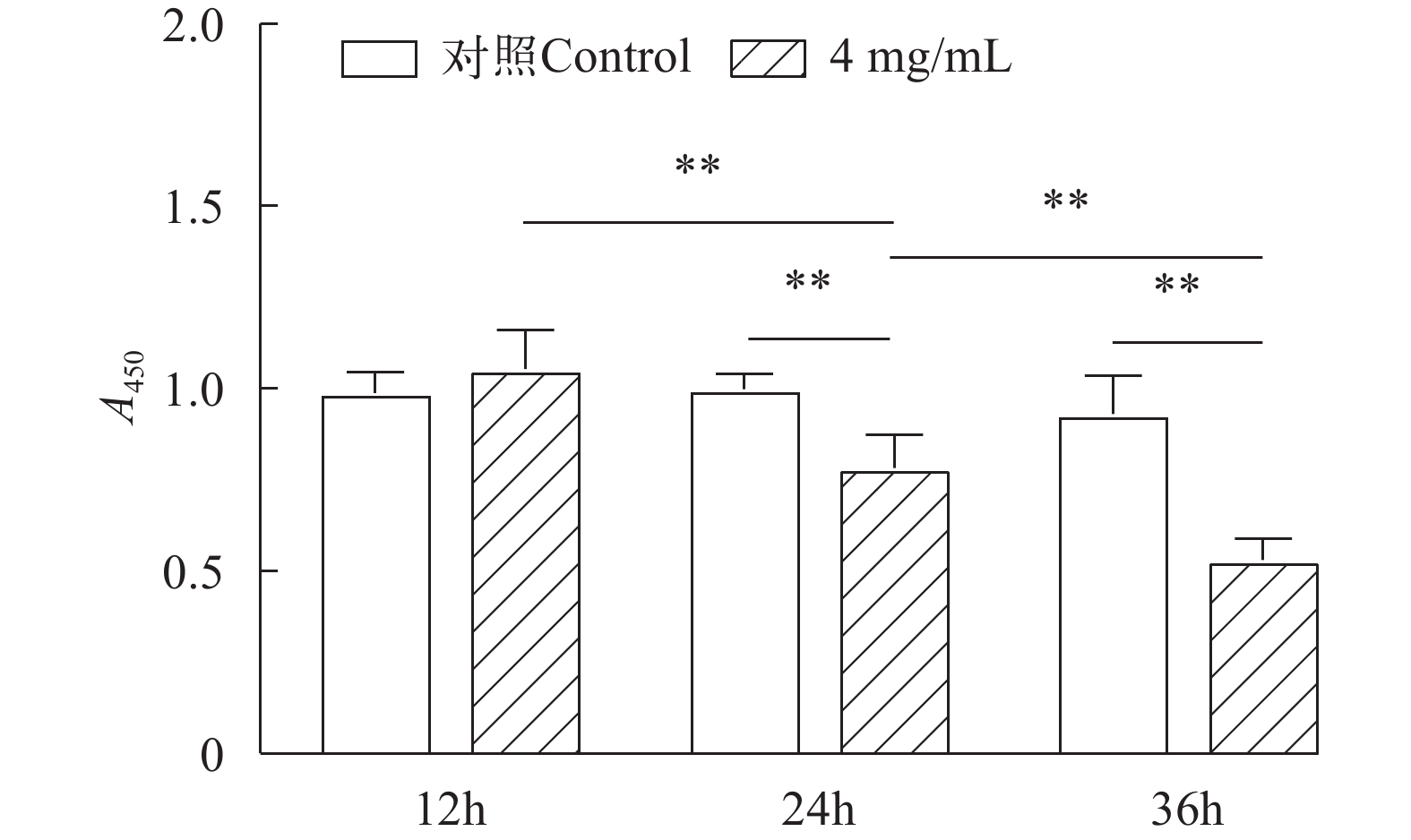
如图 4所示, 4 mg/mL β-伴大豆球蛋白浓度处理下, 细胞活性随着处理时间延长呈显著下降趋势(P<0.01)。与0处理组相比, 4 mg/mL β-伴大豆球蛋白浓度处理24h和36h的黄颡鱼肠道上皮细胞活力均极显著低于0处理组(P<0.01)。
2.5 β-伴大豆球蛋白对黄颡鱼肠道上皮细胞内质网应激相关基因的影响
如图 5所示, grp78 mRNA表达量随β-伴大豆球蛋白刺激时间延长显著上升(P<0.05), 在36h时显著最高, ire1 mRNA表达量则呈下降趋势, 并于36h时显著最低(P<0.05)。与刺激12h相比, perk mRNA表达量于刺激24h后显著升高并维持在此水平(P<0.05)。chop的mRNA水平在各时间点无显著差异(P>0.05)。
2.6 4 mg/mL β-伴大豆球蛋白对黄颡鱼肠道上皮细胞自噬和凋亡相关基因的影响
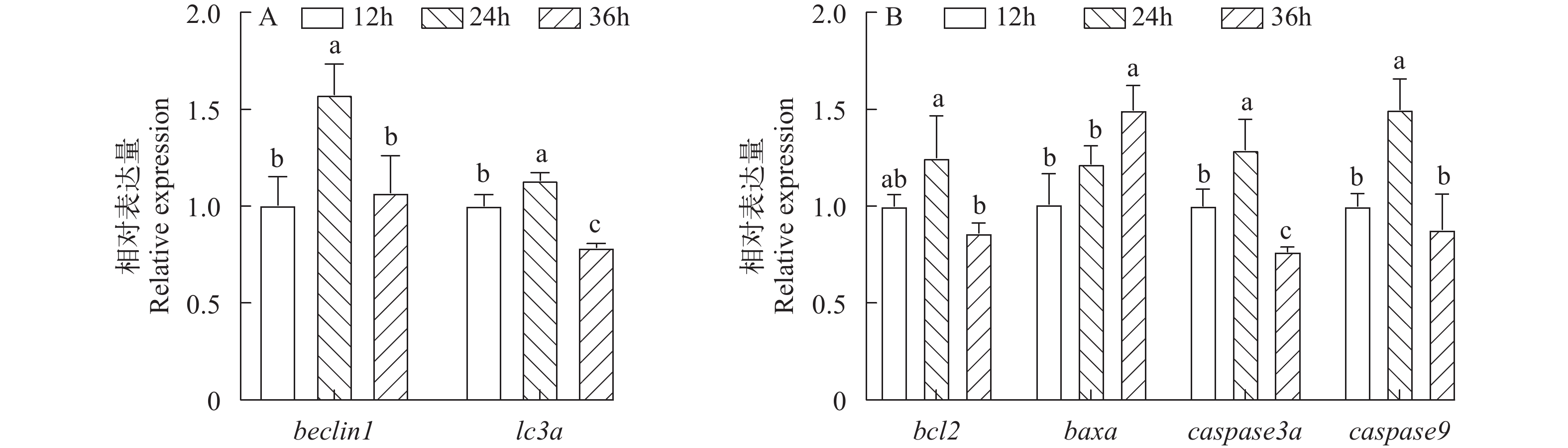
由图 6可知, 自噬相关基因beclin1和lc3a mRNA表达量均在24h显著最高(P<0.05)。其中beclin1的mRNA表达量于36h时下降至12h水平, lc3a mRNA表达量于36h时显著低于12h水平(P<0.05)。凋亡相关基因bcl2, caspase3a和caspase9的mRNA表达量均在24h时显著最高(P<0.05), baxα基因的mRNA表达量则36h时显著最高(P<0.05)。
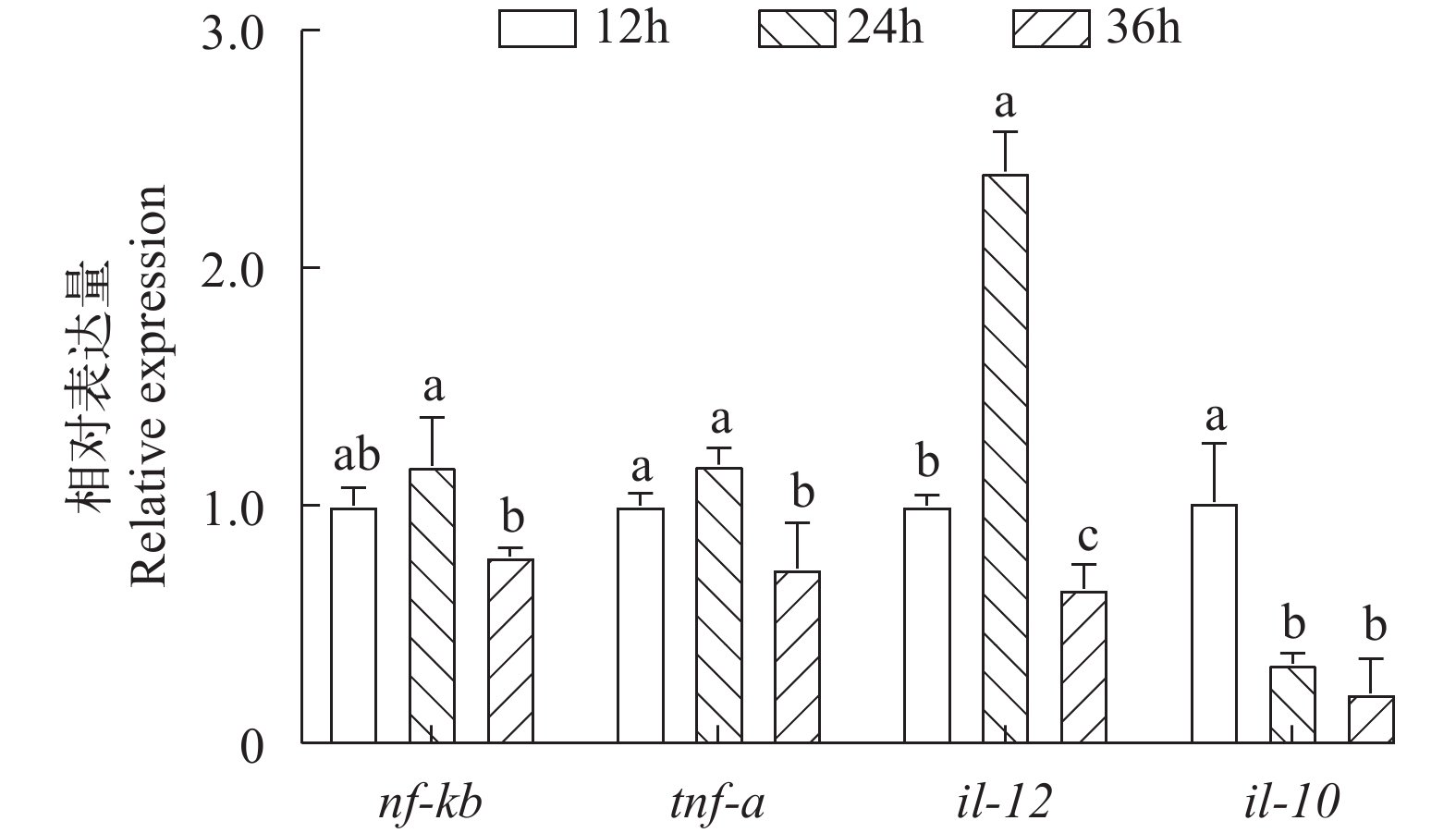
2.7 4 mg/mL β-伴大豆球蛋白对黄颡鱼肠道上皮细胞炎症相关因子mRNA表达的影响
由图 7可知, 除il-10外, 所有炎症因子相关基因mRNA表达量都在24h显著最高, 于36h显著最低, 显著低于12h时表达水平(P<0.05)。
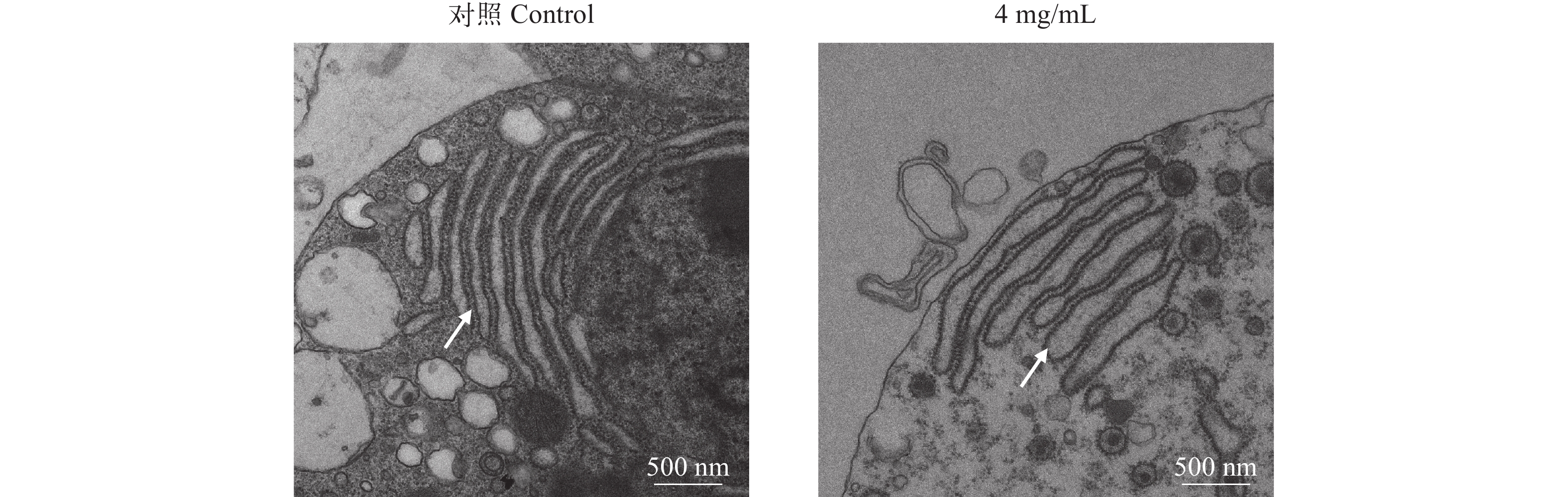
2.8 4 mg/mL β-伴大豆球蛋白对黄颡鱼肠道上皮细胞内质网结构的影响
如图 8所示, 与control组相比, 4 mg/mL β-伴大豆球蛋白处理黄颡鱼肠道上皮细胞24h后, 显著引起细胞内质网肿胀, 内质网应激发生。
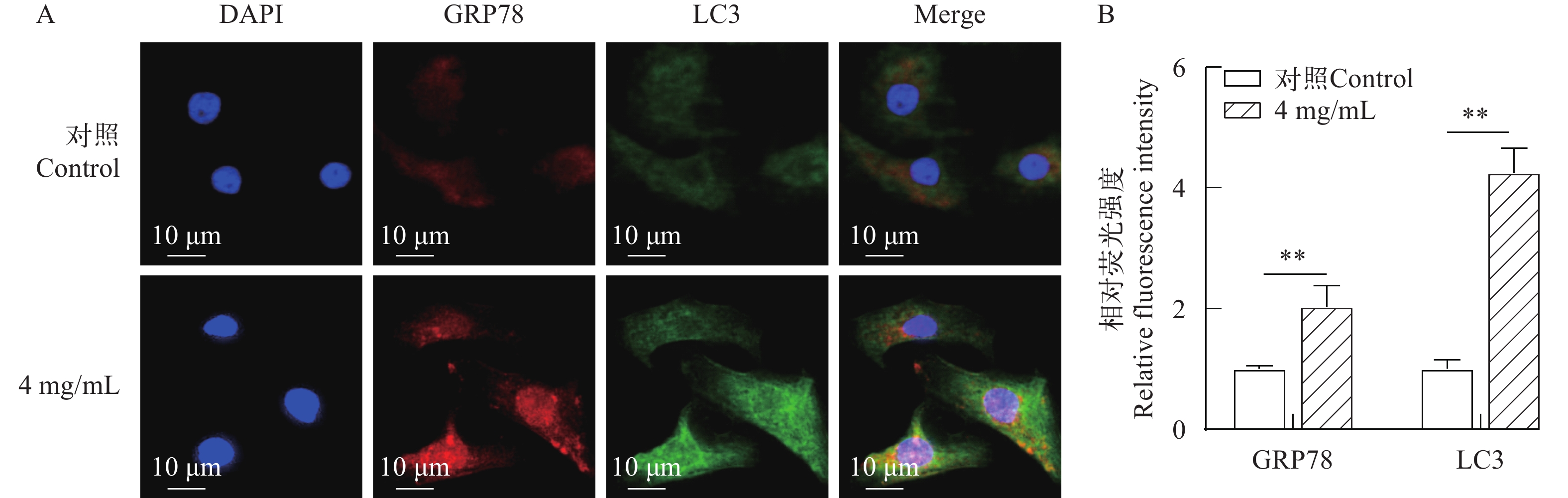
2.9 4 mg/mL β-伴大豆球蛋白对黄颡鱼肠道上皮细胞GRP78和LC3蛋白表达的影响
如图 9所示, 免疫荧光双染显示, 与对照组相比, 4 mg/mL β-伴大豆球蛋白刺激24h导致黄颡鱼肠道上皮细胞GRP78和LC3蛋白表达极显著升高(P<0.01)。
![]() 图 9 4 mg/mL β-伴大豆球蛋白处理细胞24h后GRP78和LC3免疫荧光染色A. GRP78和LC3双染免疫荧光; B. 免疫荧光强度量化; **表示差异极显著(P<0.01)Figure 9. Immunofluorescence intensity of GRP78 and LC3 in cells suffered 24h of 4 mg/mL β-conglycinin stimulationA. Immunofluorescence of GRP78 and LC3; B. Immunofluorescence intensity quantification; **indicates extremely significant difference (P<0.01)
图 9 4 mg/mL β-伴大豆球蛋白处理细胞24h后GRP78和LC3免疫荧光染色A. GRP78和LC3双染免疫荧光; B. 免疫荧光强度量化; **表示差异极显著(P<0.01)Figure 9. Immunofluorescence intensity of GRP78 and LC3 in cells suffered 24h of 4 mg/mL β-conglycinin stimulationA. Immunofluorescence of GRP78 and LC3; B. Immunofluorescence intensity quantification; **indicates extremely significant difference (P<0.01)2.10 4 mg/mL β-伴大豆球蛋白对黄颡鱼肠道上皮细胞凋亡相关蛋白的影响
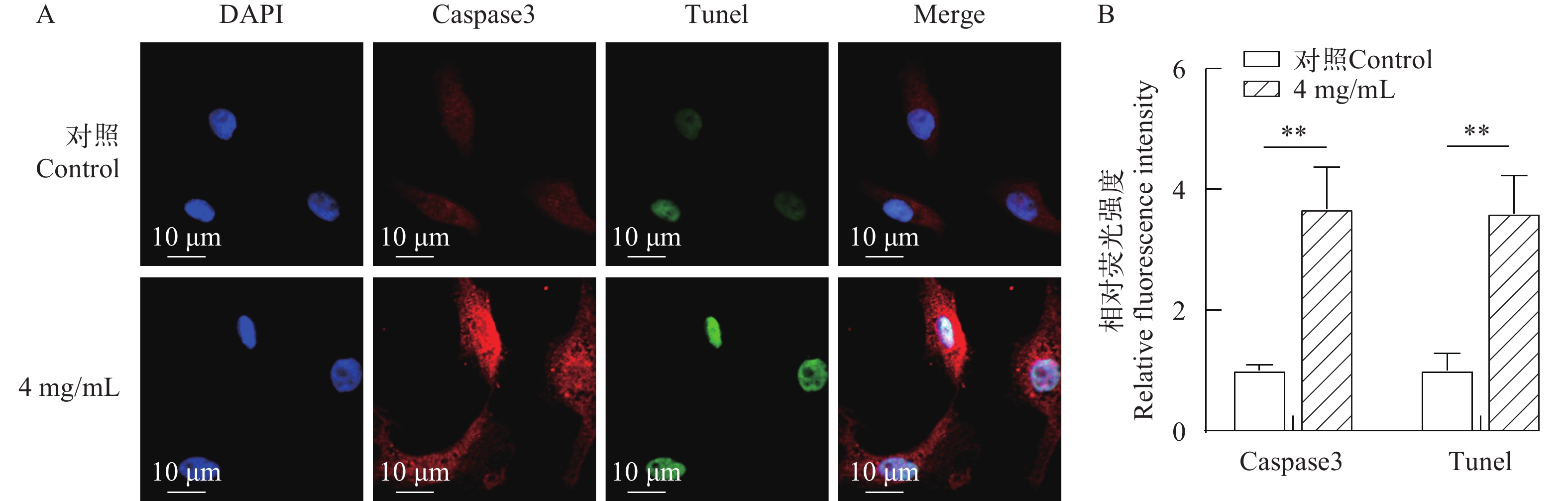
由图 10所示, 免疫荧光双染结果显示4 mg/mL的β-伴大豆球蛋白处理黄颡鱼上皮细胞24h能极显著增加凋亡相关蛋白Caspase3的表达和细胞凋亡水平(P<0.01)。
![]() 图 10 4 mg/mL β-伴大豆球蛋白处理细胞24h后Caspase3和Tunel免疫荧光染色A. Caspase3和Tunel双染免疫荧光, B. 免疫荧光强度量化; **表示差异极显著(P<0.01)Figure 10. Immunofluorescence intensity of Caspase3 and Tunel in cells suffered 24h of 4 mg/mL β-conglycinin stimulationA. Immunofluorescence of Caspase3 and Tunel, B. Immunofluorescence intensity quantification; **indicates extremely significant difference (P<0.01)
图 10 4 mg/mL β-伴大豆球蛋白处理细胞24h后Caspase3和Tunel免疫荧光染色A. Caspase3和Tunel双染免疫荧光, B. 免疫荧光强度量化; **表示差异极显著(P<0.01)Figure 10. Immunofluorescence intensity of Caspase3 and Tunel in cells suffered 24h of 4 mg/mL β-conglycinin stimulationA. Immunofluorescence of Caspase3 and Tunel, B. Immunofluorescence intensity quantification; **indicates extremely significant difference (P<0.01)3. 讨论
在以鱼类肠道上皮细胞为模型的研究中, 大都采用分离原代肠道上皮细胞的方法, 如黄姑鱼(Nibea albiflora)[19]、鲫(Carassius auratus)[20]和草鱼[21]等。在本研究中, 我们参照其他鱼类原代肠道上皮细胞的分离培养方法, 并进行进一步改良, 将3种消化酶使用比例进行调整, 通过混合酶消化法成功分离得到了黄颡鱼肠道上皮细胞。分离得到的肠上皮细胞呈铺路石状, 这与在黄姑鱼、鲫、草鱼等中观察到的形态相一致[19—21]。CK-18是肠道上皮细胞的主要骨架蛋白, 具有高度的保守性, 常用于肠道上皮细胞的鉴定[22]; 碱性磷酸酶是肠道上皮细胞微绒毛的标志性酶, 是鉴定肠上皮细胞的一个标志物[23]。本实验中CK-18免疫荧光染色和碱性磷酸酶染色结果皆为阳性, 进一步证明分离得到的细胞为黄颡鱼肠道上皮细胞。
相关研究数据显示, β-伴大豆球蛋白引起肠道损伤的程度受剂量和刺激时间的影响。如Li等[24]研究发现随着日粮β-伴大豆球蛋白添加量(20—80 g/kg)的增加, 鲫前肠中炎症因子tnf-α和il-1β的mRNA表达量先上升后下降, 以60 g/kg添加组中表达量最高; Kang等[25]通过口服给药β-伴大豆球蛋白, 发现与0h相比, 肉鸡雏鸡十二指肠il-8的mRNA表达量于1h显著降低, 于12h最高, 同时在12h的样品中观察到肠绒毛显著受损。因此为了探索黄颡鱼肠道上皮细胞内质网对不同浓度β-伴大豆球蛋白的响应, 本实验设置了0、2、4、8和12 mg/mL不同浓度β-伴大豆球蛋白处理组, 刺激黄颡鱼肠道上皮细胞24h, 从内质网角度探讨不同浓度β-伴大豆球蛋白对黄颡鱼肠道上皮细胞的影响。结果显示, 内质网应激标志基因grp78的mRNA表达量随β-伴大豆球蛋白浓度的升高而上升。除atf6外, UPR信号通路起始因子(ire1和perk)、UPR信号通路下游转录因子(traf2、xbp1、jnk、eif2a和chop)、自噬(beclin1、atg1a、atg3和lc3a)、炎症(nf-κb, tnf-α和il-12)及凋亡(baxα, bcl2和caspase9)相关基因的表达水平均在4 mg/mL处理组显著达到最高, β-伴大豆球蛋白浓度超过4 mg/mL时, 相关基因表现出下降的趋势。推测可能因过高的β-伴大豆球蛋白刺激浓度所致。过高浓度的β-伴大豆球蛋白损害黄颡鱼肠道黏膜细胞功能, 导致功能的低反应性, 反应为UPR轴、自噬、凋亡、炎症等相关因子mRNA转录水平的低表达。因刺激物浓度过高导致机体细胞生理功能低反应在Luo等[26]研究也有报道, 即饲料中使用β-伴大豆球蛋白替代鱼粉(40—160 g/kg), 60 g/kg添加组鲤肠道炎症因子mRNA表达量著达最高, 后随β-伴大豆球蛋白浓度的升高而显著下降。综上所述, 本研究认为4 mg/mL β-伴大豆球蛋白可有效引起黄颡鱼肠道上皮细胞内质网应激及相应反应。
为进一步验证上述结论, 本研究使用4 mg/mL的β-伴大豆球蛋白分别刺激黄颡鱼肠道上皮细胞, 在12h、24h和36h取样进行检测。CCK-8细胞活性实验表明, 4 mg/mL β-伴大豆球蛋白浓度刺激下黄颡鱼肠道上皮细胞的活性显著受处理时间的影响, 并随处理时间的延长显著下降, 在24h时和36h时显著低于对照组。这与Liu等[27]的研究结果相一致, 随着1 mg/mL β-伴大豆球蛋白处理时间的延长, 鱼类肠道上皮细胞的活性显著下降。
结合上述不同浓度β-伴大豆球蛋白刺激实验数据, 选取24h样品进行透射电镜观察, 结果显示4 mg/mL β-伴大豆球蛋白刺激24h显著引起黄颡鱼肠道上皮细胞内质网应激, 内质网明显发生肿胀。对不同取样时间点样品进行内质网应激相关基因表达水平检测, 发现内质网应激标志基因grp78和UPR信号通路起始因子perk的mRNA表达量随β-伴大豆球蛋白处理时间的增长而增加, 分别在36h和24h达到最高。UPR信号通路起始因子atf6、自噬(beclin1和lc3a)、凋亡(bcl2, caspase3和caspase9)和炎症因子(nf-κb, tnf-α和il-12)相关基因mRNA表达量表则均在24h表达量显著最高, 这与上述不同浓度β-伴大豆球蛋白对黄颡鱼肠道上皮细胞的影响实验中相关基因的表达均在4 mg/mL β-伴大豆球蛋白处理组表现最高的结果相一致。进一步证明了使用4 mg/mL β-伴大豆球蛋白刺激黄颡鱼肠道原代细胞24h构建内质网应激模型的可行性。
利用免疫荧光双染法进一步对4 mg/mL β-伴大豆球蛋白刺激24h的黄颡鱼肠道上皮细胞中内质网应激标志基因GRP78、自噬标志蛋白LC3的蛋白表达水平进行检测, 同时对细胞进行Caspase3蛋白和Tunel染色。结果显示, 与对照组相比, 4 mg/mL β-伴大豆球蛋白处理组的黄颡鱼肠道上皮细胞GRP78和LC3蛋白表达显著升高, 凋亡相关蛋白Caspase3的表达和细胞凋亡信号显著增多。自噬是内质网应激期间必不可少的保护机制, 内质网应激初期时可引发细胞自噬, 缓解内质网应激[28]。Liu等[29]研究发现, 鲤在含有As2O3的水体中养殖能够造成鳃组织的内质网应激, 同时自噬标志物Beclin1和LC3-Ⅱ表达上调, 自噬水平增强。细胞凋亡是内质网应激过强时的一种保护机制, 当过度或者长期处于内质网应激时, 细胞将启动凋亡, 清除多余的受损细胞, 减少组织受损。有研究表明, 内质网应激可以直接促凋亡分子Bax的表达, 诱导Caspase9活化, 激活Caspase3导致细胞最终凋亡[30]。在本研究中, 细胞在经过4 mg/mL β-伴大豆球蛋白处理24h后内质网应激、自噬和凋亡相关基因mRNA表达量显著最多, 后续免疫荧光结果与荧光定量结果一致, 证明了4 mg/mL 的β-伴大豆球蛋白能够成功构建黄颡鱼肠道上皮细胞内质网应激模型。综上所述, 本研究使用4 mg/mL β-伴大豆球蛋白处理24h细胞, 成功构建了黄颡鱼肠道上皮细胞内质网应激和自噬模型。
4. 结论
本研究通过酶消化法成功分离得到黄颡鱼肠道上皮细胞, 并使用β-伴大豆球蛋白成功构建了内质网应激模型。通过RT-qPCR、透射电镜和免疫荧光染色等手段, 发现4 mg/mL β-伴大豆球蛋白处理黄颡鱼肠道上皮细胞24h能显著引起内质网应激, 表现为细胞内质网的肿胀, UPR信号通路关键基因、炎症、自噬、凋亡等相关基因的高表达, 黄颡鱼肠道上皮细胞自噬与凋亡水平升高。本实验为研究内质网应激及UPR信号通路在鱼类SBMIE发生发展中的作用机制提供可用的离体模型, 为进一步挖掘基于内质网应激的鱼类炎性肠病调控靶点的研究提供前期基础。
-
图 1 分离得到的黄颡鱼肠道上皮细胞
A. 培养0h, 放大倍数20×; B. 培养12h, 放大倍数20×; C. 培养48h, 放大倍数40×; 白色箭头: 分离得到的上皮细胞
Figure 1. Isolated intestinal epithelial cells of hybrid yellow catfish
A. Cells cultured for 0h, magnification 20×; B. Cells cultured for 12h, magnification 20×; C. Cells cultured for 48h, magnification 40×; White arrow: Isolated epithelial cells
图 2 黄颡鱼肠道上皮细胞鉴定
A. 碱性磷酸酶染色; B. CK-18免疫荧光; a. 上皮细胞CK-18染色; b. 上皮细胞核染; c. 染色融合图; d. 阴性对照; e. 阴性对照核染; f. 阴性对照染色融合图
Figure 2. Identification of intestinal epithelial cells of yellow catfish
A. alkaline phosphatase staining; B. immunofluorescence of CK-18; a. epithelial cells with CK-18 staining; b. nuclear staining with DAPI; c. merged image; d. negative control; e. nuclear staining of negative control; f. merged image of negative control
图 3 不同浓度β-伴大豆球蛋白处理细胞24h后基因表达量
A和B. 内质网应激相关基因, C. 自噬相关基因, D. 炎症相关基因, E. 凋亡相关基因; 柱上标注不同小写字母表示在不同处理间差异显著(P<0.05); 下同
Figure 3. The expression of genes after 24h of treatment with different concentrations of β-conglycinin in cells
A and B. Genes related with endoplasmic reticulum stress, C. Genes related with autophagy, D. Genes related with inflammation, E. Genes related with apoptosis. Different lowercase letters indicate significant differences among treatments (P<0.05); The same applies below
图 9 4 mg/mL β-伴大豆球蛋白处理细胞24h后GRP78和LC3免疫荧光染色
A. GRP78和LC3双染免疫荧光; B. 免疫荧光强度量化; **表示差异极显著(P<0.01)
Figure 9. Immunofluorescence intensity of GRP78 and LC3 in cells suffered 24h of 4 mg/mL β-conglycinin stimulation
A. Immunofluorescence of GRP78 and LC3; B. Immunofluorescence intensity quantification; **indicates extremely significant difference (P<0.01)
图 10 4 mg/mL β-伴大豆球蛋白处理细胞24h后Caspase3和Tunel免疫荧光染色
A. Caspase3和Tunel双染免疫荧光, B. 免疫荧光强度量化; **表示差异极显著(P<0.01)
Figure 10. Immunofluorescence intensity of Caspase3 and Tunel in cells suffered 24h of 4 mg/mL β-conglycinin stimulation
A. Immunofluorescence of Caspase3 and Tunel, B. Immunofluorescence intensity quantification; **indicates extremely significant difference (P<0.01)
表 1 引物信息
Table 1 Primers information
基因
Gene登录号
Accession No.引物序列
Primer Sequence (5′—3′)产物长度
Product length (bp)β-actin XM_027148463 CCTTGACTTCGAGCAGGAGA 115 GGGACACCTGAACCTCTCATT ef1α XM_027175544 CTACAACCCTGCTGCCGTT 144 TCCAGGAGAGTAGTGCCGC grp78 KM114873 CATCGAGCGCATGGTAAACG 113 GGTTCTTGAGCGAGTAGGCA ire1 KP687345 TACCTCGGACGCACAGAGTA 108 GTCATCGTCTGGAAGGGTGG perk KP687344 TGAGCCCAGAACAGTTGTCAG 109 CTCTCCATCTGTGTGCGGAA atf6 KP687343 CAGATCGTGACTGTGCCGTA 198 CGGTCTGCTTCCTCTGTTGT xbp1 XM_027162925 TGCAGGTTCAGACGTTGGAG 196 TCCAGAATGCCGAGCAAGAG traf2 XM_027143648 CAACAAGGTGCGTCAGTTGG 138 CGACGGGTGAAATCGGAGAT jnk MH663998.1 CTACTACGCCTTCTGCCTGG 144 GCCTGCAGCACAGTGAGTAT eif2a XM_027143563 TCACCAGGGATGGCACTTTG 198 GAAGGTTCGCATCACCCTGA chop MG685920 CAGAGTTGGAGGCGTGGTAT 129 AGCAGCTCTCCAAGACATCC beclin1 KY062770 ATTACCCAGCGTTCCTGTGG 107 ATCTCTGAAAGCGCAGACCC atg1a KY404999 ACAGCCAATCCGTTCCTGTT 192 GAGATGGCTGGTGAGGTCTG atg3 KY062769 TTGGGCAGTGGAATTAGCGA 146 CTTGCCTCAGCCTTCCACTT lc3a KY062773 TCGACTGCAACTGAACCCTAC 142 CTGGGAGGCATAGACCATGT nf-κb KF572025 CGTGGGAAAGTAAAGGCTCG 120 GCTGCATCTTCACTCTCACG tnf-α NM_001200172 TATGAGCCACACCGTCTCTC 107 TCGACTGGTAGCCTTTGTGT il-12 XM_007231707 TCCACCTCACGAGATGCTTT 143 ATCGCCTGCTGATCTTCTGA il-10 XM_027144360 GCACTTCGTTCTTCATACGCC 161 GGCAACACGGTCTCCAAGTA bcl2 KY053838 GCGCTTTATTACCGCTGCAC 199 CCGAACTCGAGGAAGACCAC baxα KY072819 CACCTGGACTCTGGACTACC 144 ACGACAGTGGTGAGAACTCC caspase3a KY072821 GAATCAGCGCAATGGTACGG 143 TGTGGTCATCCTTGGCAACT caspase9 KY053837 CCAGAAGGAGGTGATGCTCC 155 ACTCCACATGGACTGGCTTC -
[1] Solis A G, Klapholz M, Zhao J, et al. The bidirectional nature of microbiome-epithelial cell interactions [J]. Current Opinion in Microbiology, 2020(56): 45-51.
[2] Rahimnejad S, Lu K, Wang L, et al. Replacement of fish meal with Bacillus pumillus SE5 and Pseudozyma aphidis ZR1 fermented soybean meal in diets for Japanese seabass (Lateolabrax japonicus) [J]. Fish & Shellfish Immunology, 2019(84): 987-997.
[3] Zhou Z, Ringø E, Olsen R E, et al. Dietary effects of soybean products on gut microbiota and immunity of aquatic animals: a review [J]. Aquaculture Nutrition, 2018, 24(1): 644-665. doi: 10.1111/anu.12532
[4] Liu Z Y, Yang H L, Li S, et al. Probiotic components of Bacillus siamensis LF4 mitigated β-conglycinin caused cell injury via modulating TLR2/MAPKs/NF-κB signaling in Lateolabrax maculatus [J]. Fish & Shellfish Immunology, 2023(141): 109010.
[5] Zhang J-X, Guo L-Y, Feng L, et al. Soybean β-conglycinin induces inflammation and oxidation and causes dysfunction of intestinal digestion and absorption in fish [J]. PLoS One, 2013, 8(3): e58115. doi: 10.1371/journal.pone.0058115
[6] Li Y, Hu H, Liu J, et al. Dietary soya allergen β-conglycinin induces intestinal inflammatory reactions, serum-specific antibody response and growth reduction in a carnivorous fish species, turbot Scophthalmus maximus L [J]. Aquaculture Research, 2017, 48(8): 4022-4037. doi: 10.1111/are.13224
[7] Zhang Y L, Jiang W D, Duan X D, et al. Soybean glycinin caused NADPH-oxidase-regulated ROS overproduction and decreased ROS elimination capacity in the mid and distal intestine of juvenile grass carp (Ctenopharyngodon idella) [J]. Aquaculture, 2020(516): 734651.
[8] Stengel S T, Fazio A, Lipinski S, et al. Activating transcription factor 6 mediates inflammatory signals in intestinal epithelial cells upon endoplasmic reticulum stress [J]. Gastroenterology, 2020, 159(4): 1357-1374. doi: 10.1053/j.gastro.2020.06.088
[9] Adolph T E, Niederreiter L, Blumberg R S, et al. Endoplasmic reticulum stress and inflammation [J]. Digestive Diseases, 2012, 30(4): 341-346. doi: 10.1159/000338121
[10] Hosomi S, Grootjans J, Tschurtschenthaler M, et al. Intestinal epithelial cell endoplasmic reticulum stress promotes MULT1 up-regulation and NKG2D-mediated inflammation [J]. The Journal of Experimental Medicine, 2017, 214(10): 2985-2997. doi: 10.1084/jem.20162041
[11] Ibrahim I M, Abdelmalek D H, Elfiky A A. GRP78: a cell’s response to stress [J]. Life Sciences, 2019(226): 156-163.
[12] Kokame K, Kato H, Miyata T. Identification of ERSE-Ⅱ, a new cis-acting element responsible for the ATF6-dependent mammalian unfolded protein response [J]. Journal of Biological Chemistry, 2001, 276(12): 9199-9205. doi: 10.1074/jbc.M010486200
[13] Coleman O I, Haller D. ER stress and the UPR in shaping intestinal tissue homeostasis and immunity [J]. Frontiers in Immunology, 2019(10): 2825.
[14] Tan Y R, Shen S Y, Shen H Q, et al. The role of endoplasmic reticulum stress in regulation of intestinal barrier and inflammatory bowel disease [J]. Experimental Cell Research, 2023, 424(1): 113472. doi: 10.1016/j.yexcr.2023.113472
[15] Solà Tapias N, Denadai-Souza A, Rolland-Fourcade C, et al. Colitis linked to endoplasmic reticulum stress induces trypsin activity affecting epithelial functions [J]. Journal of Crohn’s & Colitis, 2021, 15(9): 1528-1541.
[16] Xia T, Mao X J, Zhang J, et al. Effects of quercetin and hydroxytyrosol supplementation in a high-fat diet on growth, lipid metabolism, and mitochondrial function in spotted seabass (Lateolabrax maculatus) [J]. Aquaculture, 2024(582): 740538.
[17] Zhao L, Liang J, Chen F, et al. High carbohydrate diet induced endoplasmic reticulum stress and oxidative stress, promoted inflammation and apoptosis, impaired intestinal barrier of juvenile largemouth bass (Micropterus salmoides) [J]. Fish & Shellfish Immunology, 2021(119): 308-317.
[18] Li W J, Wu H X, Zhang L, et al. Effects of replacing soybean meal protein with cottonseed protein concentrate on the growth condition and intestinal health of Nile tilapia (Oreochromis niloticus) [J]. Aquaculture Nutrition, 2021, 27(6): 2436-2447. doi: 10.1111/anu.13375
[19] 王立改, 曾延清, 汪波, 等. 黄姑鱼肠道上皮细胞体外分离培养及鉴定 [J]. 动物营养学报, 2022, 34(2): 1296-1304. doi: 10.3969/j.issn.1006-267x.2022.02.061 Wang L G, Zeng Y Q, Wang B, et al. Isolation, culture and identification of intestinal epithelial cells of Nibea albiflora in vitro [J]. Chinese Journal of Animal Nutrition, 2022, 34(2): 1296-1304. doi: 10.3969/j.issn.1006-267x.2022.02.061
[20] 宋增福, 吴天星, 潘晓东. 鲫肠道上皮细胞原代培养方法的研究 [J]. 淡水渔业, 2008, 38(1): 67-69. doi: 10.3969/j.issn.1000-6907.2008.01.016 Song Z F, Wu T X, Pan X D. Study primary culture methods of intestinal epithelial cells of crucian carp (Carassius auratus) [J]. Freshwater Fisheries, 2008, 38(1): 67-69. doi: 10.3969/j.issn.1000-6907.2008.01.016
[21] 姚仕彬, 叶元土, 蔡春芳, 等. 草鱼肠道粘膜上皮细胞的分离与原代培养 [J]. 上海海洋大学学报, 2013, 22(1): 33-41. Yao S B, Ye Y T, Cai C F, et al. Dissociation and primary culture of Ctenopharyngodon idellus intestinal epithelial cells [J]. Journal of Shanghai Ocean University, 2013, 22(1): 33-41.
[22] Zhan K, Lin M, Zhao Q M, et al. Biological characterization of bovine mammary epithelial cell lines immortalized by HPV16 E6/E7 and SV40T [J]. In Vitro Cellular & Developmental Biology Animal, 2016, 52(9): 906-910.
[23] 李莎, 刘紫严, 杨红玲, 等. 花鲈肠上皮细胞原代培养及鉴定方法的探讨研究 [J]. 水产科学, 2023, 1-12. Li S, Liu Z Y, Yang H L, et al. Study on primary culture and identification of intestinal epithelial cells in Lateolabrax maculatus [J]. Fishery Sciences, 2023, 1-12
[24] Li L, Li M, Zhu R, et al. Effects of β-conglycinin on growth performance, antioxidant capacity and intestinal health in juvenile golden crucian carp, Carassius auratus [J]. Aquaculture Research, 2019, 50(11): 3231-3241. doi: 10.1111/are.14278
[25] Kang D R, Belal S A, Song K D, et al. Soybean β-conglycinin induces intestinal immune responses in chicks [J]. Brazilian Journal of Poultry Science, 2020, 22(2).
[26] Luo Q, Zhou Z, Zhao J, et al. Dietary β-conglycinin induces intestinal enteritis and affects glycerophospholipid and arginine metabolism in mirror carp (Cyprinus carpio) [J]. Aquaculture, 2023(567): 739257.
[27] Liu Z Y, Yang H L, Ding X Y, et al. Commensal Bacillus siamensis LF4 ameliorates β-conglycinin induced inflammation in intestinal epithelial cells of Lateolabrax maculatus [J]. Fish & Shellfish Immunology, 2023(137): 108797.
[28] Yang X, Srivastava R, Howell S H, et al. Activation of autophagy by unfolded proteins during endoplasmic reticulum stress [J]. The Plant Journal, 2016, 85(1): 83-95. doi: 10.1111/tpj.13091
[29] Liu Y, Zhao H, Yin K, et al. The protective effect of Zn2+ on As3+ toxicity in common carp: resistance to oxidative stress, inhibition of endoplasmic reticulum stress, apoptosis and autophagy [J]. Aquaculture, 2022(546): 737375.
[30] Xiong Z, Jiang R, Li X, et al. Different roles of GRP78 on cell proliferation and apoptosis in cartilage development [J]. International Journal of Molecular Sciences, 2015, 16(9): 21153-21176. doi: 10.3390/ijms160921153



 下载:
下载: