GENETIC DIFFERENTIATION AND LOCAL ADAPTATION OF CHINESE LENOK (BRACHYMYSTAX) POPULATIONS BASED ON WHOLE GENOME INDELS
-
摘要:
为了从全基因组InDel角度进行全国地理尺度细鳞鲑属遗传分化与适应性研究, 文章对采自陕西、甘肃、新疆、河北和黑龙江的6个细鳞鲑群体(共90尾样本)进行建库测序及InDel检测分析。结果表明: 6个细鳞鲑群体共检测到3056034个高质量InDel突变位点, 缺失位点数大于插入位点数, 将各基因区域标准化后观察到内含子区富集到相对更多的InDel位点。所有系统发育树分支中共统计到1715464个固定的InDel, 占总数的56.08%, 且主要位于每个谱系的基部。群体结构分析结果显示每个细鳞鲑地理群体均具有相对独立的遗传结构。适应性分析方面: 利用群体分支统计方法检测到秦岭地区细鳞鲑适应性相关的621个候选受选择基因, 并筛选到两个影响外显子序列的缺失位点, 分别导致insr和dnhd1缺失了两个和一个氨基酸密码子。对所有候选受选择基因的富集分析结果显示主要在神经发育和代谢等途径发挥作用。研究可为秦岭细鳞鲑山区溪流生境适应性候选基因的深入挖掘及人工增殖和保护中分子标记的开发提供基础资料, 也为进一步厘清细鳞鲑属物种分化提供参考。
Abstract:To study the genetics and evolution of the genus Brachymystax at the national geographic scale from the perspective of InDel in genome-wide, we employed whole genome resequencing and InDel detection analysis on six Brachymystax populations (a total of 90 samples) collected from Shaanxi, Gansu, Xinjiang, Hebei and Heilongjiang. The aim was to provide new insights into the genetic differentiation and local adaptation of Brachymystax populations through the perspective of InDels. Results showed the detection of a total of 3056034 high-quality InDel mutation sites among the six Brachymystax populations, with deletions exceeding insertions. After standardizing various gene regions, it was observed that intronic regions exhibited a relatively higher concentration of InDel sites. A total of 1715464 fixed InDels were identified in all branches of the phylogenetic tree, accounting for 56.08% of the total, primarily situated at the base of each lineage. Population structure analysis revealed that each geographic population of Brachymystax displayed a relatively distinct genetic structure. Regarding adaptive analysis, 621 candidate selection genes associated with local adaptation were detected using population branch statistics. Notably, two deletions affecting exonic sequences were identified, resulting in the loss of two and one amino acid codons in insr and dnhd1, respectively. Enrichment analysis of all potentially selective genes highlighted their significant involvement in pathways such as neural development and metabolism. This study provides foundational information for the comprehensive exploration of candidate adaptive genes in the mountain stream habitats of Qinling lenok, alongside facilitating the development of molecular markers for artificial breeding and conservation efforts. Additionally, it serves as a reference for further clarification of species differentiation within the genus Brachymystax.
-
Keywords:
- InDel /
- Whole genome resequencing /
- Population structure /
- Local adaptation /
- Brachymystax
-
细鳞鲑属(Brachymystax spp.)隶属于鲑形目(Salmoniforms)鲑科(Salmonidae), 是我国北方重要的珍稀鱼类, 在我国主要分布于东北地区的黑龙江、图们江、鸭绿江, 以及河北滦河、新疆额尔齐斯河、甘肃和陕西的渭河支流上游等[1—3], 由于独特的点状分布格局且各分布地间明显的地理隔离, 不同地区的细鳞鲑可能已经形成了地区性的独立遗传结构[4, 5]。细鳞鲑主要有两种生态型: 生活于平坦宽阔河流中的“江细鳞”和生活于山涧狭窄溪流的“山细鳞”, 均分布于人迹稀少的冷水性水系, 由于全球气候变化、水利工程建设开发及过度捕捞等导致其野生资源量锐减, 其中秦岭细鳞鲑(B. lenok tsinlingensis)1988年列为国家“Ⅱ”保护重点野生动物[6], 2021年该属所有鱼类(Brachymystax spp.)均列入“二级”保护重点野生动物名录[7]。
目前文献可查全世界细鳞鲑属有4个物种/亚种, 即尖吻细鳞鲑(B. lenok Pallas, 1773)[8]、钝吻细鳞鲑(B. tumensis Mori, 1930)[9]、萨式细鳞鲑(B. savinovi Mitrofanov, 1959)[10]及秦岭细鳞鲑(B. tsinlingensis Li, 1966)[11]。除萨式细鳞鲑外我国均有分布, 其中尖吻细鳞鲑和钝吻细鳞鲑分布于我国东北地区的黑龙江、图们江等流域, 为“江细鳞”, 而秦岭细鳞鲑则分布在陕西–甘肃秦岭地区的高海拔山区溪流中, 属“山细鳞”, 秦岭是该属鱼类分布的最南端(纬度最低)。由于该属鱼类分类地位仍不够明晰, 缺乏更为精细的基因组层面的谱系关系及遗传分化相关研究, 严重阻碍了种质资源保护工作有效开展。例如, 制定政策时无法准确描述其拉丁学名(亚种名/物种名), 2021年野生动物保护名录采用细鳞鲑属Brachymystax spp.而不是物种名; 且未明确遗传分化前开展跨流域增殖放流的潜在风险难以评估, 因此亟待深入开展我国细鳞鲑属不同地理种群间分子谱系关系分析, 为种质资源的保护提供科学指导。
细鳞鲑在我国北方点状不连续分布导致不同地理群体应对不同的栖息环境, 而生境差异又往往促进生物群体的遗传分化[12]。秦岭地区细鳞鲑作为第四纪冰期南下的孑遗物种及细鳞鲑属地理分布最南端的种类, 它们在冰期反复消融过程中逐渐适应了秦岭–陇山山脉的低纬度高海拔的山涧生境, 较低的年均水温等生态气候条件为其提供间冰期稳定的避难所[11, 13, 14]。秦岭地区的山涧溪流与黑龙江、乌苏里江等宽阔河流生境迥异, 在漫长的进化过程中秦岭细鳞鲑如何适应秦岭山溪低纬度高海拔的特殊生境? 在全球气候变暖的大背景下, 适应性进化机制是值得探索的重要科学问题。此外, 有研究表明秦岭地区细鳞鲑在形态学及耐热上限方面与北方黑龙江等群体存在差异, 这也可能是细鳞鲑对秦岭生态环境适应的结果[15, 16]。
小插入缺失(InDel, Insertion-Deletion)属于基因组可遗传变异的一种, 长度在1—50 bp (Base pair), 与单核苷酸多态性(SNP, Single nucleotide polymorphisms)和结构变异(SV, Structure variation)不同, InDel主要产生于DNA复制时的遗传滑动和DNA损伤修复等过程[17]。相比于SNPs, InDel由于发生反复突变的概率更小, 因此与实际的进化模式更为契合, 经常作为品种品系或特殊性状鉴定的分子标记[18-20]。然而,目前尚无利用InDel数据对我国细鳞鲑地理群体遗传差异的研究报道, 尤其是在全基因组水平。
本研究对陕西、甘肃、新疆、河北和黑龙江的6个细鳞鲑群体进行了二代重测序和InDel检测, 并基于InDel数据分析细鳞鲑遗传分化与本地适应性, 以期从全基因组InDel水平为细鳞鲑的群体结构及遗传分化提供证据, 鉴定到的受选择位点和基因可为细鳞鲑本地适应性提供新见解。此外,本研究识别到的谱系特异性InDel可为细鳞鲑物种鉴定标记的开发提供重要数据资源。
1. 材料与方法
1.1 实验材料
细鳞鲑样本于2014至2022年采自陕西、甘肃、新疆、河北和黑龙江等地, 其中黑龙江地区的细鳞鲑据吻部形态、体色等特征[15, 21, 22]分为尖吻细鳞鲑和钝吻细鳞鲑, 其余样本按分布省份描述地理群体(表 1)。采集鳍条或肌肉组织保存于95%乙醇, 采用CTAB (十六烷基三甲基溴化铵, Hexadecyl trimethyl ammonium Bromide)法提取组织DNA[23], 并于Illumina NovaSeq-6000平台进行建库测序(北京贝瑞和康生物技术有限公司)。
表 1 细鳞鲑6个类群基本信息表Table 1. Sample informations of six Brachymystax groups类群Population 采集地
Location数量Number 经度Longitude 纬度Latitude 甘肃GAN 马鹿河Malu River 15 106° 28′E 34° 42′N 陕西SNX 黑河Hei River 14 107° 49′E 33° 50′N 湑水河Xushui River 2 107° 27′E 33° 44′N 河北HEB 滦河Luan River 13 116° 56′E 42° 24′N 新疆XIN 哈巴河Haba River 16 86° 23′E 48° 08′N 黑龙江尖吻LNK 乌苏里江抓吉段
Zhuaji in Wusuli River2 134° 39′E 48°13′N 呼玛河Huma River 12 126° 29′E 51° 42′N 黑龙江钝吻TMS 乌苏里江抓吉段
Zhuaji in Wusuli River8 134° 39′E 48° 13′N 乌苏里江海青段
Haiqing in
Wusuli River8 134° 39′E 47° 52′N 1.2 InDel检测
重测序数据用Fastp v.0.20.0[24]使用默认参数进行质控, 通过BWA-MEM v.0.7.17软件[25]参数“mem -t 8 -M -R”与秦岭细鳞鲑参考基因组(ASM3130545v1)进行比对, 比对结果用SAMtools v.1.7软件[26]使用参数“sort -@ 8 -O bam”转为bam格式。GATK v.4.1.7.0软件[27]使用默认参数进行每个细鳞鲑bam文件的变异检测, 并用BCFtools v.1.12软件[28]使用参数“view -m2 -M2 -v indels”提取InDel位点[29], 之后根据位点质量、缺失率和最小等位基因频率等对InDel集合进行过滤, 参数为“view -i 'MAF>=0.1 & F_MISSING<0.1'”。
1.3 InDel统计与注释
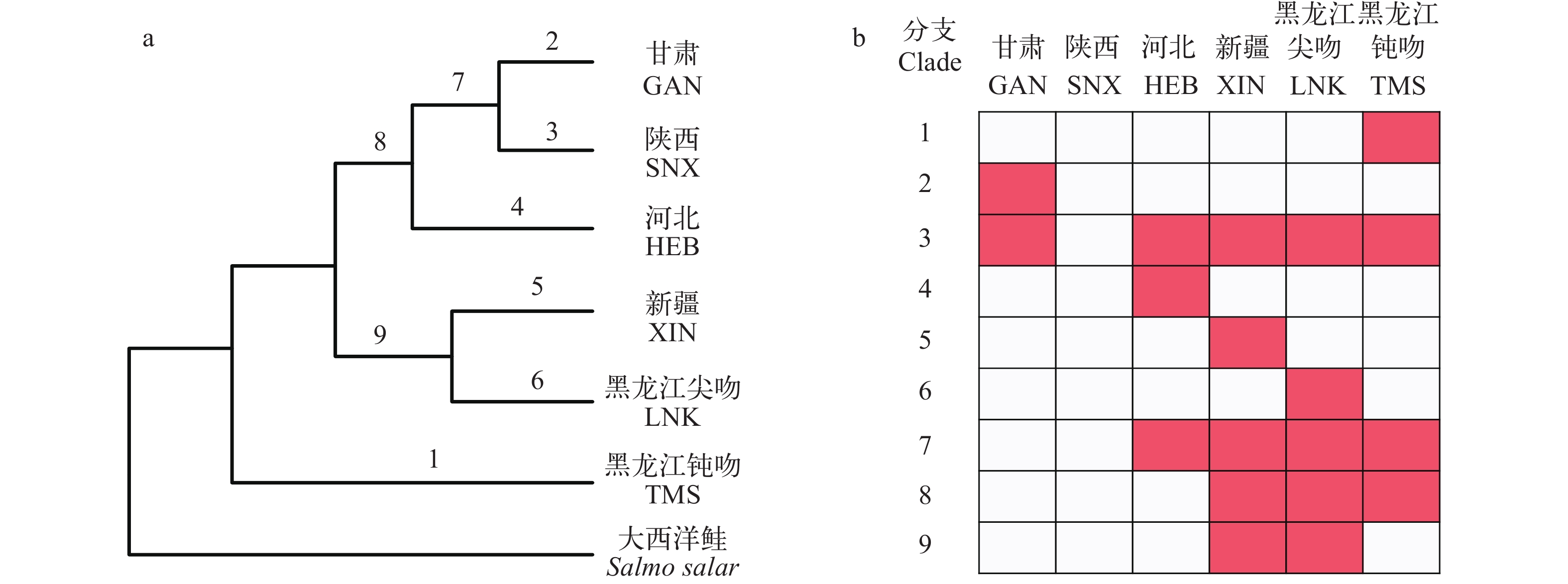
在对InDel进行过滤之后, 使用R v.4.2.2包CMplot v.4.5.0[30]进行InDel密度绘制, 组距大小设置为1 Mb。由于细鳞鲑样本群体之间的遗传差异较大, 大部分InDel属于群体基因组之间的固定差异, 且参考基因组为秦岭细鳞鲑, 因此根据系统发育关系将陕西、甘肃和河北群体中频率为0且其他群体中频率为1的变异转为衍生型变异, 即将其频率互换。此外, 为分析不同细鳞鲑群体InDel的分离情况, 对细鳞鲑每个系统发育支上固定的InDel (基因型纯合, 等位基因频率为1)进行了统计分析, 如图 1a所示, 所有InDel位点按照图 1b中每个群体的存在状况进行了划分。基于ANNOVAR软件[31]使用参数“-geneanno -dbtype refGene”对InDel在基因组中的位置进行注释, KOBAS-i[32]进行在线KEGG和GO富集分析。
![]() 图 1 系统发育分支与对应的基因型a. 以大西洋鲑(Salmo salar)为外群的细鳞鲑属各地理群体系统发育关系模式图, 拓扑结构来自线粒体基因组数据(未公布), 分支用阿拉伯数字1—9表示, 除大西洋鲑外统一使用各群体缩写(分布地/物种名)代表(下同); b. 每个分支对应的各群体基因型频率, 色块代表该群体在该位点的频率为1, 空白表示该群体在该位点的频率为0Figure 1. Phylogenetic branches with corresponding genotypesa. Phylogenetic relationships among geographic populations of the Brachymystax, with Atlantic salmon (Salmo salar) as outgroup, topology derived from mitochondrial genome data (unpublished), branches are represented by Arabic numbers 1—9, and each group abbreviation (distribution/species) is used except Atlantic salmon (the same applies below); b. Genotype frequencies of each population corresponding to each branch, the colour blocks represent the frequency of the population at that locus as 1, while the blank indicate the frequency to 0
图 1 系统发育分支与对应的基因型a. 以大西洋鲑(Salmo salar)为外群的细鳞鲑属各地理群体系统发育关系模式图, 拓扑结构来自线粒体基因组数据(未公布), 分支用阿拉伯数字1—9表示, 除大西洋鲑外统一使用各群体缩写(分布地/物种名)代表(下同); b. 每个分支对应的各群体基因型频率, 色块代表该群体在该位点的频率为1, 空白表示该群体在该位点的频率为0Figure 1. Phylogenetic branches with corresponding genotypesa. Phylogenetic relationships among geographic populations of the Brachymystax, with Atlantic salmon (Salmo salar) as outgroup, topology derived from mitochondrial genome data (unpublished), branches are represented by Arabic numbers 1—9, and each group abbreviation (distribution/species) is used except Atlantic salmon (the same applies below); b. Genotype frequencies of each population corresponding to each branch, the colour blocks represent the frequency of the population at that locus as 1, while the blank indicate the frequency to 01.4 种群结构识别
基于Python v.3.6.1sklearn v.0.18.1库的decomposition模块进行主成分分析, 设置“components”为“10”, 并使用ADMIXTURE v.1.3.0软件[33]进行群体遗传结构识别, 使用PLINK v.1.90b3.40软件[34]使用参数“--indep-pairwise 50 10 0.5”对InDel数据进行修剪, K值设置为2—7个, 并以不同的种子重复运行10次, 从中为每个K值筛选交叉验证错误率最低的结果。
1.5 受选择区域计算与位点筛选
为进一步筛选秦岭细鳞鲑特异的受选择区域, 我们将陕西和甘肃的群体合并, 同时也将两个外群黑龙江的尖吻和钝吻合并, 使用Python v.3.8.3的scikit-allel v1.3.2包[35]计算陕西-甘肃与河北(SGH)、陕西-甘肃与尖吻-钝吻(SGJD)、河北与尖吻-钝吻(HJD)之间的遗传分化系数FST, 设置为10 kb (Kilobase)窗口和2 kb步长。将FST结果按照公式T = –log2(1–FST)进行转换, 最后使用如下公式进行群体分支统计(PBS, Population Branch Statistic)的计算[36]:
$$ {\text{PBS=}}\frac{{T}^{\mathrm{S}\mathrm{G}\mathrm{H}} + {T}^{\mathrm{S}\mathrm{G}\mathrm{J}\mathrm{D}} - {T}^{\mathrm{H}\mathrm{J}\mathrm{D}}}{2} $$ 在提取候选受选择InDel位点之后使用软件SnpEff v.4.5[37]进行基因结构注释, 随机挑选不同群体个体的bam文件使用IGV v2.16.2[38]进行可视化分析。使用KOBAS网站进行在线功能富集分析, 筛选矫正P值小于0.05的条目作为富集结果。
2. 结果
2.1 重测序数据统计
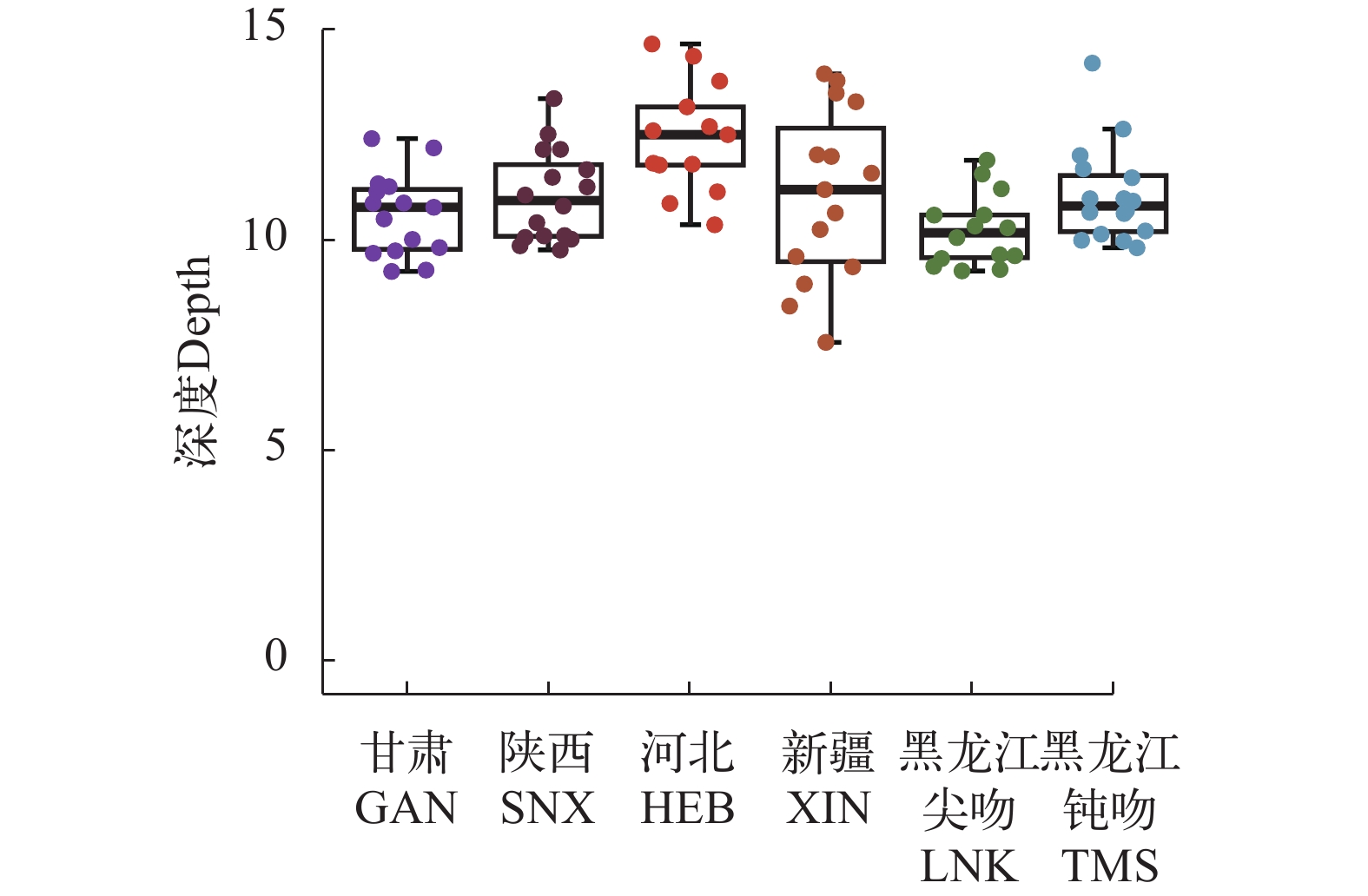
90个细鳞鲑样本经Illumina测序后总共产生8411405675条reads, 共计2.52T原始数据, 样本的GC含量为(43.53±0.77)%, 所有测序数据均保存在NCBI (PRJNA941488)。经数据质控和比对参考基因组后每个bam文件的平均深度为11.14× (图 2)。
2.2 InDel长度及分布统计
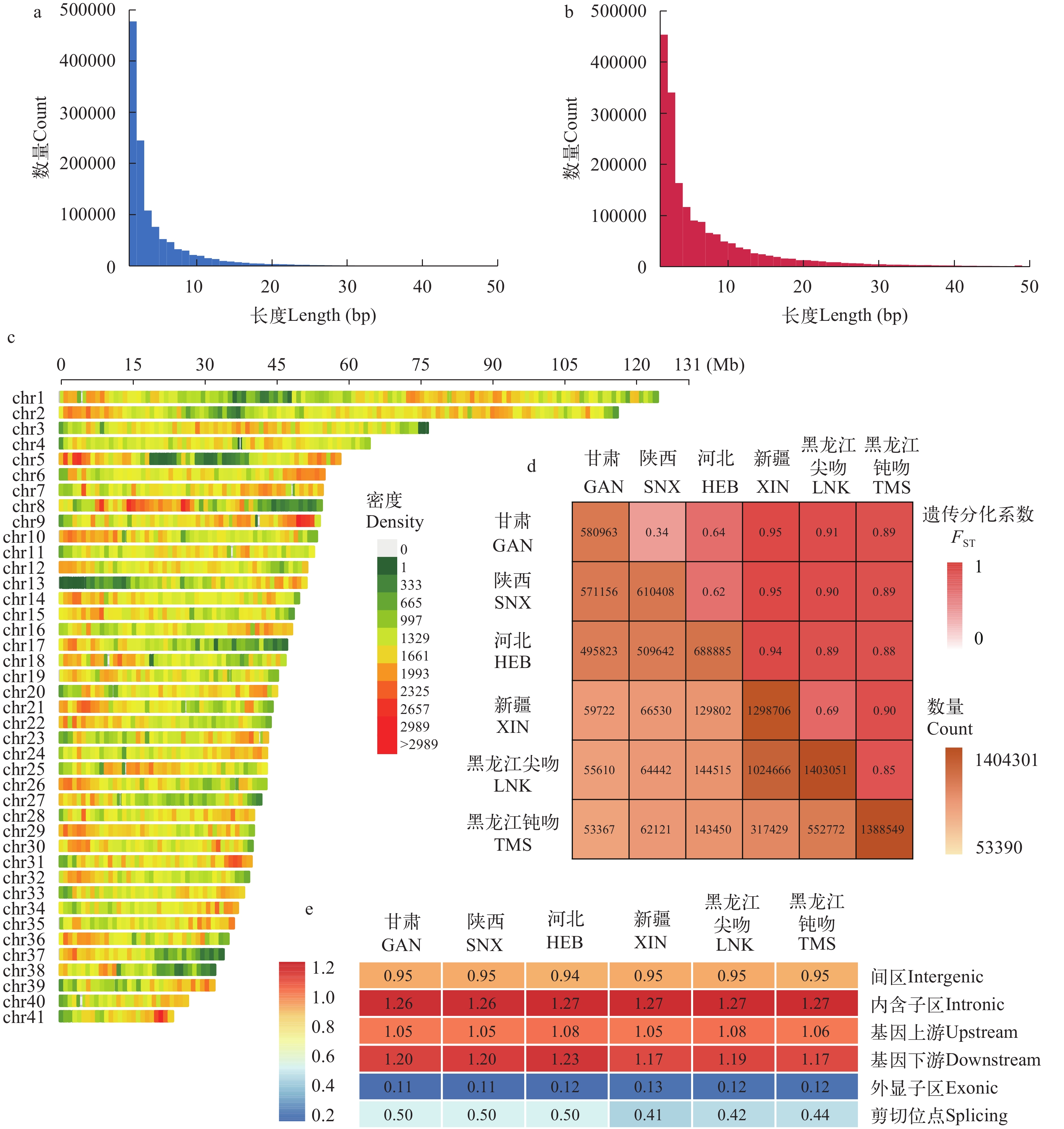
比对后的细鳞鲑重测序数据经GATK检测和BCFtools过滤共得到3056034个InDel位点。插入和缺失的总数分别为1214436和1841598, 各InDel位点的长度和数量分布如图 3a和3b所示, 除1 bp的插入位点数量多于缺失位点外, 其他长度均为缺失位点数高于插入位点。InDel平均密度为1441.19 MB, 其中9号染色体密度最高为1618.50 MB, 13号染色体密度最低为1120.64 MB(图 3c)。
![]() 图 3 细鳞鲑InDel分布与区间注释a和b分别为插入和缺失的长度分布图; c. InDel在细鳞鲑基因组染色体上的分布密度, 窗口大小为1MB; d. 各群体共享的InDel数量和基于InDel计算的FST矩阵; e. 标准化后的InDel在不同基因结构中的富集程度Figure 3. InDel distribution and location annotation of lenoka and b show the length distribution of insertions and deletions, respectively; c. InDels’ density on chromosomes using 1 MB window size; d. Matrix of shared InDels’ number and FST-value calculated based on InDels for each population; e. Standardized InDel enrichment degree in different genetic structures
图 3 细鳞鲑InDel分布与区间注释a和b分别为插入和缺失的长度分布图; c. InDel在细鳞鲑基因组染色体上的分布密度, 窗口大小为1MB; d. 各群体共享的InDel数量和基于InDel计算的FST矩阵; e. 标准化后的InDel在不同基因结构中的富集程度Figure 3. InDel distribution and location annotation of lenoka and b show the length distribution of insertions and deletions, respectively; c. InDels’ density on chromosomes using 1 MB window size; d. Matrix of shared InDels’ number and FST-value calculated based on InDels for each population; e. Standardized InDel enrichment degree in different genetic structures每个群体之间基于InDel计算的FST值以及每个群体间共享的InDel数量如图 3d所示, 统计结果显示甘肃、河北的样本与秦岭细鳞鲑接近, 新疆的群体与尖吻细鳞鲑接近, 与基于SNP的结果一致(结果未发表)。细鳞鲑群体之间显示出一定的谱系地理结构, FST值和共享InDel数量表明位于地理分布中心的河北群体与其他群体都有一定的相似性(图 3d)。黑龙江的钝吻细鳞鲑与其同域物种尖吻细鳞鲑之间的遗传分化程度较其他地理群体低(图 3d)。
对每个群体存在的InDel进行基因组位置注释的结果显示大部分InDel落入基因间区(62.30%)和内含子区(31.66%), 位于剪切连接处的数量最少(0.05%; 表 2)。由于基因各结构所占总长度的比例不同, 我们根据每个基因结构的长度比例对InDel进行了标准化, 即统计了每个群体落在每个基因结构区域的InDel与该群体总InDel数的比例, 并与各基因结构区域所占基因组总长度的比例进行比较, 结果显示基因结构对InDel的分布产生了显著影响(P<0.01, 单因素方差分析), 外显子、剪切连接和基因间区表现出对InDel的消减, 而内含子、基因上游、基因下游表现出对InDel的相对富集, 其中内含子区相对富集了更多的InDel, 基因下游相对于基因上游富集了更多InDel (图 3e)。尽管甘肃、陕西和河北的细鳞鲑群体中落在剪切位点的InDel数目比另外3个群体少, 但是其在各自集合中所占的比例更高(图 3e和表 2)。
表 2 每个细鳞鲑群体的InDel位置注释Table 2. Annotation of InDel positions on genome for each population of Brachymystax分布位置
Location甘肃
GAN陕西
SNX河北
HEB新疆
XIN黑龙江尖吻
LNK黑龙江钝吻
TMS基因间区
Intergenic region363562 (62.51%) 382294 (62.56%) 428518 (62.13%) 810320 (62.32%) 874228 (62.23%) 864702 (62.20%) 内含子区
Intron182476 (31.37%) 191260 (31.30%) 217841 (31.59%) 410348 (31.56%) 443366 (31.56%) 440409 (31.68%) 基因上游
Upstream15236 (2.62%) 16041 (2.62%) 18514 (2.68%) 34078 (2.62%) 37702 (2.68%) 36753 (2.64%) 基因下游
Downstream17404 (2.99%) 18319 (3.00%) 21103 (3.06%) 37899 (2.91%) 41652 (2.97%) 40665 (2.93%) 外显子区
Exon2615 (0.45%) 2860 (0.47%) 3337 (0.48%) 6990 (0.54%) 7170 (0.51%) 7024 (0.51%) 剪切位点
Splice site323 (0.06%) 338 (0.06%) 379 (0.05%) 586 (0.05%) 660 (0.05%) 685 (0.05%) 总和
Summary581616 611112 689692 1300221 1404778 1390238 注: 由于某个InDel可能同时落入多个注释区间, 如同时位于某基因上游及另一个基因的下游, 导致注释到的位置总和大于InDel数量总和; 下同Note: A single InDel may fall into multiple gene structure, such as the upstream-downstream of two different genes, thus the sum of annotated positions is greater than the total number of InDels; the same applies below 2.3 谱系特异性InDel注释
我们统计了在细鳞鲑每个系统发育分支上固定的InDel数量, 以追踪在细鳞鲑属鱼类系统发育过程中的InDel分离情况(图 1a和1b)。在所有的系统发育分支中总共鉴定到1715464个固定的InDel, 占全部InDel的56.08% (表 3)。结果显示固定的InDel主要位于每个谱系分支的系统发育基础位置, 即clade1、clade8和clade9, 所有分支总共产生了6529个落在外显子的InDel, 占总数的0.38% (表 3); 其中新疆群体与其他群体的地理距离最远, 具有最高的支系固定InDel数量(图 1和表 3), 这也符合细鳞鲑群体间的谱系地理结构。
表 3 每个系统发育分支中被固定的InDel注释Table 3. Fixed InDel annotation in each phylogenetic branch分布位置
Location分支1
Clade1分支2
Clade2分支3
Clade3分支4
Clade4分支5
Clade5分支6
Clade6分支7
Clade7分支8
Clade8分支9
Clade9基因间区
Intergenic region169994 208 23 17043 63589 18224 12306 126757 136875 内含子区
Intron338234 545 107 31961 125518 35869 24520 247063 265590 基因上游
Upstream13084 21 5 1347 5521 1528 1005 10138 10939 基因下游
Downstream15002 25 2 1561 6189 1657 1158 11809 12771 外显子区
Exon1851 2 1 218 1121 221 158 1386 1571 剪切位点
Splice site219 0 0 19 97 31 20 211 150 总和
Summary538384 801 138 52149 202035 57530 39167 397364 427896 2.4 基于InDel的细鳞鲑种群结构
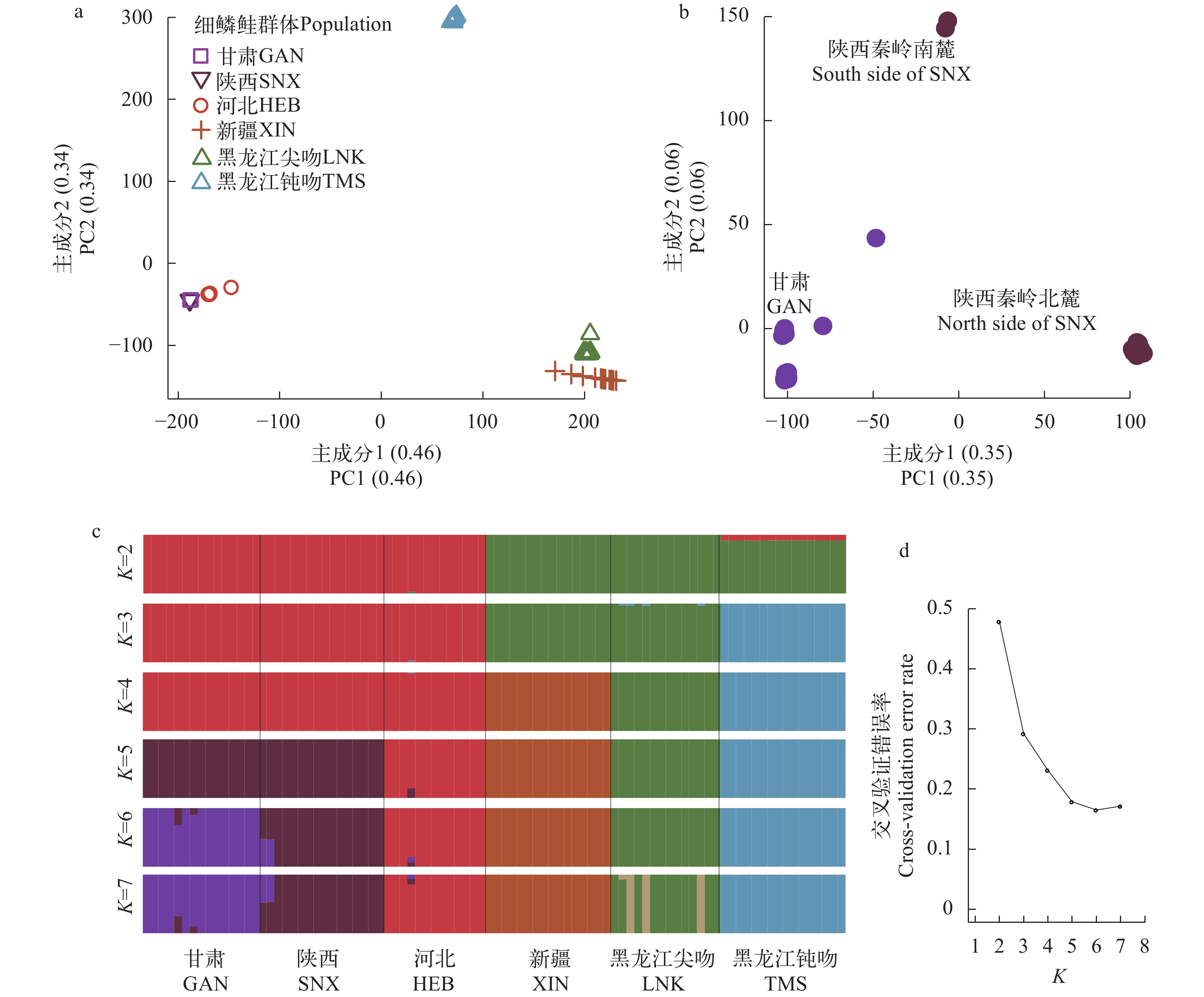
基于全基因组InDel数据进行了细鳞鲑群体的PCA和ADMIXTURE分析。PCA结果显示PC1和PC2将6个细鳞鲑群体分为3个簇, PC1中钝吻细鳞鲑簇位于秦岭细鳞鲑簇和尖吻细鳞鲑簇中间的位置, PC2中秦岭细鳞鲑簇与尖吻细鳞鲑簇更加接近, 而新疆额尔齐斯河细鳞鲑和黑龙江尖吻细鳞鲑成一簇(图 4a)。由于PCA结果中3个簇之间的遗传差异非常大, 因此导致遗传差异相对较小的甘肃和陕西群体在图中产生了重叠(图 4a)。ADMIXTURE的群体结构显示:在K=2时,6个群体被分为两个簇, 其中钝吻细鳞鲑中存在来自甘肃、陕西和河北群体的遗传成分, 而在其他K值中没有发现这一结果, 本文推测钝吻细鳞鲑在进化上与其他群体更早分离, 受不完全谱系分选的影响导致其基因组包含一定比例的其他群体的古老血统成分, 随着K值增大, 该群体获得独属于自己的血统而隐没(图 1a和4c);K=6时,6个群体分群良好各占一簇且具有最低的交叉验证错误率, 这与基于全基因组SNP计算的结果一致(结果未发表)。
![]() 图 4 基于InDel计算的各细鳞鲑地理种群的遗传结构a. 6个细鳞鲑群体的主成分分析, 括号内为解释度; b. 陕西秦岭和甘肃群体的主成分分析; c. ADMIXTURE计算的遗传结构, K值表示分配的血统/亚群数量, 颜色表示不同血统/亚群, 不同群体用竖线隔开; d.不同血统数量下ADMIXTURE结果的交叉验证错误率, 在K=6时最低, 此时每个群体都有独立的血统Figure 4. Genetic structure of each geographic population of leonk calculated based on InDel dataa. Principal component analysis of 6 lenok populations, the explained variance ratio in parentheses; b. Principal component analysis of Shaanxi Qinling (SNX) and Gansu (GAN); c. Genetic structure calculated by ADMIXTURE, K value indicates the number of lineages/ subgroups assigned, color indicates different lineages/subgroups, and different populations are separated by vertical bars; d. Cross-validation error rate of ADMIXTURE results for different numbers of lineages/subgroups, the lowest at K=6, when each population got different independent lineages/subgroups
图 4 基于InDel计算的各细鳞鲑地理种群的遗传结构a. 6个细鳞鲑群体的主成分分析, 括号内为解释度; b. 陕西秦岭和甘肃群体的主成分分析; c. ADMIXTURE计算的遗传结构, K值表示分配的血统/亚群数量, 颜色表示不同血统/亚群, 不同群体用竖线隔开; d.不同血统数量下ADMIXTURE结果的交叉验证错误率, 在K=6时最低, 此时每个群体都有独立的血统Figure 4. Genetic structure of each geographic population of leonk calculated based on InDel dataa. Principal component analysis of 6 lenok populations, the explained variance ratio in parentheses; b. Principal component analysis of Shaanxi Qinling (SNX) and Gansu (GAN); c. Genetic structure calculated by ADMIXTURE, K value indicates the number of lineages/ subgroups assigned, color indicates different lineages/subgroups, and different populations are separated by vertical bars; d. Cross-validation error rate of ADMIXTURE results for different numbers of lineages/subgroups, the lowest at K=6, when each population got different independent lineages/subgroups秦岭南北细鳞鲑的起源有争议, 有报道称秦岭南麓的细鳞鲑是20世纪30年代人为从北麓背至南麓[39], 而也有研究认为秦岭南北的细鳞鲑群体存在一定程度的分化[40, 41]。本研究的重测序数据中包含2个秦岭南麓的样本, PCA结果显示秦岭南麓的2个个体在PC2时与陕西北麓和甘肃群体分离(图 4b), 说明秦岭南麓细鳞鲑可能是一个独立种群。但由于PC2的解释度相对小, 且ADMIXTURE结果显示这两个个体各具有一半的陕西和甘肃血统(图 4c), 应扩大样本量深入分析秦岭南北细鳞鲑的遗传分化, 同时强烈呼吁禁止甘肃和陕西之间的增殖放流, 避免人为杂交、污染种质。
2.5 细鳞鲑本地适应性受选择InDel位点筛选
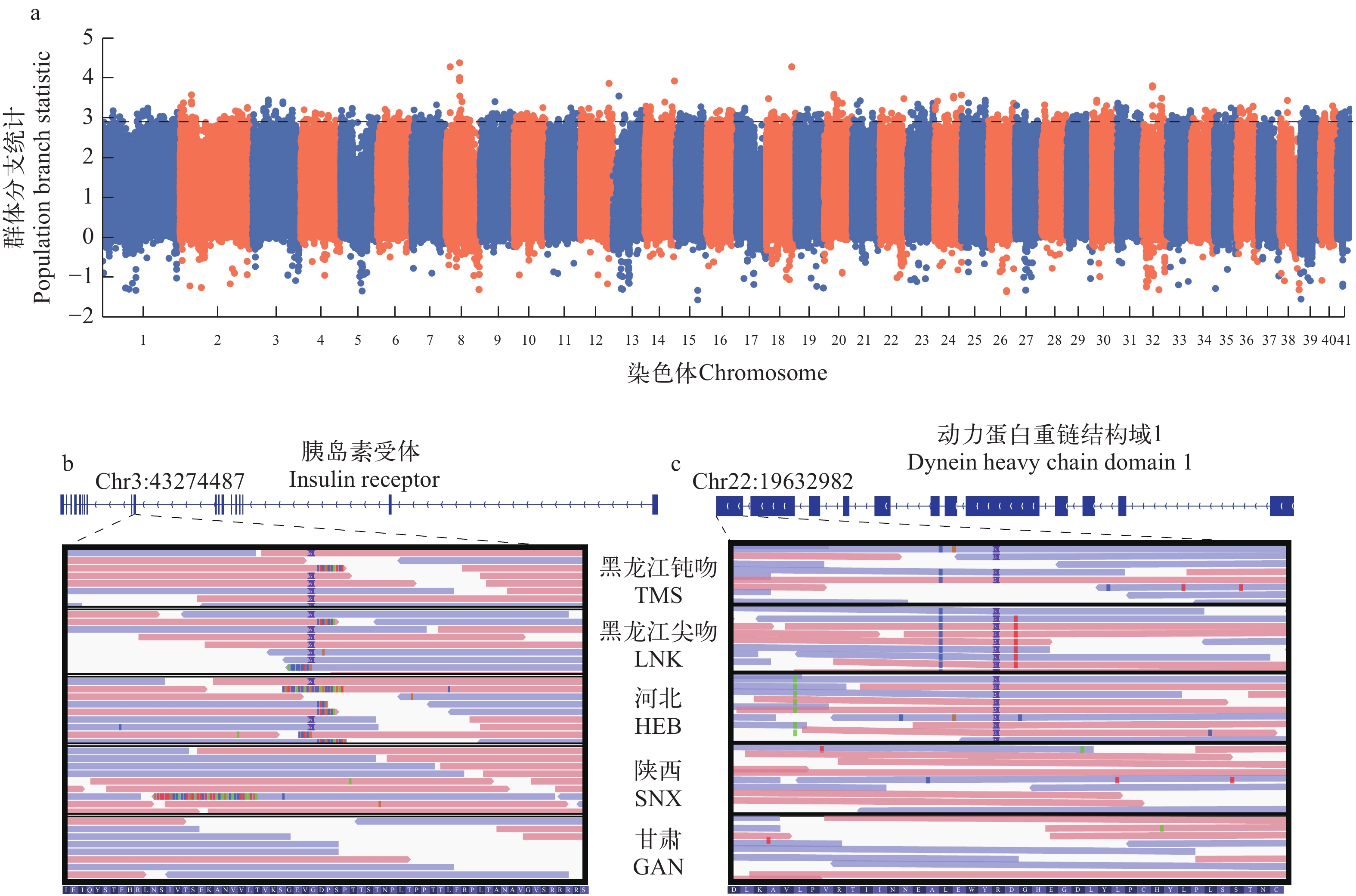
为筛选低纬度地区的甘肃与陕西的细鳞鲑群体受选择InDel位点, 以黑龙江钝吻和黑龙江尖吻细鳞鲑群体为外群, 采用PBS方法计算了甘肃–陕西和河北细鳞鲑群体之间的分支距离。将PBS值在前0.1%的区间定为潜在受选择区域, 最终从总长度为4.44 MB的基因组区域中得到8575个潜在受选择InDel位点, SnpEff注释结果显示大部分InDel位点没有对基因结构产生影响, 然而有79个InDel位点改变了候选基因的编码序列(图 5a)。从潜在受选择InDel位点集合中发现了2个使mRNA序列改变的InDel位点与设定的基因频率状况一致, 分别为3号染色体43274487处的6碱基缺失和22号染色体19632982的3碱基缺失(甘肃和陕西群体; 图 5b和5c)。Chr3:43274487的6碱基缺失位于胰岛素受体基因(insr, Insulin Receptor)的第10个外显子上, 使该外显子缺失了一个谷氨酸密码子和甘氨酸密码子, 该基因编码受体酪氨酸激酶蛋白家族成员, 胰岛素或其他配体与该受体结合激活胰岛素信号通路, 调节葡萄糖摄取和释放及碳水化合物、脂质和蛋白质的合成和储存(图 5b)。Chr22:19632982的3碱基缺失位于动力蛋白重链结构域1基因(dnhd1, Dynein Heavy Chain Domain 1)的第12个外显子上, 导致该外显子丢失一个丝氨酸密码子, dnhd1是一种蛋白质编码基因, 与精子鞭毛轴突的正常组装和功能相关(图 5c)。
![]() 图 5 基于InDel数据的低纬度山区溪流型细鳞鲑的基因组受选择分析结果a. 全基因组PBS结果, 使用10 KB窗口和2 KB步长; b和c分别为胰岛素受体基因和动力蛋白重链结构域1基因结构及受选择位点的位置, 方框内的条带为IGV可视化后的reads, 彩色竖线表示SNP紫色方框为InDel, 最下方为三联密码子对应的氨基酸Figure 5. Genomic selection analysis of lenok populations in low-latitude mountain streams based on InDel dataa. Result of genome-wide PBS, using 10-KB windows and 2-KB steps; b and c are the insulin receptor gene and dynein heavy chain domain 1 gene structure and the position of the selected InDel site, respectively. The red and blue stripes are the IGV visualized reads in plus and minus strands respectively; the SNPs are showed by the colored vertical bars; the purple box is the InDel; the amino acids corresponding to the triple codons are at the bottom
图 5 基于InDel数据的低纬度山区溪流型细鳞鲑的基因组受选择分析结果a. 全基因组PBS结果, 使用10 KB窗口和2 KB步长; b和c分别为胰岛素受体基因和动力蛋白重链结构域1基因结构及受选择位点的位置, 方框内的条带为IGV可视化后的reads, 彩色竖线表示SNP紫色方框为InDel, 最下方为三联密码子对应的氨基酸Figure 5. Genomic selection analysis of lenok populations in low-latitude mountain streams based on InDel dataa. Result of genome-wide PBS, using 10-KB windows and 2-KB steps; b and c are the insulin receptor gene and dynein heavy chain domain 1 gene structure and the position of the selected InDel site, respectively. The red and blue stripes are the IGV visualized reads in plus and minus strands respectively; the SNPs are showed by the colored vertical bars; the purple box is the InDel; the amino acids corresponding to the triple codons are at the bottom2.6 细鳞鲑本地适应性受选择区间功能注释
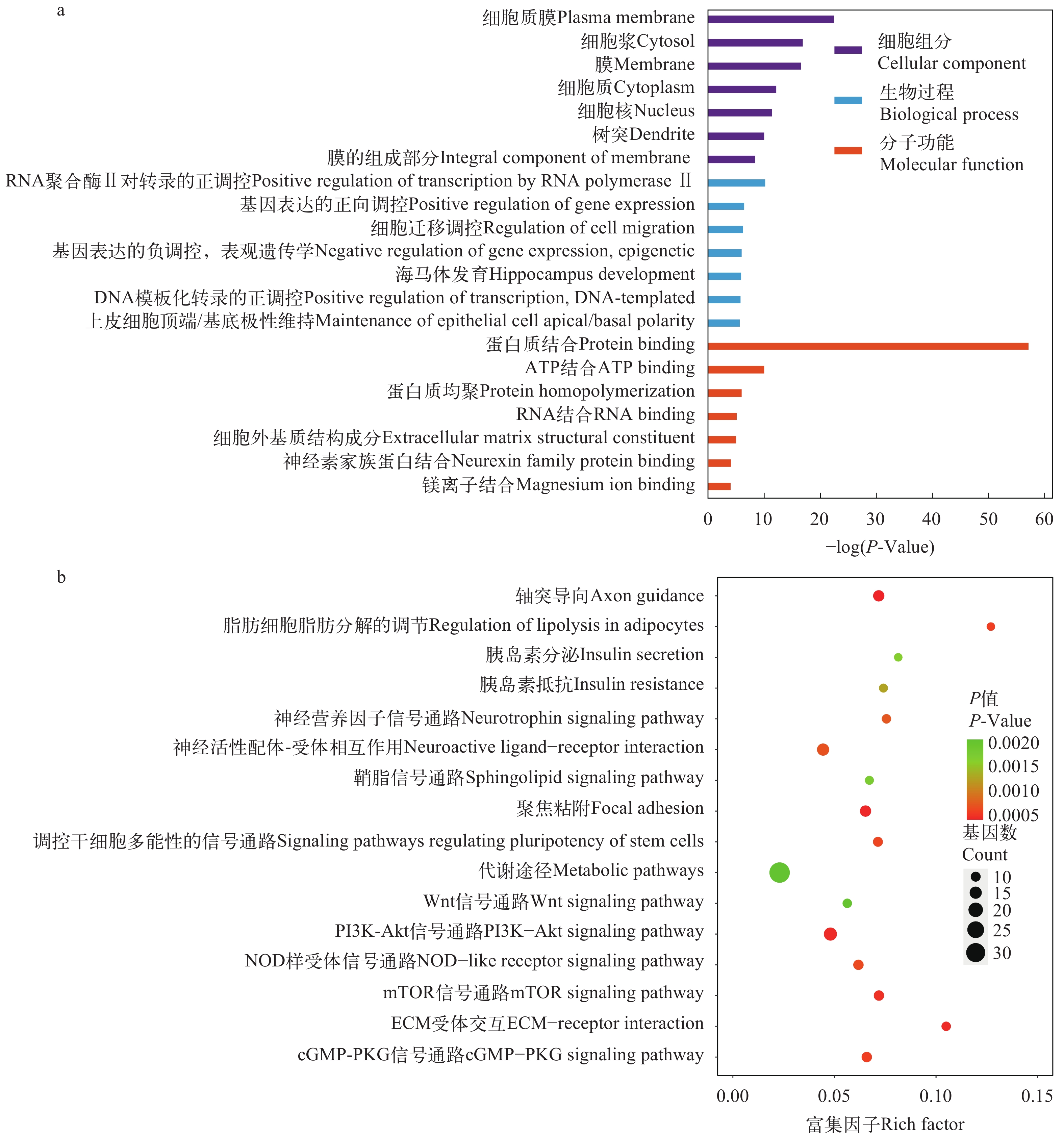
从潜在受选择区域中共注释到621个候选的受选择基因, 对其进行的功能注释, 共得到显著富集(P<0.05)的581个GO条目和62个KEGG通路(图 6a和6b)。GO分析显示细胞组分(Cellular Component)相关的候选基因中与生物膜相关的条目相对较多, 包括细胞质膜(GO:0005886)、膜(GO:0016020)等(图 6a)。生物过程(Biological Process)相关的候选基因相对较少, 主要包括转录和基因表达调控等过程, 包括RNA聚合酶Ⅱ对转录的正调控(GO:0045944)、基因表达的正向调控(GO:0010628)等(图 6a)。分子功能(Molecular Function)中与结合功能相关的基因富集较多, 其中蛋白质结合(GO:0005515)具有最高的显著性, 其次还注释到ATP结合(GO:0005524)、RNA结合(GO:0003723)等功能(图 6a)。
KEGG分析注释到多条与神经相关的通路, 主要包括轴突导向(hsa04360)、神经营养因子信号通路(hsa04722)、神经活性配体—受体相互作用(hsa04080)、鞘脂信号通路(hsa04071)等; 此外还富集到代谢过程、干细胞调控、细胞凋亡、胰岛素相关的功能及脂肪细胞脂肪分解等代谢途径, 可能与秦岭地区特异的生态与营养条件适应性有关(图 6b)。可见, GO和KEGG结果都富集了神经相关的功能, 可能与山区溪流鱼类应对湍急水流的行为及对低纬度地区的热适应有关。
3. 讨论
3.1 细鳞鲑InDel的分布模式
本研究利用高质量的重测序数据构建了6个细鳞鲑群体的InDel集合, 其中缺失数远大于插入数, 由于群体间的进化关系和遗传距离不同, 导致不同群体内部含有的InDel数量差异巨大, 根据系统发育关系和基因频率对其进行衍生型突变转换之后, 新疆、黑龙江尖吻和黑龙江钝吻三个细鳞鲑群体的InDel数量为另外3个细鳞鲑群体的两倍左右(图 3d), 说明相比于另外3个分支而言, 新疆与黑龙江的3个分支在进化上与参考基因组(秦岭细鳞鲑)所在的分支有更远的距离。此外, 本研究中根据系统发育关系筛选的分支特异性InDel可作为谱系识别的分子标记, 为细鳞鲑的物种鉴定提供了分子遗传数据。
基因结构注释结果显示位于基因间区及内含子区的InDel数目占比最大, 而外显子和剪切位点的数目较少, 相似的分布模式在卵形鲳鲹[42]和鸡[43]等动物中也观察到。由于各基因结构在整个基因组中所占的长度比例不同, 仅从InDel在各基因结构分布的比例进行评估并不能完整反映出其对不同基因结构的富集偏好性, 因此我们利用各基因结构所占总基因组长度的比例对InDel的分布进行了标准化(图 1), 结果显示外显子区和剪切位点的InDel富集程度的下降与预期一致, 然而内含子区相对于基因间区更容易产生InDel (图 3e), 这可能源于DNA复制和转录碰撞引发的突变[44, 45], 导致内含子区产生了比基因间区相对更多的InDel。
3.2 细鳞鲑群体遗传结构及分化
基于InDel数据计算细鳞鲑种群结构,结果显示秦岭细鳞鲑与尖吻细鳞鲑和钝吻细鳞鲑分离(图 4a—c),为秦岭细鳞鲑的独立物种地位提供更多的基因组学的证据支持(未发表结果)。总体上看, 群体结构分析的结果与FST一致, 本研究采集的6个细鳞鲑地理群体由三个主要的遗传谱系组成, 即尖吻谱系(LNK, XIN)、钝吻谱系(TMS)和秦岭谱系(SNX, GAN, HEB), 这3个谱系与前人的细鳞鲑分类学研究结果相对应[3, 11, 15, 21]。河北细鳞鲑(HEB)采自滦河流域, 本研究基于全基因组InDel数据认为其属于秦岭细鳞鲑谱系, 且在地理上位于黄河支流渭河流域与黑龙江流域之间, 同时PCA和FST均显示出该种群相对于陕–甘群体与另外两个谱系的遗传距离更近; 新疆群体与其他群体地理距离最远,遗传距离最大; 尽管黑龙江尖吻和钝吻是两个不同的遗传谱系, 但是两者之间比预期更低的FST和更多的共享InDel数均表明该同域物种可能存在一定程度的基因流[46]。由于当前细鳞鲑在不同地理分布区之间是完全隔离的, 鉴于其明显的生物地理格局, 我们推测古代间断的冰期中存在细鳞鲑的迁移和基因流事件, 共同促进了细鳞鲑的异域物种形成[47]。
本研究中由于无法排除杂交的干扰且样本量小, 暂时难以将秦岭南麓样本准确判为独立群体, 需扩大样本量进行深入研究以确证结论。此外, ADMIXTURE结果中也观察到甘肃群体的两个样本混合了一定比例的陕西血统(图 4b), 可能源于两细鳞鲑群体祖先的不完全谱系分选及冰期种群扩散导致的基因流。FST、PCA和ADMIXTURE结果表明甘肃和陕西地区细鳞鲑存在实质性的遗传差异, 因此我们建议严禁这两个邻近地区之间的增殖放流活动, 以及本研究中细鳞鲑其他分布地之间应停止跨地人工放流, 避免人为杂交而污染珍稀濒危鱼类种质资源[48, 49]。
3.3 秦岭细鳞鲑的本地适应性进化
生活在低纬度地区的细鳞鲑群体均具有相似生境, 栖息于海拔900—2300 m的冷水山涧溪流中[13, 50], 本研究基于InDel数据利用PBS方法在陕西和甘肃低纬度群体的受选择区间筛选到两个符合特定频率分布的位点分别位于insr和dnhd1的外显子上(图 5b和5c)。insr编码胰岛素受体蛋白, 其参与的胰岛素信号通路在代谢调节、生长调控和神经元功能等过程中起着关键作用, 胰岛素的细胞功能由其与胰岛素受体蛋白的结合而启动[51, 52]。人类INSR的突变可能会影响其对胰岛素的敏感性, 导致胰岛素抵抗性相关疾病[53, 54]。斑马鱼也具有两个insr基因——insra和insrb, 这两种基因均在成鱼大脑中广泛表达, 对其神经发生可能具有潜在作用[55]; Yang等[56]的研究表明斑马鱼insr基因在葡萄糖代谢和胚胎发育中均起着关键作用, insra在胰岛素信号通路中比insrb更为关键。甘肃和陕西群体特异的两个氨基酸插入可能影响胰岛素受体蛋白的功能, 本文推测其为细鳞鲑本地适应的结果, 然而该突变是否影响细鳞鲑的神经、代谢等生物过程还需进一步研究。dnhd1编码动力蛋白重链结构域1蛋白, 其功能对于维持正常的精子鞭毛是必需的, 突变会导致人类和小鼠的鞭毛轴突缺陷及多种形态异常[57, 58]。然而由于甘肃和陕西的细鳞鲑群体中该突变的基因频率达到1, 本文推测该突变不会导致两地细鳞鲑精子的功能异常, 该突变的生物学功能仍需进一步研究。此外, 对受选择区间的通路富集分析发现了多种与神经系统和代谢调控相关条目(图 6), 反映出甘肃和陕西的细鳞鲑对秦岭低纬度山区溪流的生境产生的适应性改变与神经和代谢等过程相关。
综上所述, 本研究对6个细鳞鲑地理群体的InDel突变进行了检测与分析, 所得的结果支持群体之间存在遗传结构差异, 受选择分析揭示了与秦岭细鳞鲑本地适应性相关的基因和InDel位点, 研究结果将为细鳞鲑的种质保护和遗传进化研究提供参考资料。
-
图 1 系统发育分支与对应的基因型
a. 以大西洋鲑(Salmo salar)为外群的细鳞鲑属各地理群体系统发育关系模式图, 拓扑结构来自线粒体基因组数据(未公布), 分支用阿拉伯数字1—9表示, 除大西洋鲑外统一使用各群体缩写(分布地/物种名)代表(下同); b. 每个分支对应的各群体基因型频率, 色块代表该群体在该位点的频率为1, 空白表示该群体在该位点的频率为0
Figure 1. Phylogenetic branches with corresponding genotypes
a. Phylogenetic relationships among geographic populations of the Brachymystax, with Atlantic salmon (Salmo salar) as outgroup, topology derived from mitochondrial genome data (unpublished), branches are represented by Arabic numbers 1—9, and each group abbreviation (distribution/species) is used except Atlantic salmon (the same applies below); b. Genotype frequencies of each population corresponding to each branch, the colour blocks represent the frequency of the population at that locus as 1, while the blank indicate the frequency to 0
图 3 细鳞鲑InDel分布与区间注释
a和b分别为插入和缺失的长度分布图; c. InDel在细鳞鲑基因组染色体上的分布密度, 窗口大小为1MB; d. 各群体共享的InDel数量和基于InDel计算的FST矩阵; e. 标准化后的InDel在不同基因结构中的富集程度
Figure 3. InDel distribution and location annotation of lenok
a and b show the length distribution of insertions and deletions, respectively; c. InDels’ density on chromosomes using 1 MB window size; d. Matrix of shared InDels’ number and FST-value calculated based on InDels for each population; e. Standardized InDel enrichment degree in different genetic structures
图 4 基于InDel计算的各细鳞鲑地理种群的遗传结构
a. 6个细鳞鲑群体的主成分分析, 括号内为解释度; b. 陕西秦岭和甘肃群体的主成分分析; c. ADMIXTURE计算的遗传结构, K值表示分配的血统/亚群数量, 颜色表示不同血统/亚群, 不同群体用竖线隔开; d.不同血统数量下ADMIXTURE结果的交叉验证错误率, 在K=6时最低, 此时每个群体都有独立的血统
Figure 4. Genetic structure of each geographic population of leonk calculated based on InDel data
a. Principal component analysis of 6 lenok populations, the explained variance ratio in parentheses; b. Principal component analysis of Shaanxi Qinling (SNX) and Gansu (GAN); c. Genetic structure calculated by ADMIXTURE, K value indicates the number of lineages/ subgroups assigned, color indicates different lineages/subgroups, and different populations are separated by vertical bars; d. Cross-validation error rate of ADMIXTURE results for different numbers of lineages/subgroups, the lowest at K=6, when each population got different independent lineages/subgroups
图 5 基于InDel数据的低纬度山区溪流型细鳞鲑的基因组受选择分析结果
a. 全基因组PBS结果, 使用10 KB窗口和2 KB步长; b和c分别为胰岛素受体基因和动力蛋白重链结构域1基因结构及受选择位点的位置, 方框内的条带为IGV可视化后的reads, 彩色竖线表示SNP紫色方框为InDel, 最下方为三联密码子对应的氨基酸
Figure 5. Genomic selection analysis of lenok populations in low-latitude mountain streams based on InDel data
a. Result of genome-wide PBS, using 10-KB windows and 2-KB steps; b and c are the insulin receptor gene and dynein heavy chain domain 1 gene structure and the position of the selected InDel site, respectively. The red and blue stripes are the IGV visualized reads in plus and minus strands respectively; the SNPs are showed by the colored vertical bars; the purple box is the InDel; the amino acids corresponding to the triple codons are at the bottom
表 1 细鳞鲑6个类群基本信息表
Table 1 Sample informations of six Brachymystax groups
类群Population 采集地
Location数量Number 经度Longitude 纬度Latitude 甘肃GAN 马鹿河Malu River 15 106° 28′E 34° 42′N 陕西SNX 黑河Hei River 14 107° 49′E 33° 50′N 湑水河Xushui River 2 107° 27′E 33° 44′N 河北HEB 滦河Luan River 13 116° 56′E 42° 24′N 新疆XIN 哈巴河Haba River 16 86° 23′E 48° 08′N 黑龙江尖吻LNK 乌苏里江抓吉段
Zhuaji in Wusuli River2 134° 39′E 48°13′N 呼玛河Huma River 12 126° 29′E 51° 42′N 黑龙江钝吻TMS 乌苏里江抓吉段
Zhuaji in Wusuli River8 134° 39′E 48° 13′N 乌苏里江海青段
Haiqing in
Wusuli River8 134° 39′E 47° 52′N 表 2 每个细鳞鲑群体的InDel位置注释
Table 2 Annotation of InDel positions on genome for each population of Brachymystax
分布位置
Location甘肃
GAN陕西
SNX河北
HEB新疆
XIN黑龙江尖吻
LNK黑龙江钝吻
TMS基因间区
Intergenic region363562 (62.51%) 382294 (62.56%) 428518 (62.13%) 810320 (62.32%) 874228 (62.23%) 864702 (62.20%) 内含子区
Intron182476 (31.37%) 191260 (31.30%) 217841 (31.59%) 410348 (31.56%) 443366 (31.56%) 440409 (31.68%) 基因上游
Upstream15236 (2.62%) 16041 (2.62%) 18514 (2.68%) 34078 (2.62%) 37702 (2.68%) 36753 (2.64%) 基因下游
Downstream17404 (2.99%) 18319 (3.00%) 21103 (3.06%) 37899 (2.91%) 41652 (2.97%) 40665 (2.93%) 外显子区
Exon2615 (0.45%) 2860 (0.47%) 3337 (0.48%) 6990 (0.54%) 7170 (0.51%) 7024 (0.51%) 剪切位点
Splice site323 (0.06%) 338 (0.06%) 379 (0.05%) 586 (0.05%) 660 (0.05%) 685 (0.05%) 总和
Summary581616 611112 689692 1300221 1404778 1390238 注: 由于某个InDel可能同时落入多个注释区间, 如同时位于某基因上游及另一个基因的下游, 导致注释到的位置总和大于InDel数量总和; 下同Note: A single InDel may fall into multiple gene structure, such as the upstream-downstream of two different genes, thus the sum of annotated positions is greater than the total number of InDels; the same applies below 表 3 每个系统发育分支中被固定的InDel注释
Table 3 Fixed InDel annotation in each phylogenetic branch
分布位置
Location分支1
Clade1分支2
Clade2分支3
Clade3分支4
Clade4分支5
Clade5分支6
Clade6分支7
Clade7分支8
Clade8分支9
Clade9基因间区
Intergenic region169994 208 23 17043 63589 18224 12306 126757 136875 内含子区
Intron338234 545 107 31961 125518 35869 24520 247063 265590 基因上游
Upstream13084 21 5 1347 5521 1528 1005 10138 10939 基因下游
Downstream15002 25 2 1561 6189 1657 1158 11809 12771 外显子区
Exon1851 2 1 218 1121 221 158 1386 1571 剪切位点
Splice site219 0 0 19 97 31 20 211 150 总和
Summary538384 801 138 52149 202035 57530 39167 397364 427896 -
[1] 张觉民. 黑龙江省鱼类志 [M]. 哈尔滨: 黑龙江科学技术出版社, 1995: 52. Zhang J M. Fish Fauna of Heilongjiang Province [M]. Harbin: Heilongjiang Science and Technology Press, 1995: 52.
[2] 陈毅峰, 何舜平, 何长才. 中国淡水鱼类原色图集(第三集) [M]. 上海: 上海科学技术出版社, 1993: 166. Cheng Y F, He S P, He C C. Chinese Freshwater Fish Color Atlas (Part Ⅲ) [M]. Shanghai: Shanghai Science and Technology Press, 1993: 166.
[3] 熊冬梅, 蒙彦晓, 张鑫淼, 等. 基于线粒体控制区和微卫星标记探讨秦岭细鳞鲑物种有效性 [J]. 水生生物学报, 2023, 47(5): 809-818. Xiong D M, Meng Y X, Zhang X M, et al. The validity of species of Brachymystax tsinlingensis Li based on mitochondria control region and microsatellite [J]. Acta Hydrobiologica Sinica, 2023, 47(5): 809-818.
[4] Planes S, Fauvelot C. Isolation by distance and vicariance drive genetic structure of a coral reef fish in the Pacific Ocean [J]. Evolution; International Journal of Organic Evolution, 2002, 56(2): 378-399.
[5] Gaither M R, Bernal M A, Coleman R R, et al. Genomic signatures of geographic isolation and natural selection in coral reef fishes [J]. Molecular Ecology, 2015, 24(7): 1543-1557. doi: 10.1111/mec.13129
[6] 国家林业部, 国家农业部: 国家重点保护野生动物名录 [Z]. 1988-12-10 Ministry of Agriculture, Ministry of National Forestry. The List of National Key Protected Wild Animals [Z]. 1988-12-10.
[7] 国家林业和草原局, 农业农村部. 国家重点保护野生动物名录 (2021年2月1日修订) [Z]. 2021-2-1. National Forestry and Grassland Administration, Ministry of Agriculture and Rural Affairs. The List of National Key Protected Wild Animals (Revised on February 1, 2021) [Z]. 2021-2-1.
[8] Pallas P S. Reise Durch Verschiedene Provinzen des Russischen Reiches [M]. St Petersburg: Kayserliche Akademie der Wissenschaften. 1773: 455-760.
[9] Mori T. On the freshwater fishes from the Tumen River, Korea, with description of new species [J]. The Journal of Chosen Natural History Society, 1930(11): 1-11.
[10] Mitrofanov V. On the taxonomy of Brachymystax lenok of the Lake Marka-Kul [J]. Sbornik Rabot po Ikhtiologii Gidrobiologii, 1959(2): 267-275.
[11] 李思忠. 陕西太白山细鳞鲑的一新亚种 [J]. 动物分类学报, 1966, 3(1): 92-94. Li S Z. On a new subspecies of fresh-water trout, Branchymystax lenok tsinlingensis, from Taibaishan, Shannxi, China [J]. Acta Zootaxon Sinica, 1966, 3(1): 92-94.
[12] Orr M R, Smith T B. Ecology and speciation [J]. Trends in Ecology & Evolution, 1998, 13(12): 502-506.
[13] Zhao Y H, Zhang C G. Threatened fishes of the world: Brachymystax lenok tsinlingensis Li, 1966 (Salmonidae) [J]. Environmental Biology of Fishes, 2009, 86(1): 11-12. doi: 10.1007/s10641-008-9337-7
[14] Provan J, Bennett K D. Phylogeographic insights into cryptic glacial refugia [J]. Trends in Ecology & Evolution, 2008, 23(10): 564-571.
[15] 蒙彦晓, 王桂华, 熊冬梅, 等. 基于形态学差异探讨秦岭细鳞鲑亚种有效性问题 [J]. 水生生物学报, 2018, 42(3): 550-560. Meng Y X, Wang G H, Xiong D M, et al. The validity of subspecies of Brachymystax lenok tsinlingensis Li based on morphological difference analysis [J]. Acta Hydrobiologica Sinica, 2018, 42(3): 550-560.
[16] Xia J, Ma Y, Fu C, et al. Effects of temperature acclimation on the critical thermal limits and swimming performance of Brachymystax lenok tsinlingensis: a threatened fish in Qinling Mountain Region of China [J]. Ecological Research, 2017, 32(1): 61-70. doi: 10.1007/s11284-016-1418-z
[17] Garcia-Diaz M, Kunkel T A, Thomas A. Mechanism of a genetic glissando: structural biology of indel mutations [J]. Trends in Biochemical Sciences, 2006, 31(4): 206-214. doi: 10.1016/j.tibs.2006.02.004
[18] 蒲伟军, 谭冰兰, 贺丹晨, 等. 利用重测序技术开发高粱InDel分子标记 [J]. 生物技术进展, 2023, 13(5): 730-741. Pu W J, Tan B L, He D C, et al. Development of InDel molecular markers in sorghum using re-sequencing technology [J]. Current Biotechnology, 2023, 13(5): 730-741.
[19] Du J, Li S, Shao J, et al. Genetic diversity analysis and development of molecular markers for the identification of largemouth bass (Micropterus salmoides L.) based on whole-genome re-sequencing [J]. Frontiers in Genetics, 2022(13): 936610.
[20] 黄智康, 江世贵, 周发林, 等. 基于InDel标记的斑节对虾早期性别鉴定方法的建立 [J]. 南方水产科学, 2020, 16(3): 113-118. Huang Z K, Jiang S G, Zhou F L, et al. Establishment of a sex identification method for black tiger shrimp (Penaeus monodon) in embryonic and early postembryonic development based on an InDel molecular marker [J]. South China Fisheries Science, 2020, 16(3): 113-118.
[21] 马波, 尹家胜, 李景鹏. 黑龙江流域两种细鳞鲑的形态学比较及其分类地位初探 [J]. 动物分类学报, 2005, 30(2): 257-260. Ma B, Yin J S, Li J P. Comparative studies on morphology and taxonomic position of two species of lenok [J]. Acta Zootaxonomica Sinica, 2005, 30(2): 257-260.
[22] 王丰. 秦岭细鳞鲑的研究进展 [J]. 陕西农业科学, 2011, 57(5): 181-183. Wang F. Research progress of Brachymystax lenok tsinlingensis Li [J]. Shaanxi Journal of Agricultural Sciences, 2011, 57(5): 181-183.
[23] Stefanova P, Taseva M, Georgieva T, et al. A modified CTAB method for DNA extraction from soybean and meat products [J]. Biotechnology & Biotechnological Equipment, 2013, 27(3): 3803-3810.
[24] Chen S, Zhou Y, Chen Y, et al. Fastp: an ultra-fast all-in-one FASTQ preprocessor [J]. Bioinformatics, 2018, 34(17): i884-i890. doi: 10.1093/bioinformatics/bty560
[25] Jung Y, Han D. BWA-MEME: BWA-MEM emulated with a machine learning approach [J]. Bioinformatics, 2022, 38(9): 2404-2413. doi: 10.1093/bioinformatics/btac137
[26] Li H, Handsaker B, Wysoker A, et al. The Sequence Alignment/Map format and SAMtools [J]. Bioinformatics, 2009, 25(16): 2078-2079. doi: 10.1093/bioinformatics/btp352
[27] McKenna A, Hanna M, Banks E, et al. The Genome Analysis Toolkit: a MapReduce framework for analyzing next-generation DNA sequencing data [J]. Genome Research, 2010, 20(9): 1297-1303. doi: 10.1101/gr.107524.110
[28] Danecek P, Bonfield J K, Liddle J, et al. Twelve years of SAMtools and BCFtools [J]. GigaScience, 2021, 10(2): giab008. doi: 10.1093/gigascience/giab008
[29] Danecek P, Auton A, Abecasis G, et al. The variant call format and VCFtools [J]. Bioinformatics, 2011, 27(15): 2156-2158. doi: 10.1093/bioinformatics/btr330
[30] Yin L, Zhang H, Tang Z, et al. rMVP: a memory-efficient, visualization-enhanced, and parallel-accelerated tool for genome-wide association study [J]. Genomics,Proteomics & Bioinformatics, 2021, 19(4): 619-628.
[31] Wang K, Li M, Hakonarson H. ANNOVAR: functional annotation of genetic variants from high-throughput sequencing data [J]. Nucleic Acids Research, 2010, 38(16): e164. doi: 10.1093/nar/gkq603
[32] Bu D, Luo H, Huo P, et al. KOBAS-i: intelligent prioritization and exploratory visualization of biological functions for gene enrichment analysis [J]. Nucleic Acids Research, 2021, 49(W1): W317-W325. doi: 10.1093/nar/gkab447
[33] Shringarpure S S, Bustamante C D, Lange K, et al. Efficient analysis of large datasets and sex bias with ADMIXTURE [J]. BMC Bioinformatics, 2016(17): 218.
[34] Purcell S, Neale B, Todd-Brown K, et al. PLINK: a tool set for whole-genome association and population-based linkage analyses [J]. American Journal of Human Genetics, 2007, 81(3): 559-575. doi: 10.1086/519795
[35] Miles A, Ralph P, Rae S, et al. cggh/scikit-allel: v1.3. 2 [CP]. Zenodo, 2020.
[36] Yi X, Liang Y, Huerta-Sanchez E, et al. Sequencing of 50 human exomes reveals adaptation to high altitude [J]. Science, 2010, 329(5987): 75-78. doi: 10.1126/science.1190371
[37] Cingolani P, Patel V M, Coon M, et al. Using Drosophila melanogaster as a model for genotoxic chemical mutational studies with a new program, SnpSift [J]. Frontiers in Genetics, 2012(3): 35.
[38] Thorvaldsdóttir H, Robinson J T, Mesirov J P. Integrative Genomics Viewer (IGV): high-performance genomics data visualization and exploration [J]. Briefings in Bioinformatics, 2013, 14(2): 178-192. doi: 10.1093/bib/bbs017
[39] 杜汉斌, 武金星, 王绿洲. 湑水河流域秦岭细鳞鲑背后的故事 [J]. 中国水产, 2006(12): 79-80. Du H B, Wu J X, Wang L Z. The story behind Branchymystax lenok tsinlingensis in Xushui River [J]. China Fisheries, 2006(12): 79-80.
[40] 杜汉斌. 秦岭南北鲑科鱼类渊源质疑 [J]. 河南水产, 2012(2): 5-7+9. Du H B. Query on the origin of the family Salmonidae in the north and south Qinling Mountains [J]. Henan Fisheries, 2012(2): 5-7+9.
[41] 原居林, 朱俊杰, 王高学. 秦岭细鳞鲑黑河种群和湑水河种群的遗传多样性分析 [J]. 南方水产, 2009, 5(3): 63-66. Yuan J L, Zhu J J, Wang G X. Analysis of the genetic diversity in Heihe River and Xushuihe River populations of Qinling Brachymystax lenok [J]. South China Fisheries Science, 2009, 5(3): 63-66.
[42] 伞利择, 刘宝锁, 张楠, 等. 基于卵形鲳鲹基因组重测序的InDel标记挖掘与耐低氧性状关联分析 [J]. 南方水产科学, 2022, 18(5): 100-109. San L Z, Liu B S, Zhang N, et al. Mining of InDel marker and association analysis of hypoxia tolerance traits in Trachinotus ovatus based on resequencing [J]. South China Fisheries Science, 2022, 18(5): 100-109.
[43] Godoy T F, Moreira G C M, Boschiero C, et al. SNP and INDEL detection in a QTL region on chicken chromosome 2 associated with muscle deposition [J]. Animal Genetics, 2015, 46(2): 158-163. doi: 10.1111/age.12271
[44] Sankar T S, Wastuwidyaningtyas B D, Dong Y, et al. The nature of mutations induced by replication–transcription collisions [J]. Nature, 2016, 535(7610): 178-181. doi: 10.1038/nature18316
[45] Paul S, Million-Weaver S, Chattopadhyay S, et al. Accelerated gene evolution through replication-transcription conflicts [J]. Nature, 2013, 495(7442): 512-515. doi: 10.1038/nature11989
[46] Froufe E, Alekseyev S, Alexandrino P, et al. The evolutionary history of sharp- and blunt-snouted lenok (Brachymystax lenok (Pallas, 1773)) and its implications for the paleo-hydrological history of Siberia [J]. BMC Evolutionary Biology, 2008, 8(1): 40. doi: 10.1186/1471-2148-8-40
[47] He Z, Li X, Yang M, et al. Speciation with gene flow via cycles of isolation and migration: insights from multiple mangrove taxa [J]. National Science Review, 2019, 6(2): 275-288. doi: 10.1093/nsr/nwy078
[48] Muhlfeld C C, Kovach R P, Al-Chokhachy R, et al. Legacy introductions and climatic variation explain spatiotemporal patterns of invasive hybridization in a native trout [J]. Global Change Biology, 2017, 23(11): 4663-4674. doi: 10.1111/gcb.13681
[49] 杨君兴, 潘晓赋, 陈小勇, 等. 中国淡水鱼类人工增殖放流现状 [J]. 动物学研究, 2013, 34(4): 267-280. Yang J X, Pan X F, Chen X Y, et al. Overview of the artificial enhancement and release of endemic freshwater fish in China [J]. Zoological Research, 2013, 34(4): 267-280.
[50] 任剑, 梁刚. 千河流域秦岭细鳞鲑资源调查报告 [J]. 陕西师范大学学报(自然科学版), 2004, 32(S2): 165-168. Ren J, Liang G. Resource survey report of Brachymystax lenok tsinlingensis in Qianhe River valleys of Qinling Mountains [J]. Journal of Shaanxi Normal University (Natural Science Edition), 2004, 32(S2): 165-168.
[51] Dharshini Kottaisamy C P, Raj D S, Dwivedi M. Insights into evolutionary and conservancy analytics on human Insulin Receptor Proteins [J]. Letters in Drug Design & Discovery, 2023, 20(5): 536-544.
[52] Payankaulam S, Raicu A M, Arnosti D N. Transcriptional regulation of INSR, the insulin receptor gene [J]. Genes, 2019, 10(12): 984. doi: 10.3390/genes10120984
[53] Clausen J O, Hansen T, Bjørbaek C, et al. Insulin resistance: interactions between obesity and a common variant of insulin receptor substrate-1 [J]. Lancet, 1995, 346(8972): 397-402.
[54] Chen Y, Huang L, Qi X, et al. Insulin receptor trafficking: consequences for insulin sensitivity and diabetes [J]. International Journal of Molecular Sciences, 2019, 20(20): 5007. doi: 10.3390/ijms20205007
[55] Gence L, Fernezelian D, Meilhac O, et al. Insulin signaling promotes neurogenesis in the brain of adult zebrafish [J]. The Journal of Comparative Neurology, 2023, 531(17): 1812-1827. doi: 10.1002/cne.25542
[56] Yang B, Zhai G, Gong Y, et al. Depletion of insulin receptors leads to β-cell hyperplasia in zebrafish [J]. Science Bulletin, 2017, 62(7): 486-492. doi: 10.1016/j.scib.2017.03.001
[57] Martinez G, Barbotin A L, Cazin C, et al. New mutations in DNHD1 cause multiple morphological abnormalities of the sperm flagella [J]. International Journal of Molecular Sciences, 2023, 24(3): 2559. doi: 10.3390/ijms24032559
[58] Tan C, Meng L, Lv M, et al. Bi-allelic variants in DNHD1 cause flagellar axoneme defects and asthenoteratozoospermia in humans and mice [J]. American Journal of Human Genetics, 2022, 109(1): 157-171. doi: 10.1016/j.ajhg.2021.11.022



 下载:
下载: