REDESCRIPTION AND MOLECULAR PHYLOGENETIC ANALYSIS ON MYXOBOLUS ACUTUS WU AND CHEN, 1987 (MYXOZOA: MYXOBOLIDAE)
-
摘要: 研究基于形态和分子信息重描述了寄生于嘉陵江重庆段鲫(Carassius auratus Linnaeus)鳃部和胆囊的尖形碘泡虫(Myxobolus acutus Wu and Chen, 1987), 并获得了该虫体的18S rDNA和ITS1 rDNA序列。尖形碘泡虫成熟孢子壳面观呈梨形, 前端稍尖, 后端钝圆, 缝面观呈宽纺锤形。孢子长(13.6±0.9) µm [(11.4—15.3) µm], 宽(10.2±0.9) µm [(7.5—12.8) µm], 厚(7.6±0.6) µm [(6.9—8.3) µm]。两梨形极囊开口处紧靠并位于孢子前端, 极囊大小不等, 大极囊长(6.2±0.4) µm [(5.1—7.5) µm], 宽(3.8±0.4) µm [(2.8—4.7) µm], 极丝盘绕5—8圈, 小极囊长(2.7±0.4) µm [(1.7—3.7) µm], 宽(1.4±0.2) µm [(0.9—1.9) µm], 极丝盘绕2—3圈。基于18S rDNA为分子标记的系统发育分析显示: 尖形碘泡虫与中华单极虫(Thelohanellus sinensis)有最近的亲缘关系, 两物种形成的进化支与贝壳碘泡虫(M. musseliusae)、苍梧碘泡虫(M. tsangwuensis)和鳃基碘泡虫(M. basilamellaris)形成的进化支呈姐妹群关系。通过系统发育与寄生部位关系的分析结果推测, 尖形碘泡虫的初始寄生部位可能为鳃, 而胆囊则是该物种后来适应的新的寄生部位。Abstract: Myxosporeans are obiligate endoparasites belonging to the phylum Cnidaria that includes mainly free-living species, such as sea anemones, hydras or jellyfish. Myxosporeans infecting wild and farmed fishes represent an important pathogenic group with a worldwide distribution. Myxosporidiosis can cause severe ecological and economic effects, which draw extensive attention to many people. Although myxosporeans were discovered almost 200 years ago, their classification was debated for a long time, especially about their higher taxonomic placement. Until recently, many discoveries sealed the demise of Myxozoa as a phylum and supported its inclusion in Cnidaria. Up to now, there are some 2600 described myxosporeans species with only about 23% of them have molecular sequence data. Therefore, there are still a lot of molecular information of known species to be supplemented and perfected. The traditional classification and identification of these species were based on their spore morphology. However, many taxonomists are aware of the limitations of the morphology-only classification because of the simplified body structure and the plasticity of some myxospores. Nowadays, almost all studies about taxonomy of myxosporeans are conducted using a combination of morphological and molecular data. Myxobolus acutus Wu and Chen, 1987 was first reported from gills and kidneys of Carassius auratus Linnaeus collected from Hubei, China, in the year 1983—1984. Wu and Chen named the species and gave a full description of the morphology of the parasite but without molecular data. This study redescribed the species infected the gills and gallbladders of C. auratus from Jialing River of Chongqing using the 18S rDNA and ITS1 rDNA sequences and its morphological and molecular data. The mature myxospores of M. acutus were pyriform with slightly narrow anterior and blunt posterior in valvular view. They were wide spindle-shaped in sutural view. The spores were (13.6±0.9) μm [(11.4—15.3) μm] in length, (10.2±0.9) μm [(7.5—12.8) μm] in width and (7.6±0.6) μm [(6.9—8.3) μm] in thickness. Two polar capsules with pores adjoined were unequal in the anterior of the spore. The larger polar capsules were pyriform with (6.2±0.4) μm [(5.1—7.5) µm] long and (3.8±0.4) μm [(2.8—4.7) μm] wide and 5—8 turns of polar filaments; the smaller ones were pyriform with (2.7±0.4) μm [(1.7—3.7) μm] long and (1.4±0.2) μm [(0.9—1.9) μm] wide and 2—3 turns of polar filaments. The 18S rDNA sequence similarity, genetic distance and variation site of the 7 strains of M. acutus were 100%, 0.000 and 0, respectively. ITS1 sequence analysis from three strains of M. acutus reflected genetic diversity and the different genetic resources of the two genotypes. Phylogenetic analysis based on 18S rDNA revealed that M. acutus and Thelohanellus sinensis had the closest relationship and they were clustered into a clade sister to the clade composing of M. musseliusae, M. tsangwuensis and M. basilamellaris. The analysis also indicates that the original parasitic site of M. acutus might be gill while gallbladder should be the later adaptive site of M. acutus.
-
黏孢子虫(Myxosporeans)是一类个体微小、形态简单且分布广泛的后生动物寄生虫, 主要寄生于鱼类, 少数寄生于两栖类、爬行类、鸟类和哺乳类[1-3]。迄今已记录的黏孢子虫有2600余种[4]。碘泡虫科(Myxobolidae Thélohan, 1892)是黏孢子虫中最大的一科, 包含碘泡虫属(Myxobolus Bütschli, 1882)、单极虫属(Thelohanellus Kudo, 1933)和尾孢虫属(Henneguya Thélohan, 1892)等, 其中碘泡虫属是该科中物种最丰富的属, 约有900种之多[5]。黏孢子虫早期的分类主要基于孢子形态, 然而后来大量的研究表明, 经典分类学很难对形态相似种进行有效区分, 特别是当其宿主特异性和组织趋向性极其相似的情况下, 鉴定工作尤为困难[6-9]。近30年来, 分子生物学方法的介入, 为黏孢子虫分类学的发展起到了极大的促进作用, 解决了诸多经典分类学未能妥善处理的问题, 厘清了过去一些类群划分和物种鉴定的遗留问题[8, 10, 11]。然而在全世界所记录的黏孢子虫中, 仅有约23%的物种具有分子序列数据, 因此仍有大量已知种的分子信息亟待补充和完善[4]。
鲫(Carassius auratus Linnaeus)具有生长速度快、繁殖能力强、肉质鲜美和营养价值高等特点, 是我国重要的淡水养殖鱼类[12]。同时, 鲫也是黏孢子虫病发生率较高的经济鱼类之一, 据统计, 寄生于鲫的碘泡虫就达64种之多[13-15], 其中包含尖形碘泡虫Myxobolus acutus Wu and Chen, 1987。尖形碘泡虫由吴灶和与陈启鎏在湖北五湖发现并命名, 其宿主为鲫, 寄生部位为肾和鳃[16]。因条件限制, 当时并未提供分子序列信息。本研究在嘉陵江重庆段检获尖形碘泡虫, 宿主为鲫, 寄生部位为鳃和胆囊, 这是续发现该物种30余年以来的第一次记录。本研究首次提供了尖形碘泡虫的18S rDNA及ITS1序列, 并基于形态和分子信息对其进行重描述的基础上, 开展了分子系统学研究, 以期为人们进一步了解该寄生虫的进化生物学特征及鱼类病原鉴定积累基础资料。
1. 材料与方法
1.1 样本采集与物种鉴定
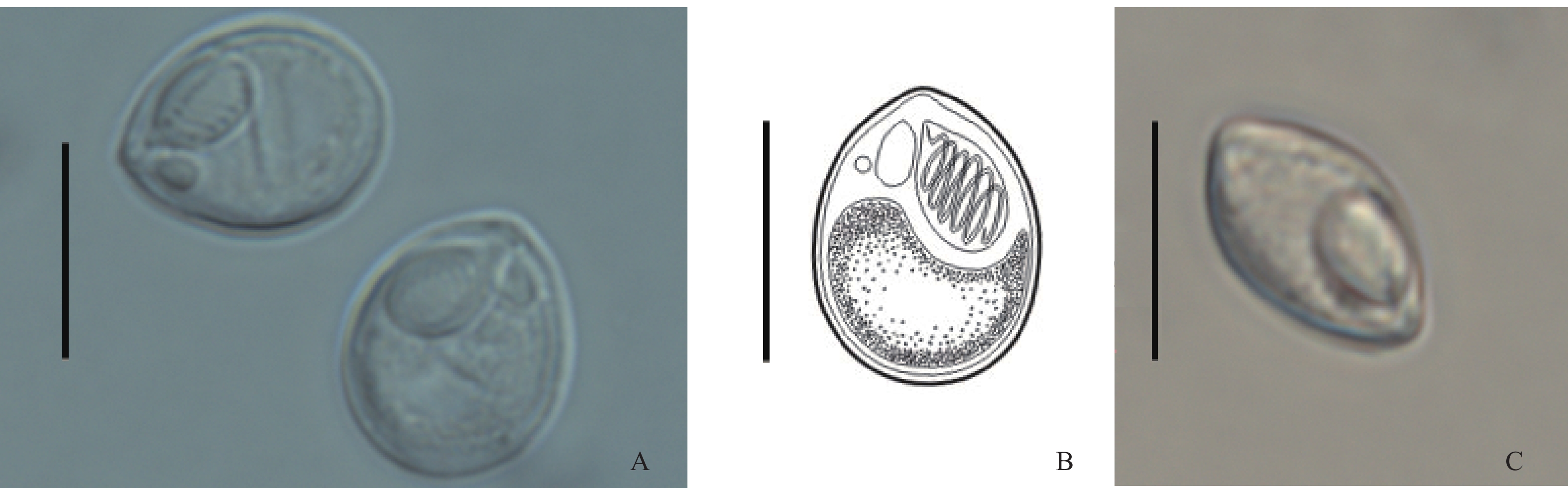
2015年4月、2018年4月和2019年5月在嘉陵江重庆段共采集鲫76尾。活体送往重庆市动物生物学重点实验室用过量的MS-222麻醉剂(350 mg/L)进行安乐死, 随后剖检, 用肉眼检查体表、鳃、肌肉、肝胰脏、肠、脾脏、心脏、胆囊、肾脏、膀胱等部位是否有明显病症及黏孢子虫孢囊, 镜检各组织器官涂片中分散孢子的存在。后对获取的黏孢子虫新鲜样本直接进行图像采集(图 1)及基因组DNA提取等工作, 对黏孢子虫样本的处理和种类鉴定参照文献[12]进行。
1.2 DNA提取与PCR反应
DNA提取 将从宿主鲫的鳃部获得的黏孢子虫孢囊用镊子小心地剥离至1.5 mL离心管中, 用灭菌后的解剖针戳破后立即挑取部分孢子镜检, 显微拍照, 剩下的孢子分散于盛有灭菌双蒸水的离心管中, 离心富集, 悬浮洗2—3次以除去杂质。从宿主胆囊中检获的黏孢子虫立即镜检, 显微拍照, 剩余胆汁保存于1.5 mL离心管中, 从离心管中吸取10 µL含有孢子的胆汁, 用灭菌后的双蒸水清洗2—3次, 除去杂质。按照DNeasy Tissue Kit(QIAGEN, Germany)试剂盒的使用说明书对黏孢子虫基因组DNA进行提取, 用1.5%琼脂糖凝胶电泳进行检测, 将获得的基因组DNA溶液在−20℃条件下保存备用。另外, 按照海洋动物组织 DNA提取试剂盒(TIANGEN, China)的说明书对宿主鱼基因组DNA进行提取, 用1.5%琼脂糖凝胶电泳进行检测, 将获得的宿主鱼基因组DNA溶液在−20℃条件下保存备用。
PCR反应 对提取成功的黏孢子虫样本基因组DNA进行18S rDNA序列片段扩增, 扩增引物为18E: 5′-CTGGTTGATCCTGCCAGT-3′和18R: 5′-CTACGGAAACCTTGTTACG-3′[17, 18]。20 µL的PCR反应体系: 引物各0.5 μL, 模板DNA 5 μL, Mix(上海英潍捷基生物公司)5 μL, 然后添加超纯水补至20 μL; 反应程序为: 94℃预变性90s, 94℃变性20s, 56℃退火20s, 72℃延伸2min, 循环35次, 最后72℃再次延伸5min, 反应完成后于PCR仪12℃条件下保温。将PCR反应产物通过1.5%的琼脂糖凝胶电泳检测, 然后将有目的条带的PCR产物用胶回收试剂盒Gel Extraction Kit(OMEGA, America)纯化回收。将每个回收产物插入pMD18-T载体(TaKaRa, Japan), 随后导入大肠杆菌(Escherichia coli)中进行单克隆培养, 将2个克隆子送英潍捷基(上海)生物公司测序。黏孢子虫ITS1序列扩增引物为28S1R: 5'-GTGTTTCAAGACGGGTCG-3' 和ERIB10-V: 5'-CCGTAGGTGAACCTGCGGAAG-3' , 采用上述相似的方法进行PCR扩增。宿主鱼的COI基因部分序列的PCR扩增参照文献[19]。
1.3 序列分析与系统发育
序列分析 样本序列与相似度较高物种序列之间的遗传距离用MEGA6.0软件在K2P模型下计算获得。序列相似度借助在线软件Pairwise Sequence Alignment (网址: www.ebi.ac.uk/Tools/psa/)基于Global Alignment模式计算获得。序列间变异位点采用Bioedit软件分析。
系统发育分析 用于构建系统发育树的黏孢子虫18S rDNA序列共有66条, 其中包括本研究得到的1条尖形碘泡虫代表序列和65条与尖形碘泡虫相似度较高的序列(通过NCBI在线BLAST结果), 包括碘泡虫、单极虫、尾孢虫等。另外, 选用Tetracapsuloides bryosalmonae(KF731712)和Buddenbrockia plumatellae(AY074915)为外群。利用在线软件The CIPRES Science Gateway V.3.3 (网址: http://www.phylo.org/)中的RAxML-HPC2 XSEDE(8.2.12)模式构建最大似然树(Maximum likelihood, ML), 并选择1000次自举(Bootstrap)重复检测。利用MrBayes 3.1.2软件构建贝叶斯树(Bayesian inference, BI), 位点变异设置为invgamma分布, 序列最佳进化模型为GTR+I+G(通过Model test 3.7计算获得), 运行10000000代, 每200代抽样1次, 在舍弃25%的老化样本后, 根据剩余样本构建一致树。系统树的绘制由FigTree v1.4.2和Photoshop共同完成[20]。
1.4 主成分分析
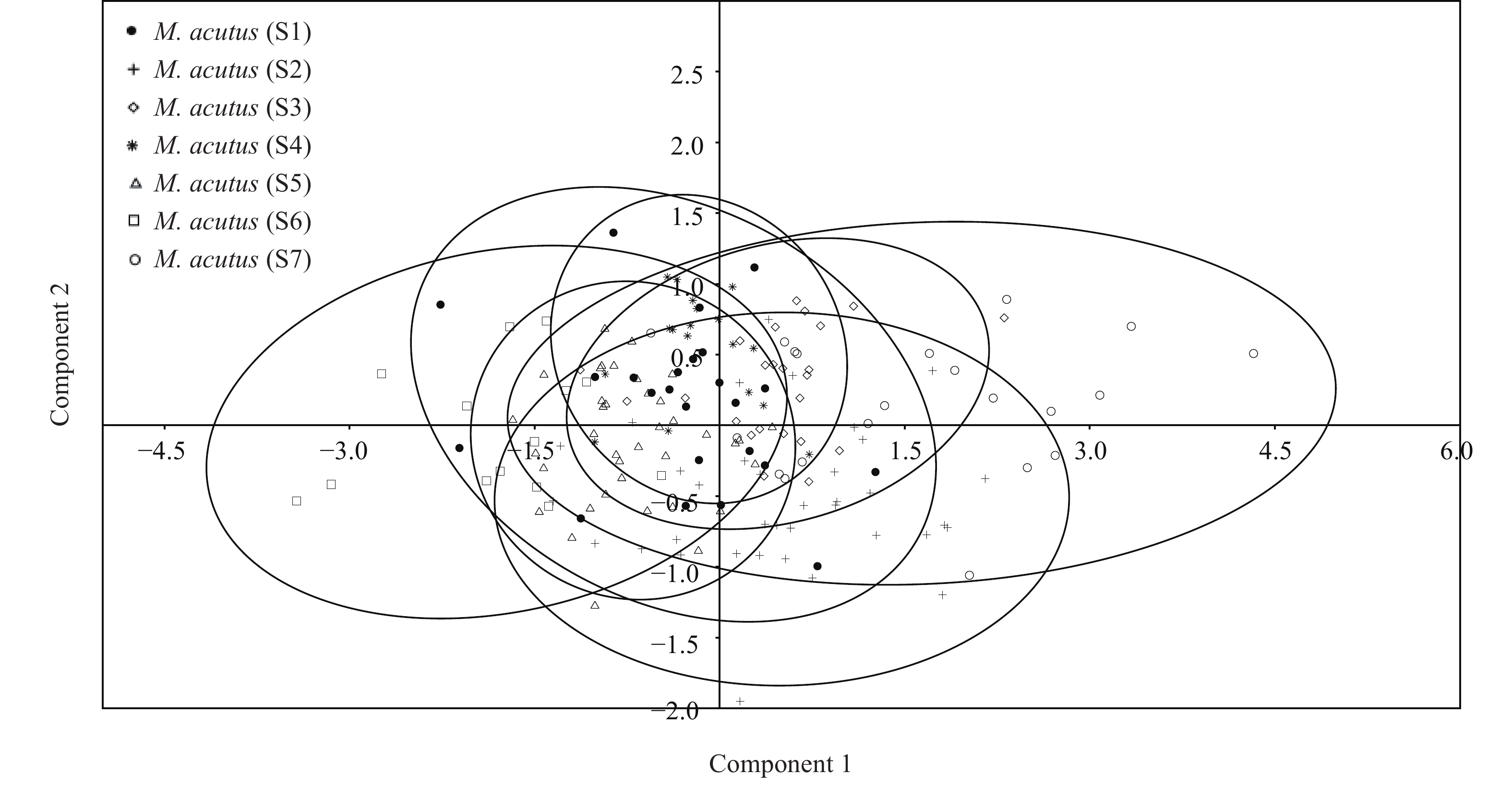
基于成熟孢子的孢子长、孢子宽、大极囊长、大极囊宽、小极囊长和小极囊宽的测量值, 利用PAST3进行主成分分析(PCA), 以分析尖形碘泡虫7个株系间的形态差异。使用变量协变矩阵生成具有95.0%置信的散点图。
2. 结果
基于形态及COI基因测序(GenBank登录号: MZ769123)鉴定宿主鱼为鲫。本实验共发现7尾鲫感染尖形碘泡虫(感染率为9.2%), 其中6尾感染部位为鳃, 均形成乳白色圆形孢囊(直径为1—2 mm), 1尾感染部位为胆囊, 孢子游离于胆汁中, 未形成孢囊。本文将从上述感染宿主中获得的尖形碘泡虫分离株称为株系, 共得到7个分离株即S1—S7株系, 整体称为重庆株系。
2.1 尖形碘泡虫Myxobolus acutus Wu and Chen, 1987重庆株系形态学描述
尖形碘泡虫重庆株系成熟孢子壳面观呈梨形, 前端稍尖, 后端钝圆, 缝面观呈宽纺锤形(图 1)。孢子长(13.6±0.9) µm [(11.4—15.3) µm] (n=175), 宽(10.2±0.9) µm [(7.5—12.8) µm] (n=175), 厚(7.6±0.6) µm [(6.9—8.3) µm] (n=5)。两梨形极囊开口处紧靠并位于孢子前端, 极囊大小不等, 大极囊长(6.2±0.4) µm [(5.1—7.5) µm] (n=175), 宽(3.8±0.4) µm [(2.8—4.7) µm] (n=175), 极丝盘绕5—8圈, 小极囊长(2.7±0.4) µm [(1.7—3.7) µm] (n=175), 宽(1.4±0.2) µm [(0.9—1.9) µm] (n=175), 极丝盘绕2—3圈。尖形碘泡虫重庆7株系形态与原始描述相符(图 1和表 1)[16]。通过比较发现, 与尖形碘泡虫形态较相似的种有微孢碘泡虫(Myxobolus microspores Li and Nie, 1973)、葡萄碘泡虫(Myxobolus acinosus Nie and Li, 1973)和异样碘泡虫(Myxobolus diversus Nie and Li, 1973)。与微孢碘泡虫相比, 尖形碘泡虫的孢子略大(11.3—15.5 µm vs. 9.6—12.0 µm)。葡萄碘泡虫孢子呈茄形, 前端狭窄而稍弯, 这与尖形碘泡虫的梨形孢子前端略尖且不弯曲的形态有所不同。异样碘泡虫的孢子比尖形碘泡虫稍大(13.2—16.8 µm vs. 11.3—15.5 µm), 且大极囊长约占孢子长的1/3, 而尖形碘泡虫的大极囊长约占孢子长的1/2(表 1)[21]。
表 1 尖形碘泡虫与相似种的形态学比较Table 1. Morphological comparison of Myxobolus acutus with its similar species (µm)碘泡虫物种
Myxobolus spp.宿主
Host寄生部位
Infection site采集地
Location孢子长
SL孢子宽
SW孢子厚
ST极囊长×宽
PCL×PCW资料来源
Data resourceM. acutus 鲫 鳃、肾 湖北 13.5
(12.9—14.3)10.1
(9.0—11.2)7.4
(6.7—8.1)5.8(5.2—7.1)×4.3(2.4—4.8)
3.2(2.4—4.8)×1.3(1.2—2.1)[16] M. acutus (S1)
(n=24)鲫 鳃 重庆 13.2
(11.4—14.6)10.0
(8.5—11.1)7.9 6.2(5.5—7.5)×3.8(2.8—4.5)
2.6(2.0—3.4)×1.7(0.9—1.8)本研究 M. acutus (S2)
(n=36)鲫 鳃 重庆 14.3
(12.8—15.3)10.3
(9.0—12.2)— 6.0(5.2—6.7)×3.9(2.8—4.6)
2.6(1.9—3.6)×1.3(1.0—1.7)本研究 M. acutus (S3)
(n=24)鲫 胆囊 重庆 13.7
(12.6—14.6)10.7
(10.1—12.6)— 6.4(5.2—7.1)×3.7(3.0—4.3)
2.7(2.2—3.1)×1.4(1.0—1.8)本研究 M. acutus (S4)
(n=18)鲫 鳃 重庆 13.0
(12.2—14.2)10.5
(9.4—10.7)— 6.2(5.5—7.2)×3.9(3.4—4.5)
2.7(2.0—3.6)×1.3(0.9—1.8)本研究 M. acutus (S5)
(n=38)鲫 鳃 重庆 13.8
(12.4—14.2)9.7
(8.7—10.4)7.9
(7.5—8.3)6.1(5.2—6.9)×3.6(2.8—4.5)
2.6(2.0—3.2)×1.3(1.0—1.8)本研究 M. acutus (S6)
(n=14)鲫 鳃 重庆 12.4
(11.6—13.5)9.0
(7.5—9.8)7.1
(6.9—7.2)5.8(5.1—6.5)×3.4(2.8—4.1)
2.6(1.7—3.0)×1.4(1.1—1.6)本研究 M. acutus (S7)
(n=21)鲫 鳃 重庆 14.1
(12.7—15.1)10.9
(10.1—12.8)— 6.3(6.0—6.8)×4.2(3.7—4.5)
3.0(2.4—3.7)×1.4(1.1—1.9)本研究 M. microsporus 草鱼 脾、膀胱、鳃、肾 湖北 10.8
(10.2—12.0)7.1
(6.2—8.2)5.4 5.1(5.0—5.6)×3.0(2.8—3.6)
2.5(2.4—2.6)×1.4(1.2—1.8)[21] M. acinosus 鲤 鳃 湖北 10.0 (9.6—10.8) 5.6
(5.4—6.0)4.8 4.6 (3.8—4.9)×2.4
—[21] M. diversus 鲫 脾、肾、
胆囊、
肠、肌肉、
膀胱湖北 15.4
(13.2—16.8)9.0
(7.8—9.6)6.9
(6.6—7.2)5.8(4.8—6.0)×3.4(3.0—3.6)
2.8(2.4—3.0)×1.6(1.2—1.8)[21] 注: S 株系; SL 孢子长; SW 孢子宽; ST 孢子厚; PCL 极囊长; PCW极囊宽; — 无数据Note: S. strain; SL. spore length; SW. spore width; ST. spore thickness; PCL. polar capsule length; PCW. polar capsule width; —. no data 主成分分析结果显示, 本研究所检获的尖形碘泡虫7株系间(S1—S7)孢子形态量度无显著差异(图 2)。
2.2 尖形碘泡虫18S rDNA分子特征及系统发育分析
获得尖形碘泡虫S1—S7株系18S rDNA序列片段长度分别为1851 nt(GenBank登录号: MZ782721)、1932 nt(GenBank登录号: MZ782722)、1896 nt(GenBank登录号: MZ782723)、1871 nt(GenBank登录号: MZ782724)、1810 nt(GenBank登录号: MZ782725)、1677 nt(GenBank登录号: MZ782726)和1839 nt(GenBank登录号: MZ782727)。7株系间序列相似度为100%, 遗传距离为0, 变异位点0个, 即7株系18S rDNA序列为同一基因型。尖形碘泡虫18S rDNA序列与GenBank数据库中的中华单极虫(Thelohanellus sinensis, KY469292)相似度最高(95.4%), 遗传距离最小(0.047), 其次为苍梧碘泡虫(Myxobolus tsangwuensis, KJ561441; 93.6%, 0.081)和贝壳碘泡虫(Myxobolus musseliusae, FJ710801; 93.2%, 0.080)。
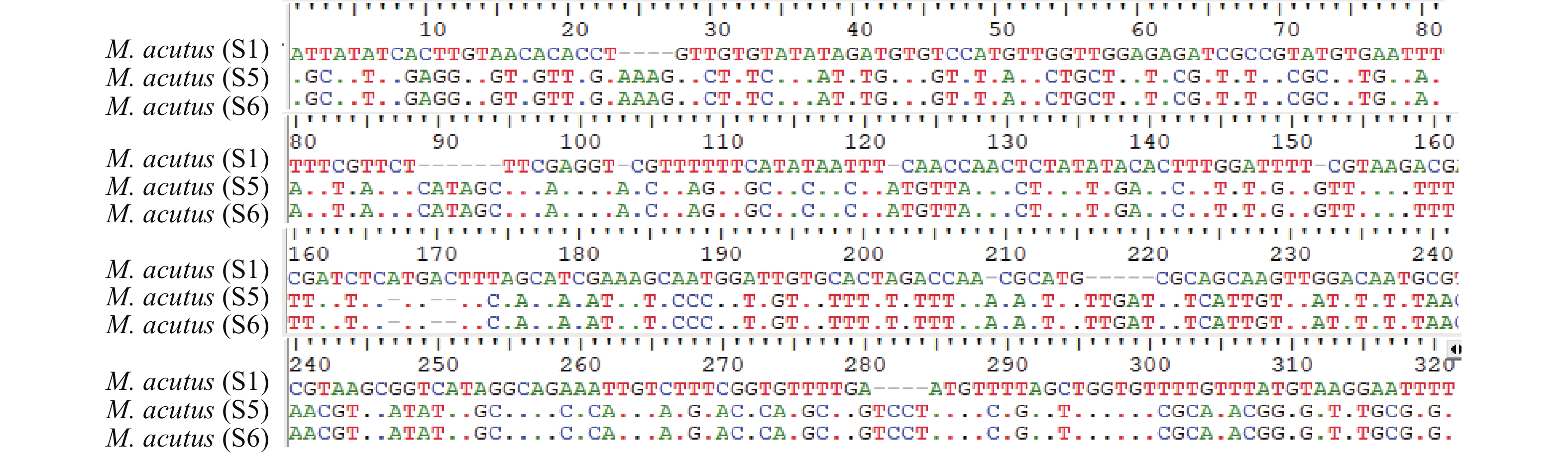
本研究获得株系S1、S5和S6的ITS1序列, 长度分别为298、318和318 nt。序列分析结果显示, 株系S5与株系S6共享同一基因型, 该基因型与株系S1的基因型序列差异较大, 差异位点数有168个(图 3)。
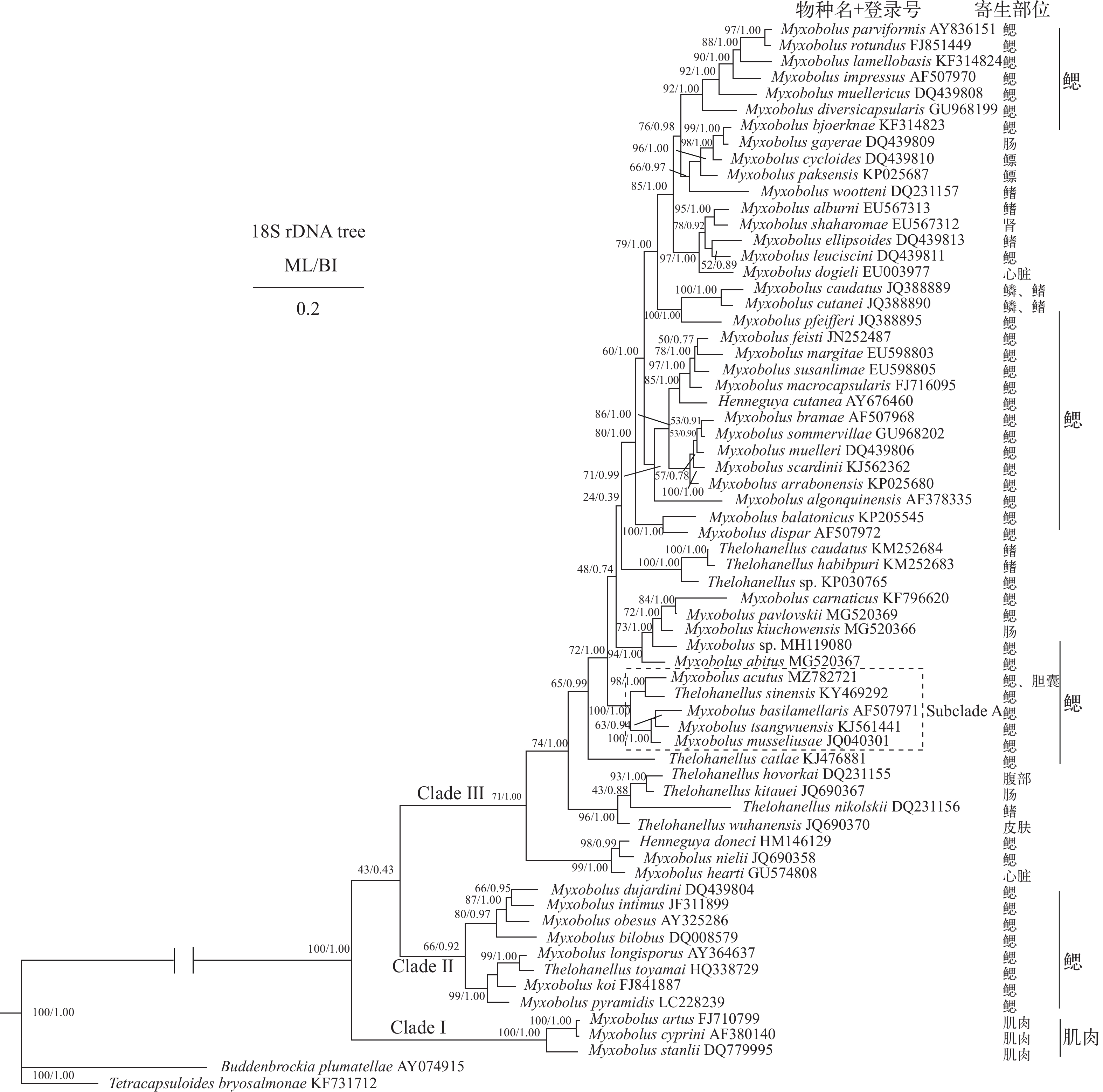
本研究构建的ML树和BI树拓扑结构一致(图 4)。系统树聚为三大支系, 其中进化支Clade Ⅰ处于系统树的基部位置, 后依次为Clade Ⅱ和Clade Ⅲ进化支。尖形碘泡虫位于Clade Ⅲ支系中Subclade A亚支: 尖形碘泡虫与中华单极虫(KY469292)聚为一支, 该支与贝壳碘泡虫(JQ040301)、苍梧碘泡虫(KJ561441)和鳃基碘泡虫(AF507971)形成的进化支呈姐妹群关系(图 4)。
3. 讨论
本研究获得的尖形碘泡虫孢子形态符合原始描述。宿主鲫的胆囊为尖形碘泡虫的感染部位新记录, 重庆地区为地理新分布。原始报道的尖形碘泡虫仅以游离孢子的形式存在, 而本研究发现该物种可以形成孢囊。尖形碘泡虫重庆各株系间成熟孢子形态相似, 主成分分析结果进一步表明各株系间孢子形态量度无显著差异, 应为同一物种。同时, 7株系间18S rDNA序列无差异, 进一步证实这些株系为同一物种。
以往的研究表明, ITS1是研究物种种内关系的理想分子标记, 在不同生物类群中得到了广泛应用[22-27], 而在黏孢子虫类群中的相关应用则很少[28-30]。本研究分别获得了尖形碘泡虫S1、S5和S6株系的ITS1序列。序列分析显示, S5和S6共享1个基因型, 该基因型与S1的序列存在很大差异(共有168个差异位点)。这表明尖形碘泡虫在嘉陵江重庆段江域具有一定程度的遗传多样性水平, 并且S1可能与S5和S6有着不同的遗传来源。
本研究系统发育分析显示, 处于分化较早支系的寄生虫其寄生部位表现出了较高的一致性, 如Clade Ⅰ物种的寄生部位均为肌肉, Clade Ⅱ物种的寄生部位均为鳃。而分化较晚的Clade Ⅲ支系, 虽然没有完全表现出寄生部位的高度一致性, 但在一些小的进化亚支中的物种仍有较为一致的寄生部位(图 4)。这表明, 碘泡虫科物种的系统发育与其寄生部位有着较为密切的关系。在碘泡虫科物种进化过程中, 逐渐由原来的寄生部位高度一致性向多寄生部位演化, 在分化最晚的Clade Ⅲ进化支中即出现了一些物种具有多寄生部位的现象(图 4)。从进化角度来看, 在一个支系中大多数物种共有的寄生部位应是初始寄生部位, 其他的则是后来适应的新寄生部位。如Subclade A进化亚支中, 物种均寄生于鳃部, 而其中的尖形碘泡虫不仅可寄生于鳃, 还可寄生于胆囊(图 4), 从系统发育与寄生部位演化的角度推测, 尖形碘泡虫的初始寄生部位应为鳃, 而胆囊则是其后来适应的新的寄生部位。
-
表 1 尖形碘泡虫与相似种的形态学比较
Table 1 Morphological comparison of Myxobolus acutus with its similar species (µm)
碘泡虫物种
Myxobolus spp.宿主
Host寄生部位
Infection site采集地
Location孢子长
SL孢子宽
SW孢子厚
ST极囊长×宽
PCL×PCW资料来源
Data resourceM. acutus 鲫 鳃、肾 湖北 13.5
(12.9—14.3)10.1
(9.0—11.2)7.4
(6.7—8.1)5.8(5.2—7.1)×4.3(2.4—4.8)
3.2(2.4—4.8)×1.3(1.2—2.1)[16] M. acutus (S1)
(n=24)鲫 鳃 重庆 13.2
(11.4—14.6)10.0
(8.5—11.1)7.9 6.2(5.5—7.5)×3.8(2.8—4.5)
2.6(2.0—3.4)×1.7(0.9—1.8)本研究 M. acutus (S2)
(n=36)鲫 鳃 重庆 14.3
(12.8—15.3)10.3
(9.0—12.2)— 6.0(5.2—6.7)×3.9(2.8—4.6)
2.6(1.9—3.6)×1.3(1.0—1.7)本研究 M. acutus (S3)
(n=24)鲫 胆囊 重庆 13.7
(12.6—14.6)10.7
(10.1—12.6)— 6.4(5.2—7.1)×3.7(3.0—4.3)
2.7(2.2—3.1)×1.4(1.0—1.8)本研究 M. acutus (S4)
(n=18)鲫 鳃 重庆 13.0
(12.2—14.2)10.5
(9.4—10.7)— 6.2(5.5—7.2)×3.9(3.4—4.5)
2.7(2.0—3.6)×1.3(0.9—1.8)本研究 M. acutus (S5)
(n=38)鲫 鳃 重庆 13.8
(12.4—14.2)9.7
(8.7—10.4)7.9
(7.5—8.3)6.1(5.2—6.9)×3.6(2.8—4.5)
2.6(2.0—3.2)×1.3(1.0—1.8)本研究 M. acutus (S6)
(n=14)鲫 鳃 重庆 12.4
(11.6—13.5)9.0
(7.5—9.8)7.1
(6.9—7.2)5.8(5.1—6.5)×3.4(2.8—4.1)
2.6(1.7—3.0)×1.4(1.1—1.6)本研究 M. acutus (S7)
(n=21)鲫 鳃 重庆 14.1
(12.7—15.1)10.9
(10.1—12.8)— 6.3(6.0—6.8)×4.2(3.7—4.5)
3.0(2.4—3.7)×1.4(1.1—1.9)本研究 M. microsporus 草鱼 脾、膀胱、鳃、肾 湖北 10.8
(10.2—12.0)7.1
(6.2—8.2)5.4 5.1(5.0—5.6)×3.0(2.8—3.6)
2.5(2.4—2.6)×1.4(1.2—1.8)[21] M. acinosus 鲤 鳃 湖北 10.0 (9.6—10.8) 5.6
(5.4—6.0)4.8 4.6 (3.8—4.9)×2.4
—[21] M. diversus 鲫 脾、肾、
胆囊、
肠、肌肉、
膀胱湖北 15.4
(13.2—16.8)9.0
(7.8—9.6)6.9
(6.6—7.2)5.8(4.8—6.0)×3.4(3.0—3.6)
2.8(2.4—3.0)×1.6(1.2—1.8)[21] 注: S 株系; SL 孢子长; SW 孢子宽; ST 孢子厚; PCL 极囊长; PCW极囊宽; — 无数据Note: S. strain; SL. spore length; SW. spore width; ST. spore thickness; PCL. polar capsule length; PCW. polar capsule width; —. no data -
[1] MacKenzie K, Kalavati C. Myxosporean parasites of marine fishes: their distribution in the world’s oceans [J]. Parasitology, 2014, 141(13): 1709-1717. doi: 10.1017/S0031182014001425
[2] Hallett S L, Hartigan A, Atkinson S D. Myxozoans on the Move: Dispersal Modes, Exotic Species and Emerging Diseases [M]//Okamura B, Gruhl A, Bartholomew J (Eds.), Myxozoan Evolution, Ecology and Development. Cham: Springer, 2015: 343-362.
[3] 陈围, 杨承忠, 赵元莙. 碘泡虫属粘孢子虫分子进化及其与宿主协同关系的研究 [J]. 四川动物, 2016, 35(2): 183-189. doi: 10.11984/j.issn.1000-7083.20150322 Chen W, Yang C Z, Zhao Y J. Molecular evolution of Myxobolus (Myxosporea) and coevolution with their hosts [J]. Sichuan Journal of Zoology, 2016, 35(2): 183-189. doi: 10.11984/j.issn.1000-7083.20150322
[4] Okamura B, Hartigan A, Naldoni J. Extensive uncharted biodiversity: the parasite dimension [J]. Integrative and Comparative Biology, 2018, 58(6): 1132-1145.
[5] Úngari L P, Vieira D H M D, Santos A L Q, et al. Myxobolus spp. (Cnidaria: Myxobolidae) in the circulating blood of fishes from Goiás and Mato Grosso States, Brazil: case report [J]. Brazilian Journal of Biology, 2022, 82(3): e242823.
[6] Liu Y, Whipps C M, Gu Z M, et al. Myxobolus musseliusae (Myxozoa: Myxobolidae) from the gills of common carp Cyprinus carpio and revision of Myxobolus dispar recorded in China [J]. Parasitology Research, 2013, 112(1): 289-296. doi: 10.1007/s00436-012-3136-y
[7] Molnár K. Remarks to the validity of GenBank sequences of Myxobolus spp. (Myxozoa, Myxosporidae) infecting Eurasian fishes [J]. Acta Parasitologica, 2011, 56(3): 263-269.
[8] 刘晓聪, 杨承忠, 赵元莙. 洪湖碘泡虫的再描述及其近缘种的鉴别性研究 [J]. 水生生物学报, 2016, 40(2): 350-357. Liu X C, Yang C Z, Zhao Y J. Redescription of Myxobolus honghuensis Liu et al. 2012 and identification on its genetic related species [J]. Acta Hydrobiologica Sinica, 2016, 40(2): 350-357.
[9] 李超, 索栋, 杨承忠, 等. 楔形两极虫(黏体门, 双壳目)的形态学重描述及其近缘种的分子系统学研究 [J]. 四川动物, 2016, 35(3): 384-390. doi: 10.11984/j.issn.1000-7083.20150350 Li C, Suo D, Yang C Z, et al. Redescription of Myxidium cuneiforme Fujita, 1924 (Myxosporea: Bivalvulida) and molecular phylogeny with its relative species [J]. Sichuan Journal of Zoology, 2016, 35(3): 384-390. doi: 10.11984/j.issn.1000-7083.20150350
[10] Liu X, Zhang D, Yang C, et al. Morphological and molecular identification of Myxobolus parakoi sp. nov (Myxozoa: Myxobolidae), from Cyprinus carpio in Chongqing China [J]. Zootaxa, 2019, 4657(1): 117-126. doi: 10.11646/zootaxa.4657.1.4
[11] Zhao Y J, Li N N, Tang F H, et al. Remarks on the validity of Myxobolus ampullicapsulatus and Myxobolus honghuensis (Myxozoa: Myxosporea) based on SSU rDNA sequences [J]. Parasitology Research, 2013, 112(11): 3817-3823. doi: 10.1007/s00436-013-3569-y
[12] 赵元莙, 马成伦, 宋微波. 海水养殖中原生动物病原虫的鉴定—Ⅱ粘孢子虫的研究及鉴定方法 [J]. 青岛海洋大学学报(自然科学版), 2001, 31(5): 681-688. doi: 10.3969/j.issn.1672-5174.2001.05.007 Zhao Y J, Ma C L, Song W B. Illustrated guide to the identification of pathogenetic protozoa in maricuture-Ⅱ diagnostic methods for the myxosporean [J]. Journal of Ocean University of Qingdao, 2001, 31(5): 681-688. doi: 10.3969/j.issn.1672-5174.2001.05.007
[13] 陈启鎏, 马成伦. 中国动物志, 粘体门 [M]. 北京: 科学出版社, 1998: 412-524. Chen Q L, Ma C L. China Fauna: Myxozoa, Bivalvulida (Freshwater) [M]. Beijing: Science Press, 1998: 412-524
[14] Eiras J C, Molnár K, Lu Y S. Synopsis of the species of Myxobolus Butschli, 1882 (Myxozoa: Myxosporea: Myxobolidae) [J]. Systematic Parasitology, 2005(61): 1-46. doi: 10.1007/s11230-004-6343-9
[15] Eiras J C, Zhang J, Molnár K. Synopsis of the species of Myxobolus Bütschli, 1882 (Myxozoa: Myxosporea, Myxobolidae) described between 2005 and 2013 [J]. Systematic Parasitology, 2014, 88(1): 11-36. doi: 10.1007/s11230-014-9484-5
[16] 吴灶和, 陈启鎏. 淡水鱼类寄生粘孢子虫九新种 [J]. 水生生物学报, 1987, 11(2): 161-172. Wu Z H, Chen Q L. Nine new species of myxosporidia from freshwater fish of Wuhu Lake, Hubei, China [J]. Acta Hydrobiologica Sinica, 1987, 11(2): 161-172.
[17] Hillis D M, Dixon M T. Ribosomal DNA: molecular evolution and phylogenetic inference [J]. The Quarterly Review of Biology, 1991, 66(4): 411-453. doi: 10.1086/417338
[18] Whipps C M, Adlard R D, Bryant M S, et al. First report of three Kudoa species from eastern Australia: Kudoa thyrsites from mahi mahi (Coryphaena hippurus), Kudoa amamiensis and Kudoa minithyrsites n. sp. from sweeper (Pempheris ypsilychnus) [J]. Journal of Eukaryotic Microbiology, 2003, 50(3): 215-219. doi: 10.1111/j.1550-7408.2003.tb00120.x
[19] Ward R D, Zemlak T S, Innes B H, et al. DNA barcoding Australia’s fish species [J]. Philosophical Transactions of the Royal Society of London Series B, Biological Sciences, 2005, 360(1462): 1847-1857. doi: 10.1098/rstb.2005.1716
[20] 李楠楠, 赵元莙, 唐发辉, 等. 基于18Sr DNA序列对单尾虫属(粘体门, 双壳目)的系统学研究 [J]. 内江师范学院学报, 2012, 27(12): 38-42. doi: 10.3969/j.issn.1671-1785.2012.12.011 Li N N, Zhao Y J, Tang F H, et al. Phylogenetic Study on genus Unicauda (Myxozoa, Bivalvulida) based on 18S rDNA sequences [J]. Journal of Neijiang Normal University, 2012, 27(12): 38-42. doi: 10.3969/j.issn.1671-1785.2012.12.011
[21] 湖北省水生生物研究所. 湖北省鱼病病原区系图志 [M]. 北京: 科学出版社, 1973: 74-75. Hubei Institute of Hydrobiology. Flora of Fish Diseases in Hubei Province [M]. Beijing, China: Science Press, 1973: 74-75
[22] Hoste H, Gasser R B, Chilton N B, et al. Lack of intraspecific variation in the second Internal Transcribed Spacer (ITS-2) of Trichostrongylus colubriformis ribosomal DNA [J]. International Journal for Parasitology, 1993, 23(8): 1069-1071. doi: 10.1016/0020-7519(93)90128-L
[23] Coleman A W, Mai J C. Ribosomal DNA ITS-1 and ITS-2 sequence comparisons as a tool for predicting genetic relatedness [J]. Journal of Molecular Evolution, 1997, 45(2): 168-177. doi: 10.1007/PL00006217
[24] De Barro P J, Driver F, Trueman J W H, et al. Phylogenetic relationships of world populations of Bemisia tabaci (Gennadius) using ribosomal ITS1 [J]. Molecular Phylogenetics and Evolution, 2000, 16(1): 29-36. doi: 10.1006/mpev.1999.0768
[25] Harris D J, Crandall K A. Intragenomic variation within ITS1 and ITS2 of freshwater crayfishes (Decapoda: Cambaridae): implications for phylogenetic and microsatellite studies [J]. Molecular Biology and Evolution, 2000, 17(2): 284-291. doi: 10.1093/oxfordjournals.molbev.a026308
[26] Cooke D E L, Duncan J M. Phylogenetic analysis of Phytophthora species based on ITS1 and ITS2 sequences of the ribosomal RNA gene repeat [J]. Mycological Research, 1997, 101(6): 667-677. doi: 10.1017/S0953756296003218
[27] Phillips R B, Gudex L I, Westrich K M, et al. Combined phylogenetic analysis of ribosomal ITS1 sequences and new chromosome data supports three subgroups of Dolly Varden char (Salvelinus malma) [J]. Canadian Journal of Fisheries and Aquatic Sciences, 1999, 56(8): 1504-1511. doi: 10.1139/f99-103
[28] Whipps C M, El-Matbouli M, Hedrick R P, et al. Myxobolus cerebralis internal transcribed spacer 1 (ITS-1) sequences support recent spread of the parasite to North America and within Europe [J]. Diseases of Aquatic Organisms, 2004, 60(2): 105-108.
[29] 高永杰, 杨承忠, 赵元莙. 多涅茨尾孢虫ITS-5.8S rDNA的种群地理学研究 [J]. 重庆师范大学学报(自然科学版), 2015, 32(3): 48-53. Gao Y J, Yang C Z, Zhao Y J. Population geography of Henneguya doneci base on ITS-5.8S rDNA [J]. Journal of Chongqing Normal University (
Natural Science ) , 2015, 32(3): 48-53. [30] 黄艳梅, 赵元莙, 周杨, 等. 石斑角形虫(黏体门, 角形虫科)的分子证据及其在不同宿主中的遗传变异 [J]. 水生生物学报, 2020, 44(6): 1263-1269. doi: 10.7541/2020.147 Huang Y M, Zhao Y J, Zhou Y, et al. First molecular evidence of Ceratomyxa epinephela (Myxozoa: Ceratomyxidae) and its genetic variation from different host species [J]. Acta Hydrobiologica Sinica, 2020, 44(6): 1263-1269. doi: 10.7541/2020.147
-
期刊类型引用(1)
1. 陆子茜. 透镜碘泡虫的研究进展. 生物化工. 2024(01): 220-222 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: