PHYSIOLOGICAL EFFECTS OF SALT STRESS ON LARGE-FRAGMENT DELETION MUTANTS OF SYNECHOCOCCUS ELONGATUS PCC 7942
-
摘要: 在对聚球藻PCC 7942开展基因组简化的过程中, 发现一些非必需大片段的删除可导致耐盐胁迫能力降低。突变株∆Synpcc7942_0233-0253和∆Synpcc7942_2169-2187, 其基因组中分别删除了18和14 kb的区域, 在BG11培养液中的生长与野生型没有显著差异, 但在含有0.4 mol/L NaCl的培养液中的生长相对于野生型被严重抑制。进一步分析发现, 在盐胁迫下2个突变株的光合放氧速率比野生型显著下降, 光系统Ⅰ和Ⅱ电子传递速率均低于野生型, 呼吸耗氧速率与野生型相比却维持在较高水平。这些结果说明, 蓝藻基因组中有些非必需基因实际上对于适应胁迫条件是需要的。
-
关键词:
- 聚球藻PCC 7942 /
- 大片段删除突变株 /
- 盐胁迫 /
- 光合作用
Abstract: Cyanobacteria are oxygen-evolving photosynthetic prokaryotes that synthesize organic substances from CO2 and other inorganic nutrients. As a unicellular cyanobacterium, Synechococcus elongatus PCC 7942 can be cultured in large scale photobioreactors and easily genetically manipulated. Through systematic deletions of non-essential genes or regions, the genome of this cyanobacterium can be trimmed into a more suitable chassis for synthetic biological studies. The non-essential genes usually include those involved in responses to environmental changes or stresses. Even so, during the process of genome simplification, physiological effects of large fragment deletions should be monitored at each step. ∆Synpcc7942_0233-0253 and ∆Synpcc7942_2169-2187 are two mutants of S. elongatus with an 18 kb or a 14 kb deletion of non-essential genome region, named as Synpcc7942_0233-0253 and Synpcc7942_2169-2187, respectively. PCR examinations indicated that these mutants were completely segregated (no wild type genome copy was found). Comparisons of the two mutants and the wild type under different stressful conditions demonstrated that addition of 0.4 mol/L NaCl significantly inhibited the growth of the two mutants; under normal conditions, however, these 2 mutants showed no or very slight difference from the wild type.Under the salt stress condition, the photosynthetic activities of ∆Synpcc7942_0233-0253 and ∆Synpcc7942_2169-2187 decreased to 41% and 51% of wild type at 96h, respectively; in contrast, the two mutants showed increased respiratory activities. The salt stress reduced electron transfer reactions (ETR) of photosystems (PS) II in the wild type by 52%, in ∆Synpcc7942_0233-0253 by 77% and in ∆Synpcc7942_2169-2187 by 82%. At the same time, the ETR of PS I decreased by 32% in the wild type, by 50% and 47% in the two mutants, respectively. We reported two examples of large genomic fragment deletion mutants with greatly reduced stress tolerance, and the findings provided necessary information for the design of chassis genome of the cyanobacterium and the control of conditions for industrialization in the future. -
蓝藻(蓝细菌)是一类进行放氧光合作用的原核生物, 可利用太阳光能固定CO2, 并利用碳、氮、磷和硫等无机营养合成生命活动所需要的各种有机分子。一些蓝藻种类可进行大规模培养, 并具备遗传操作系统, 适合于合成生物学改造[1]。在合成生物学的研究中, 基因组简化是底盘生物构建的一个重要方面。通过简化基因组删除掉在人工培养条件下不需要的基因, 包括响应环境变化和各类胁迫的复杂系统[2]。蓝藻底盘生物的构建同样需要对基因组开展系统的删除和改造。
目前大肠杆菌、枯草芽孢杆菌和链霉菌等模式生物均有基因组简化的报道。譬如, 有人构建了基因组简化22.2%的大肠杆菌MGF-01, 与野生型菌株相比其生长和苏氨酸产量都有所提高[3]; 还有人构建了基因组简化20.7%的枯草芽孢杆菌MBG874, 其纤维素酶和蛋白激酶的产量较野生型均获得提高[4]。由此可见, 通过适当的基因组简化, 微生物可表现出更好的生产特性, 成为合成生物学理想的底盘细胞。但是也有研究表明, 基因组简化可导致生长速率减缓, 对生长环境的适应能力变弱, 遗传稳定性变差。譬如, 有人通过同源重组和P1噬菌体转导获得基因组简化29.7%的大肠杆菌∆16, 与野生型相比生长减慢, 细胞的长度和宽度发生改变, 胞内核酸定位异常[5]。还有人获得基因组删减达23.5%的枯草芽孢杆菌MG1M, 其生长速率、细胞形态和重组蛋白产量等性状均不稳定[6]。因此, 对基因组不适当的删减也可能对生长、代谢及后续遗传改造产生不利影响。
本实验室利用DNA同源重组和基于RNA介导的DNA剪切筛选对聚球藻PCC 7942基因组开展了系统的删除, 得到了一系列大片段非必需区域删除的突变株。在BG11培养条件下, 这些突变株与野生型在生长上无差异, 但测试不同胁迫条件时发现, 盐度对某些突变株有显著影响。其中将基因组区域Synpcc7942_0233-0253和Synpcc7942_2169-2187分别敲除得到的突变株, 在BG11+0.4 mol/L NaCl培养条件下生长被抑制, 与野生型差异显著。比较聚球藻PCC 7942和这两个突变株在盐胁迫下的光合电子传递链和呼吸活性的差异, 结果显示, 这两个区域很可能存在适应胁迫所需要的基因。然而, 这些区域的删除并不妨碍在非胁迫条件下的生长, 是有利于合成生物学目标实现的。
1. 材料与方法
1.1 藻株和培养条件
聚球藻(Synechococcus elongatus)PCC 7942, 由中国科学院青岛生物能源所吕雪峰实验室提供。野生型与突变株均在30℃、30 μE/(m2·s)连续光照下于BG11中静置或旋转摇动培养(转速为90 r/min), 测试盐胁迫效应时加0.4 mol/L NaCl。通过测定培养物在730 nm的光密度(OD730)来监测藻细胞的生长。生长曲线是3个平行培养的测试结果。
1.2 聚合酶链式反应(PCR)
PCR反应总体积为20 μL, 其中含10 mmol/L Tris-HCl(pH 8.3), 50 mmol/L (NH4)2SO4, 2.5 mmol/L MgCl2, 50 μmol/L dNTPs, 引物各100 pmol(引物序列见表 1), DNA模板50 ng, 1U Taq DNA聚合酶(TaKaRa)。反应先经过94℃预变性6min, 之后为30个循环(94℃ 30s, 58℃ 30s, 72℃ 2min), 最后在72℃再反应7min。
表 1 本研究中所用到的引物Table 1. Primers used in this study引物名称
Primer序列Sequence (5′—3′) 用途
Usage0233-0253-F′ CTCTCGCCAAGAAGTTTTTGGGCA 检测Synpcc 0233—0253
删除0233-0253-R′ TGGGAACTCTGGAAACAGGCCT 0233-0253-2 ATCGACTAACTCCATCTCTCCTAGG 2169-2187-F′ GGTGGCTTGCGGTTCTATGATCG 检测Synpcc 2169—2187
删除2169-2187-R′ ACAGGCCGAAGGTGCAACTCTAG 2169-2187-2 GCCCAGGCTAAATCGACTGTTGCG 1.3 藻细胞扫描吸收光谱
取适量野生型和突变株藻液, 在4000 r/min离心3min收集后重悬于新鲜培养液, 调整OD730到相同水平, 再用UV-1601分光光度计(Shimadzu)在400—800 nm波长范围内扫描测定吸收光谱。分别用BG11和添加0.4 mol/L NaCl的BG11培养基作空白对照, 比色皿的毛玻璃面朝向光源。
1.4 聚球藻PCC 7942总膜的制备
根据文献[7]所述方法制备聚球藻PCC 7942的总膜。离心收集50 mL藻液, 重悬于1 mL的磷酸钾缓冲液(20 mmol/L, pH 7.8)。再加入适量的直径为0.17 mm左右的玻璃珠(Sigma), 在漩涡振荡器振荡1min, 然后置于冰上1min, 重复此步骤5次。先后在4000 r/min、6000 r/min 离心10min, 收集上清, 再以35000 r/min超速离心收集总膜, 重悬于2 mL 10 mmol/L NaHCO3(pH 7.0)溶液。
1.5 光合放氧、呼吸耗氧速率的测定
按Gao和Xu描述的方法[7], 具体操作如下: 离心收集2 mL藻细胞(A730=0.5), 重悬于含10 mmol/L NaHCO3的25 mmol/L HEPES(pH 7.0), 先在黑暗条件下用Oxy-Lab氧电极(Hansatech)在30℃条件下测定藻细胞的呼吸耗氧速率, 每个样品测定时间为5min左右; 打开光源, 光强800 μmol/(m2·s), 测定藻细胞的放氧速率。
利用全细胞测量PSII电子传递链的活性, 在细胞悬浮液中加入1 mmol/L K3Fe(CN)6和0.5 μmol/L DCBQ(2,6-dichloro-p-benzoquinone), 测定放氧速率。利用总膜测定PSI电子传递链活性, 在2 mL总膜悬浮液中加入10 μmol/L DCMU[3-(3,4-dichlorophenyl)-l, l-dimethyl urea], 1 mmol/L 抗坏血酸钠, l mmol/L MV(methyl viologen)和l μmol/L DCPIP(2,6-dichlorophenol-indophenol), 测定耗氧速率。
光合放氧速率/呼吸耗氧速率 [μmol O2/(mg Chl.a)∙h]=(斜率×60000)/(13.34×A664)。式中, 13.34×A664为叶绿素a含量, 是叶绿素的甲醇提取液在664 nm处的光吸收值。
2. 结果
2.1 突变株的检测验证
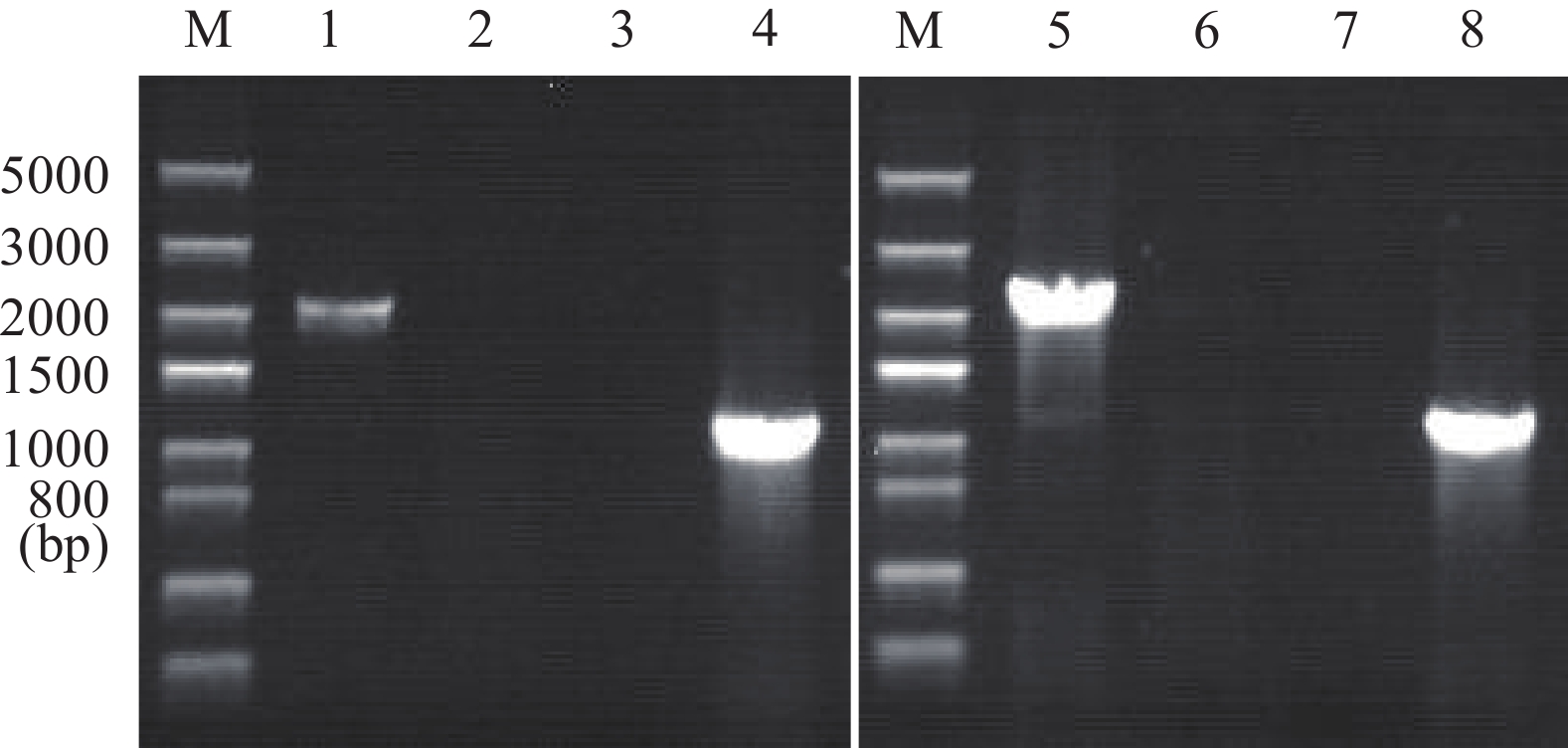
∆Synpcc7942_0233-0253和∆Synpcc7942_2169-2187是基因组非必需区域Synpcc7942_0233-0253(18 kb)和Synpcc7942_2169-2187(14 kb)分别被删除的聚球藻PCC 7942突变株(基因组系统删除和简化过程将另文发表)。由于蓝藻基因组在细胞中存在多拷贝, 我们利用PCR检测确认突变株中是否仍残留部分野生型。如图 1所示, 引物对0233-0253-F′/R′在基因组中相距20.0 kb, 2169-2187-F′/R′相距16.2 kb, 均位于删除区域之外, 而0233-0253-2和2169-2187-2位于删除区域内。对野生型和突变株进行检测, 结果如图 2所示。以引物0233-0253-F′/R′或2169-2187- F′/R′进行PCR检测, 突变株可扩增出约2.1 kb的条带, 说明已删除该区域。以普通PCR检测并不能检测出野生型的20 或16.2 kb条带, 所以我们还用引物0233-0253-F′/2和2169-2187- F′/2进行PCR, 如果扩增出1.1或者1.2 kb的条带, 则说明存在野生型拷贝, 但是扩增结果证明并没有野生型拷贝, 说明突变株确实是完全分离的。
![]() 图 1 两个缺失突变检测引物在基因组上位置的示意图在这2个基因组区域中, Synpcc7942_0242预测为Na+/Ca2+交换转运蛋白基因, Synpcc7942_2186预测为Na+/H+交换转运蛋白基因Figure 1. Schematic diagrams showing genomic positions of the primers for detection of deletionsIn these two genomic regions, Synpcc7942_0242 is predicted to be a Na+/Ca2+ exchanger gene, while Synpcc7942_2186 is a Na+/H+ exchanger gene
图 1 两个缺失突变检测引物在基因组上位置的示意图在这2个基因组区域中, Synpcc7942_0242预测为Na+/Ca2+交换转运蛋白基因, Synpcc7942_2186预测为Na+/H+交换转运蛋白基因Figure 1. Schematic diagrams showing genomic positions of the primers for detection of deletionsIn these two genomic regions, Synpcc7942_0242 is predicted to be a Na+/Ca2+ exchanger gene, while Synpcc7942_2186 is a Na+/H+ exchanger gene![]() 图 2 两个突变株的PCR检测结果1和2. 引物0233-0253-F′/R′; 3和4. 引物0233-0253-F′/2; 1和3. 突变株∆Synpcc7942_0233-0253; 2和4. 野生型(wt); 5和6. 引物2169-2187-F′/R′; 7和8. 引物2169-2187-F′/2; 5和7. 突变株∆Synpcc7942_2169-2187; 6和8. 野生型; M. DNA标记Figure 2. PCR examination of 2 mutants1, 2. primers 0233-0253-F′/R′; 3, 4. primers 0233-0253-F′/2; 1, 3. ∆Synpcc7942_0233-0253; 2, 4. wild type (wt); 5, 6. primers 2169-2187-F′/R′; 7, 8. primers 2169-2187-F′/2; 5, 7. ∆Synpcc7942_2169-2187; 6, 8. wild type; M. DNA markers
图 2 两个突变株的PCR检测结果1和2. 引物0233-0253-F′/R′; 3和4. 引物0233-0253-F′/2; 1和3. 突变株∆Synpcc7942_0233-0253; 2和4. 野生型(wt); 5和6. 引物2169-2187-F′/R′; 7和8. 引物2169-2187-F′/2; 5和7. 突变株∆Synpcc7942_2169-2187; 6和8. 野生型; M. DNA标记Figure 2. PCR examination of 2 mutants1, 2. primers 0233-0253-F′/R′; 3, 4. primers 0233-0253-F′/2; 1, 3. ∆Synpcc7942_0233-0253; 2, 4. wild type (wt); 5, 6. primers 2169-2187-F′/R′; 7, 8. primers 2169-2187-F′/2; 5, 7. ∆Synpcc7942_2169-2187; 6, 8. wild type; M. DNA markers2.2 盐胁迫下生长的差异
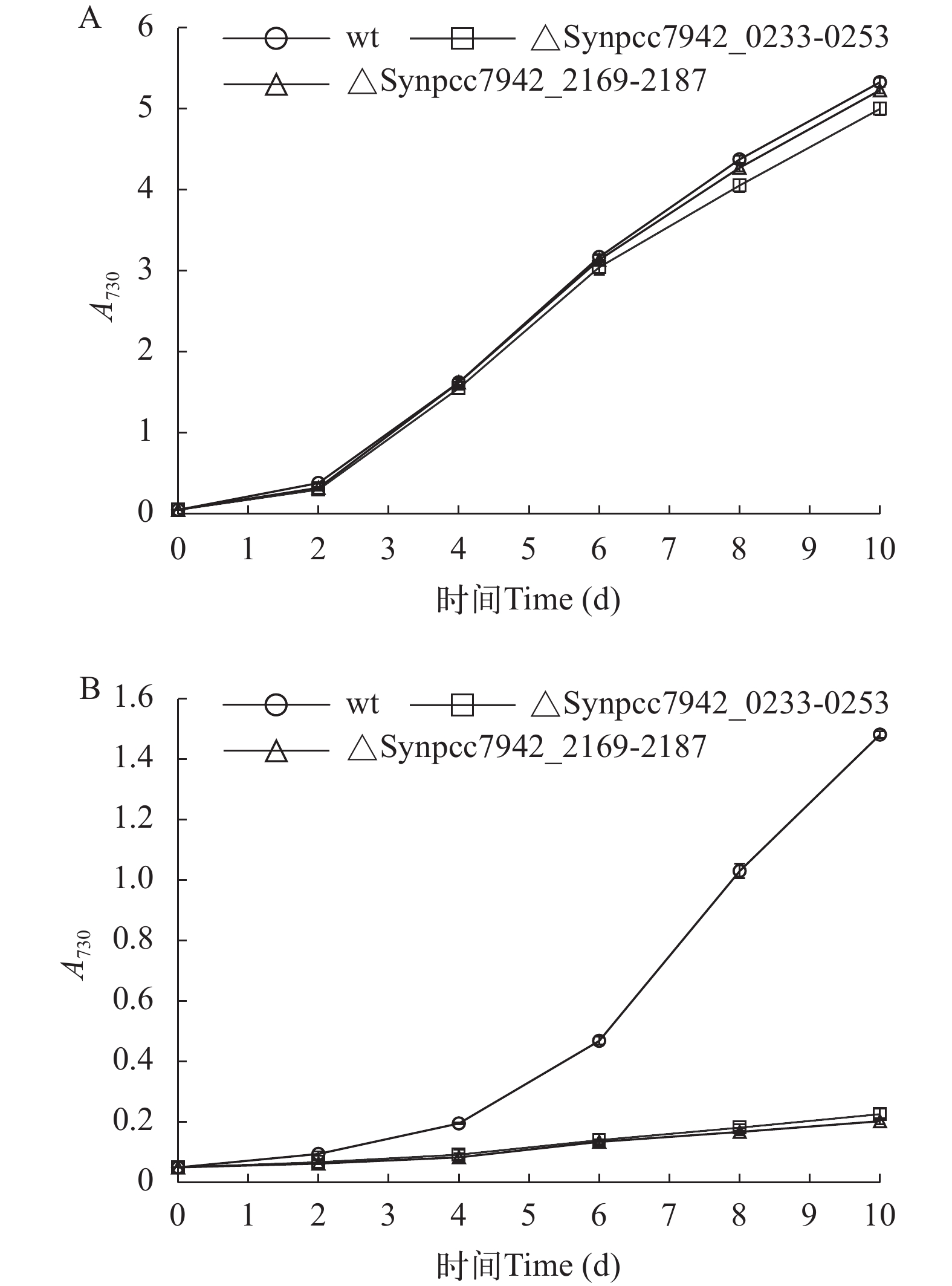
比较突变株ΔSynpcc7942_0233-0253、ΔSynpcc7942_2169-2187与野生型在不同条件下的生长, 发现在BG11中没有显著差异或仅有微小差异(图 3A), 但在BG11+0.4 mol/L NaCl中, 突变株的生长相对于野生型被严重抑制了(图 3B)。
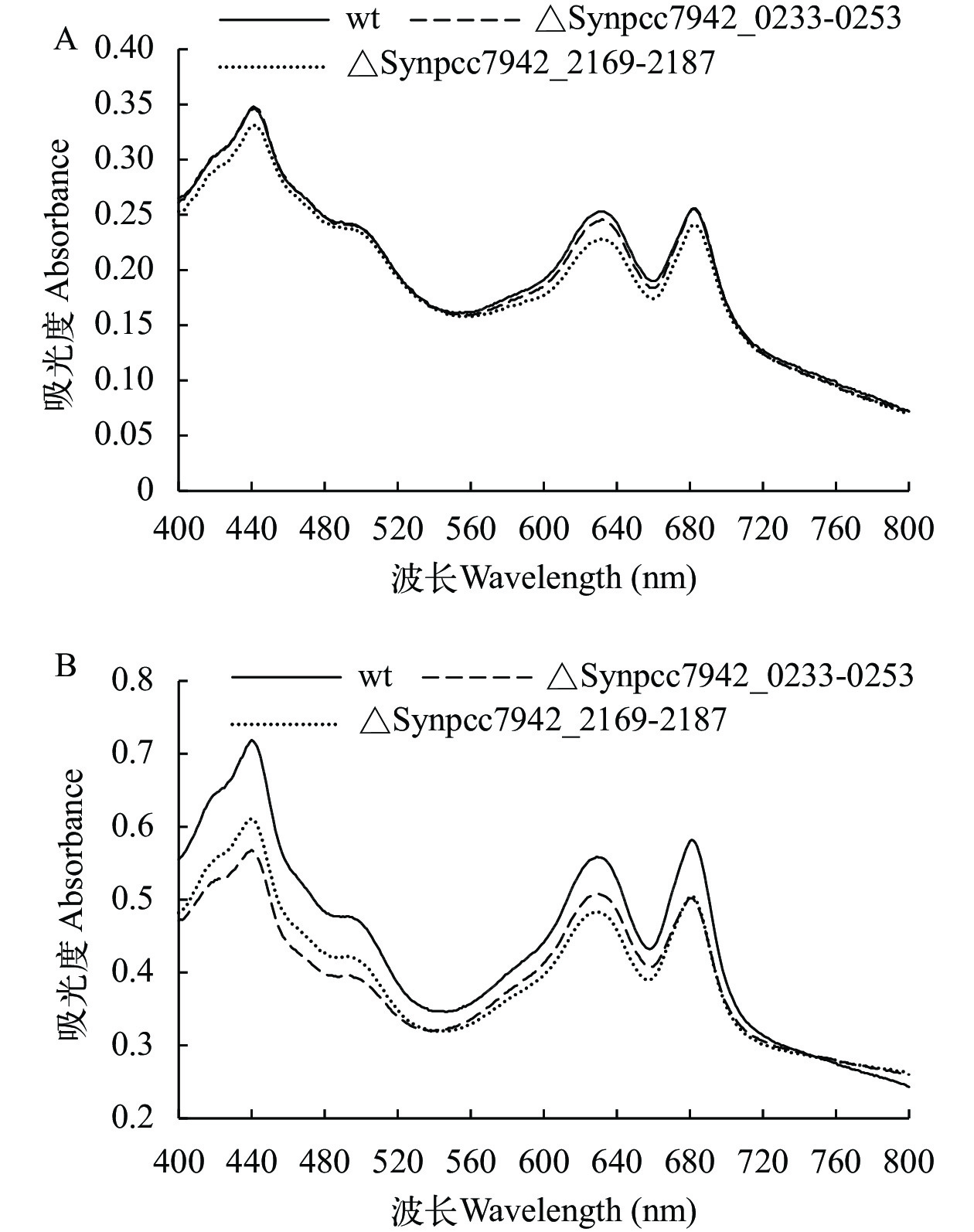
在0和96h两个时间点扫描藻细胞吸收光谱, 将各样品在730 nm处调成一致(调整浊度使生物量一致), 结果显示: 在0时突变株与野生型差异较小(图 4A), 而在盐胁迫96h后, 突变株的叶绿素(440和680 nm)、藻胆素(630 nm)、类胡萝卜素(480—490 nm肩峰)吸收峰均明显低于野生型(图 4B)。
2.3 光合电子传递和呼吸活性的分析
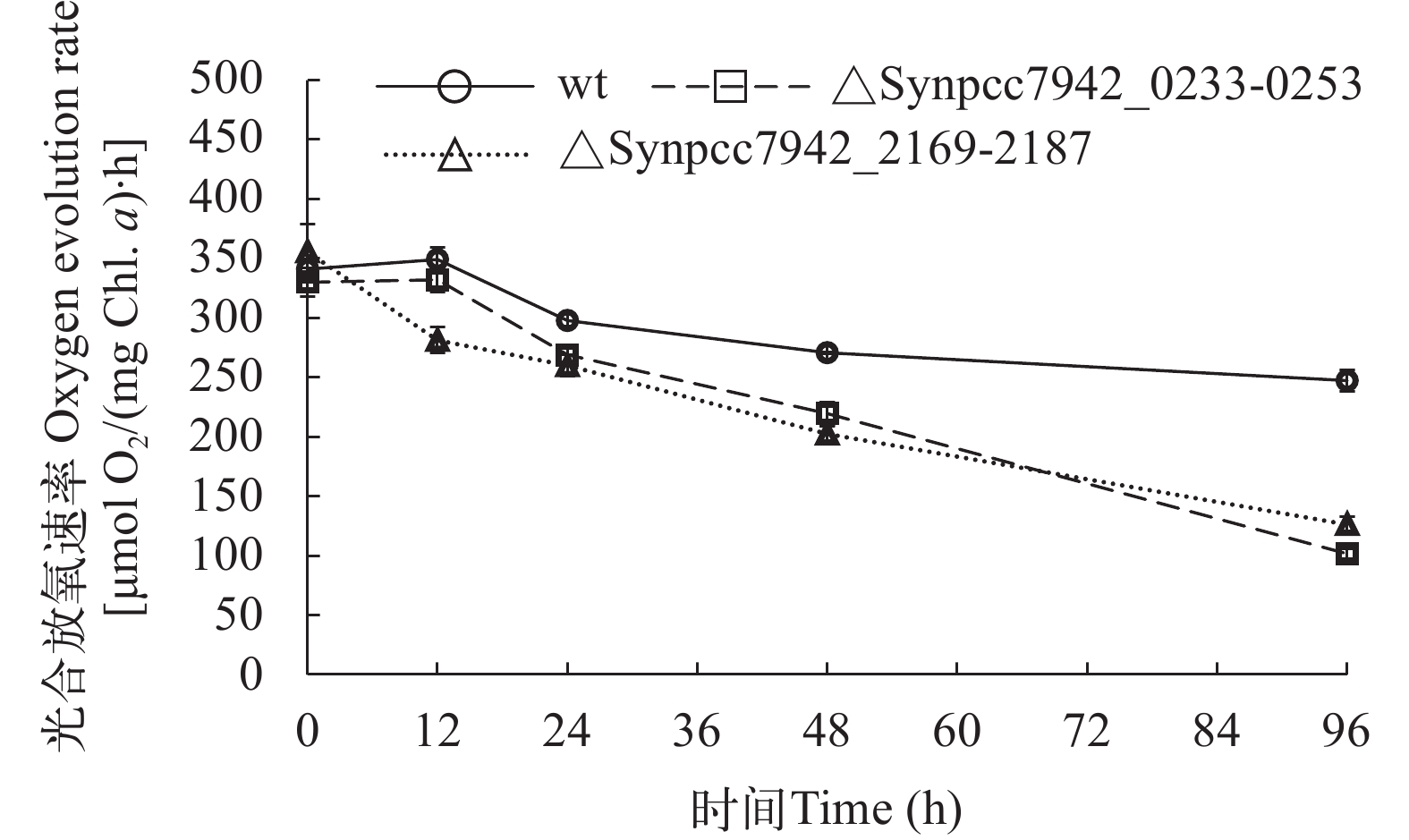
进一步检测盐胁迫对突变株光合放氧速率的影响, 结果发现野生型和突变株总体都呈下降趋势, 但2个突变株下降得更快, 96h后分别是野生型的41%和51%(图 5)。
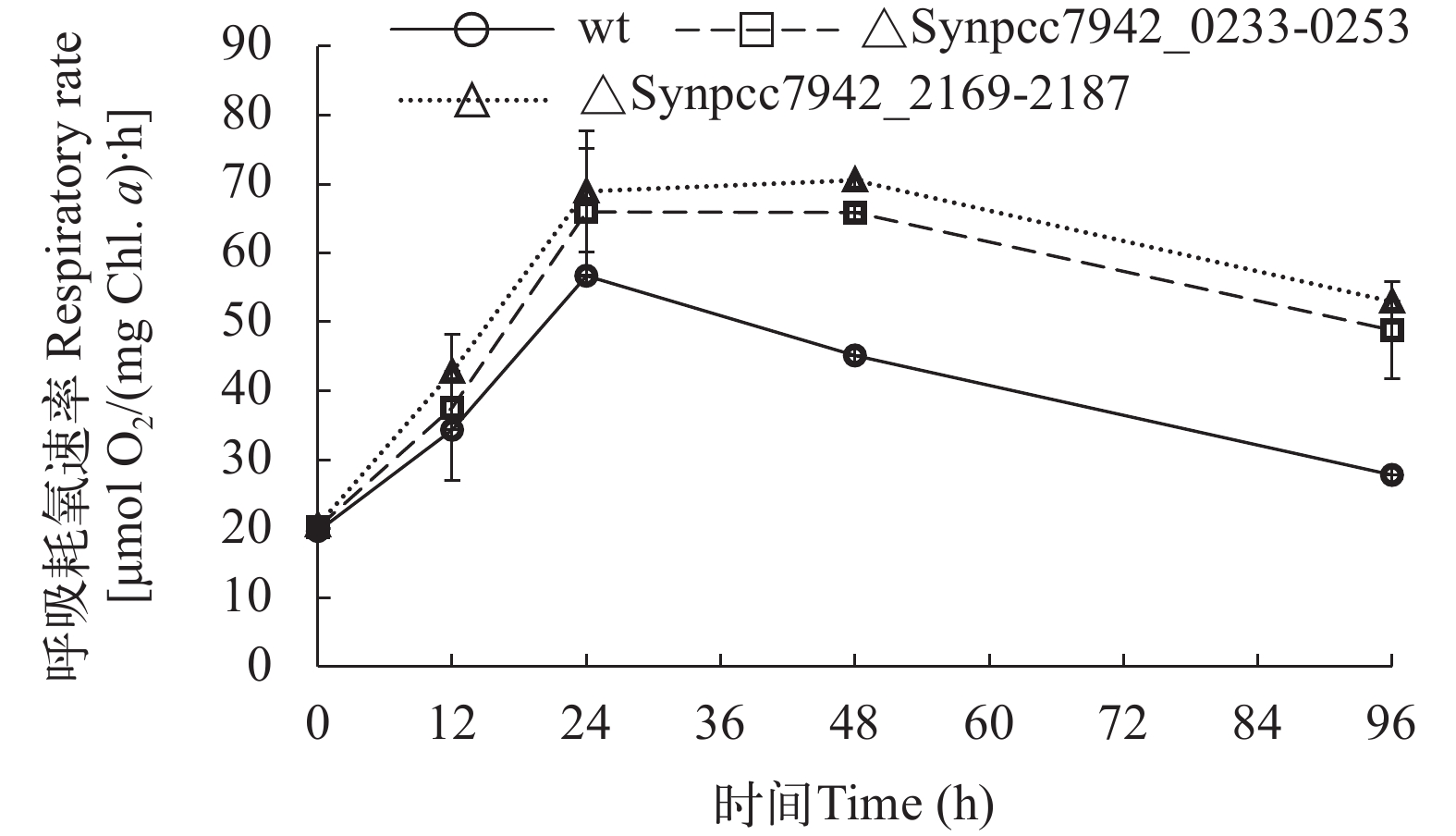
同时测定突变株与野生型的呼吸速率, 发现在24h内呼吸耗氧都明显升高, 随后野生型逐步降低, 而突变株在48h后降低, 至96h仍维持较高水平(图 6)。
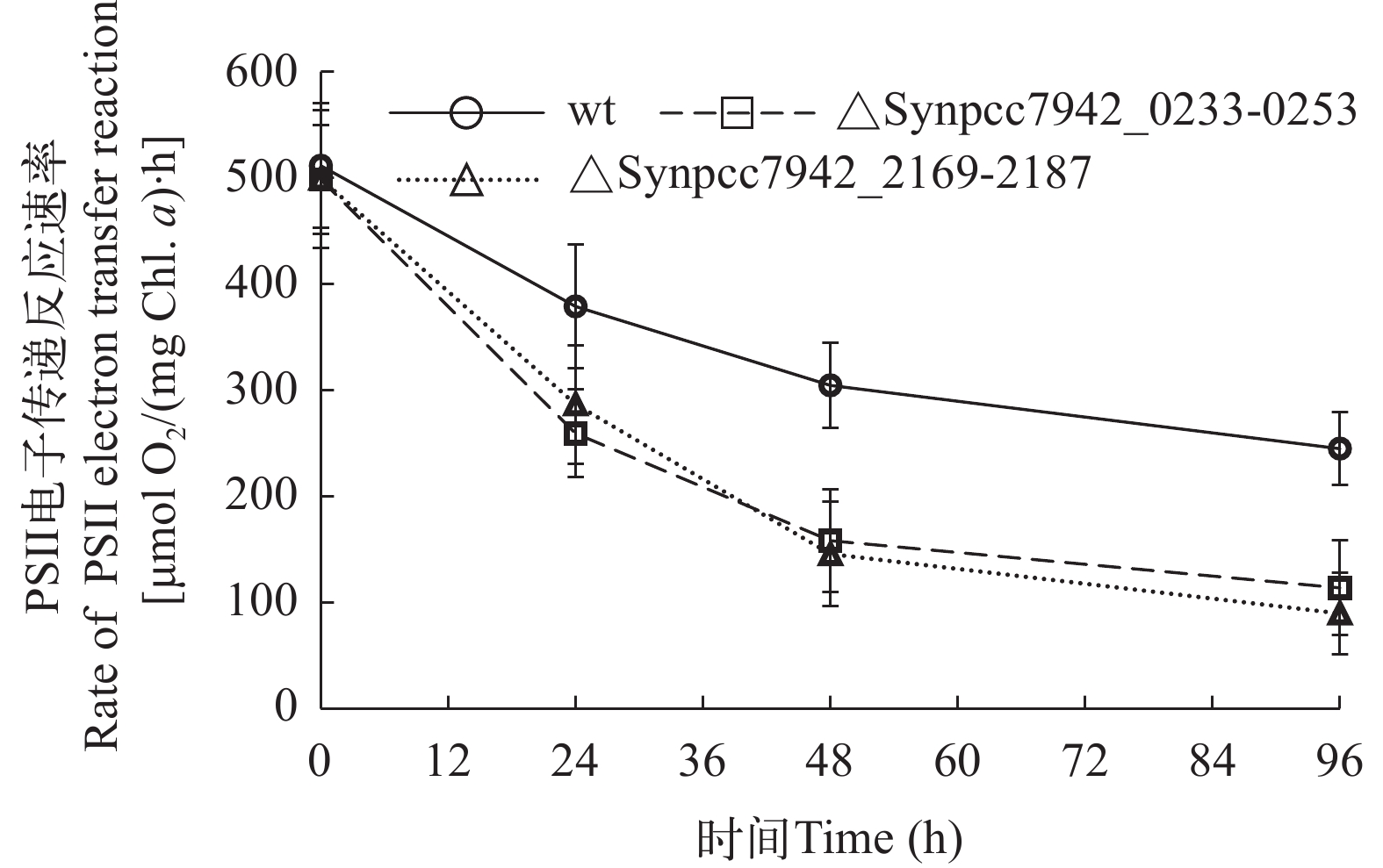
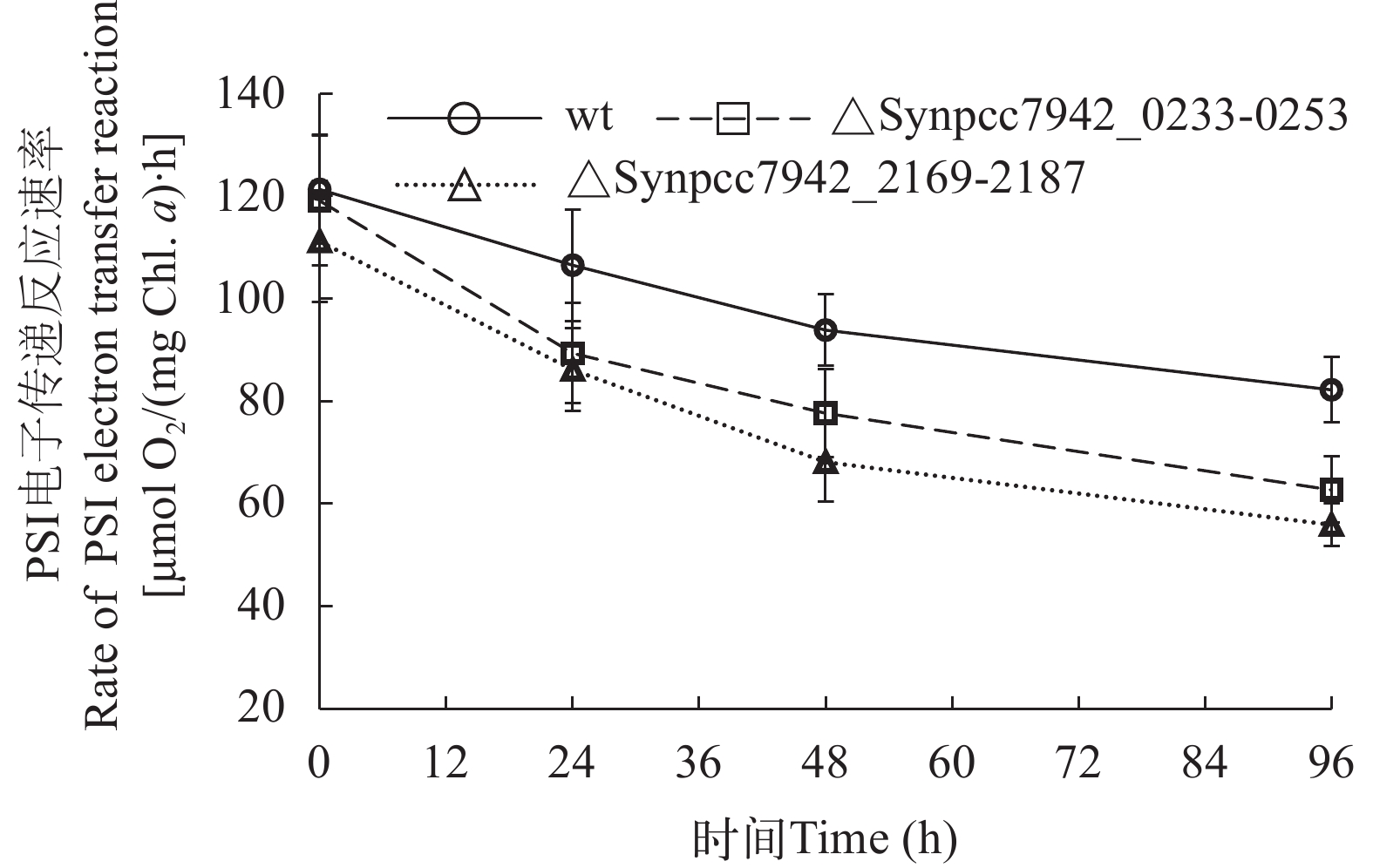
为进一步阐释盐胁迫对光合活性的影响, 本研究测量了光系统(PS)Ⅰ和Ⅱ的电子传递速率。在盐胁迫96h后, 野生型PSⅡ电子传递反应速率下降了52%, 而∆Synpcc7942_0233-0253和∆Synpcc7942_2169-2187分别下降了77%和82%(图 7); 野生型PSⅠ电子传递速率下降了32%, 而∆Synpcc7942_0233-0253和∆Synpcc7942_2169-2187分别下降了50%和47%(图 8)。
3. 讨论
聚球藻PCC 7942有望发展成为燃料与高价值化学品的生产平台[8], 其基因组中的必需基因与非必需基因已有系统的鉴定[9]。针对非必需基因区域开展基因组简化可以使其遗传背景简单化, 提升合成生物学操作的可预测性和可控制性。本实验室对其大片段非必需区域开展系统删除, 并在不同温度、光强和盐胁迫等条件下检查突变株适应能力的变化, 发现少数区域的删除导致耐盐胁迫能力的降低。
盐胁迫是最常见的非生物胁迫之一, 通过离子胁迫和渗透胁迫改变代谢过程和光合作用[10]。此外, 盐胁迫会增加细胞内活性氧(ROS)的含量[11]。在盐胁迫下细胞产生的ROS抑制转录因子活性[12], 抑制D1蛋白以及其他光系统相关蛋白的合成, 甚至破坏类囊体膜结构, 使光合作用受阻[13]。聚球藻PCC 7942维持稳定生长能耐受NaCl的最高浓度约为0.4 mol/L[14], 而在此浓度的NaCl胁迫下, Synpcc7942_0233-0253和Synpcc7942_2169-2187区域删除突变株的生长被严重抑制。整细胞扫描吸收光谱还显示, 突变株在盐胁迫下各种色素吸收峰比野生型降低, 可能与光合复合体、藻胆体等结构的破坏有关。在盐胁迫下, 2个突变株的光合放氧活性均比野生型下降得更快; 进一步测定野生型和突变株PSⅡ和PSⅠ的电子传递速率, 观察到突变株的PSⅡ和PSⅠ都受到更显著的损害, 尤以PSⅡ更加敏感。实际上, 在更高浓度的NaCl胁迫下(0.5 mol/L), 聚球藻的PSⅡ和PSⅠ均失活[15], 这与本研究观察到的情况相映证。与光合作用相反, 在盐胁迫下突变株的呼吸活性比野生型维持在更高水平。这种情况尚未在文献中有类似报道, 值得进一步研究。光合作用活性比野生型降低, 而呼吸活性比野生型高, 两相叠加导致突变株在盐胁迫下合成少、消耗多, 生长受到严重抑制。
聚球藻PCC 7942耐受NaCl胁迫主要依赖于蔗糖合成和Na+泵出维持胞内渗透压平衡。蔗糖的合成涉及基因Synpcc7942_0808, 其产物具有蔗糖磷酸合成酶(SPS)和蔗糖磷酸酶(SPP)结构域[16]。Na+的泵出主要是借助于Na+/H+反向转运蛋白(Antiporter)和Na+/K+反向转运蛋白[17], 其中涉及编码Na+/H+泵的有6个基因, 即napA、nha4、nha1、nha2、nha3和nha6。在突变株∆Synpcc7942_0233-0253和∆Synpcc7942_2169-2187缺失的区域中并没有这些基因, 但有预测编码Na+/Ca2+交换转运蛋白的基因Synpcc7942_0242, 还有预测为Na+/H+交换转运蛋白的基因nha7(Synpcc7942_2186)[18, 19]。这些基因是否参与耐盐生理效应, 有待实验证据支持。
基因组简化既可能提高合成生物学底盘生物的生理和生产性状, 也可能带来某些不利影响。因此, 在蓝藻基因组简化的过程中需要保持对生长特性、生理适应性和遗传稳定性的监测。本研究报道了两个非必需基因区域的删除导致耐盐能力降低, 但并不妨碍在非胁迫条件下的生长。这些信息的掌握对于底盘生物基因组的设计和未来生产条件的控制都是需要的。
-
图 1 两个缺失突变检测引物在基因组上位置的示意图
在这2个基因组区域中, Synpcc7942_0242预测为Na+/Ca2+交换转运蛋白基因, Synpcc7942_2186预测为Na+/H+交换转运蛋白基因
Figure 1. Schematic diagrams showing genomic positions of the primers for detection of deletions
In these two genomic regions, Synpcc7942_0242 is predicted to be a Na+/Ca2+ exchanger gene, while Synpcc7942_2186 is a Na+/H+ exchanger gene
图 2 两个突变株的PCR检测结果
1和2. 引物0233-0253-F′/R′; 3和4. 引物0233-0253-F′/2; 1和3. 突变株∆Synpcc7942_0233-0253; 2和4. 野生型(wt); 5和6. 引物2169-2187-F′/R′; 7和8. 引物2169-2187-F′/2; 5和7. 突变株∆Synpcc7942_2169-2187; 6和8. 野生型; M. DNA标记
Figure 2. PCR examination of 2 mutants
1, 2. primers 0233-0253-F′/R′; 3, 4. primers 0233-0253-F′/2; 1, 3. ∆Synpcc7942_0233-0253; 2, 4. wild type (wt); 5, 6. primers 2169-2187-F′/R′; 7, 8. primers 2169-2187-F′/2; 5, 7. ∆Synpcc7942_2169-2187; 6, 8. wild type; M. DNA markers
表 1 本研究中所用到的引物
Table 1 Primers used in this study
引物名称
Primer序列Sequence (5′—3′) 用途
Usage0233-0253-F′ CTCTCGCCAAGAAGTTTTTGGGCA 检测Synpcc 0233—0253
删除0233-0253-R′ TGGGAACTCTGGAAACAGGCCT 0233-0253-2 ATCGACTAACTCCATCTCTCCTAGG 2169-2187-F′ GGTGGCTTGCGGTTCTATGATCG 检测Synpcc 2169—2187
删除2169-2187-R′ ACAGGCCGAAGGTGCAACTCTAG 2169-2187-2 GCCCAGGCTAAATCGACTGTTGCG -
[1] Heidorn T, Camsund D, Huang H, et al. Synthetic biology in cyanobacteria: engineering and analyzing novel functions [J]. Methods in Enzymology, 2011(497): 539-579.
[2] Acevedo-Rocha C G, Fang G, Schmidt M, et al. From essential to persistent genes: a functional approach to constructing synthetic life [J]. Trends in Genetics, 2013, 29(5): 273-279. doi: 10.1016/j.tig.2012.11.001
[3] Mizoguchi H, Mori H, Fujio T, et al. Escherichia coli minimum genome factory [J]. Biotechnology and Applied Biochemistry, 2007, 46(3): 157-167. doi: 10.1042/BA20060107
[4] Morimoto T, Kadoya R, Endo K, et al. Enhanced recombinant protein productivity by genome reduction in Bacillus subtilis [J]. DNA Research, 2008, 15(2): 73-81. doi: 10.1093/dnares/dsn002
[5] Hashimoto M, Ichimura T, Mizoguchi H, et al. Cell size and nucleoid organization of engineered Escherichia coli cells with a reduced genome [J]. Molecular Microbiology, 2005, 55(1): 137-149.
[6] Ara K, Ozaki K, Nakamura K, et al. Bacillus minimum genome factory: effective utilization of microbial genome information [J]. Biotechnology and Applied Biochemistry, 2007, 46(3): 169-178. doi: 10.1042/BA20060111
[7] Gao H, Xu X. Depletion of Vipp1 in Synechocystis sp. PCC 6803 affects photosynthetic activity before the loss of thylakoid membranes [J]. FEMS Microbiology Letters, 2009, 292(1): 63-70. doi: 10.1111/j.1574-6968.2008.01470.x
[8] Angermayr S A, Gorchs Rovira A, Hellingwerf K J. Metabolic engineering of cyanobacteria for the synthesis of commodity products [J]. Trends in Biotechnology, 2015, 33(6): 352-361. doi: 10.1016/j.tibtech.2015.03.009
[9] Rubin B E, Wetmore K M, Price M N, et al. The essential gene set of a photosynthetic organism [J]. Proceedings of the National Academy of Sciences of the United States of America, 2015, 112(48): E6634-E6643. doi: 10.1073/pnas.1519220112
[10] Allakhverdiev S I, Murata N. Salt stress inhibits photosystems Ⅱ and I in cyanobacteria [J]. Photosynthesis Research, 2008, 98(1): 529-539.
[11] Yang W J, Wang F, Liu L N, et al. Responses of membranes and the photosynthetic apparatus to salt stress in cyanobacteria [J]. Front Plant Science, 2020(11): 1-10.
[12] Jimbo H, Yutthanasirikul R, Nagano T, et al. Oxidation of translation factor EF-Tu inhibits the repair of photosystem Ⅱ [J]. Plant Physiology, 2018, 176(4): 2691-2699. doi: 10.1104/pp.18.00037
[13] Gill S S, Tuteja N. Reactive oxygen species and antioxidant machinery in abiotic stress tolerance in crop plants [J]. Plant Physiology and Biochemistry, 2010, 48(12): 909-930. doi: 10.1016/j.plaphy.2010.08.016
[14] Sudhir P, Murthy S P S. Effects of salt stress on basic processes of photosynthesis [J]. Photosynthetica, 2004, 42(2): 481-486.
[15] Allakhverdiev S I, Sakamoto A, Nishiyama Y, et al. Inactivation of photosystems I and Ⅱ in response to osmotic stress in Synechococcus. Contribution of water channels [J]. Plant Physiology, 2000, 122(4): 1201-1208. doi: 10.1104/pp.122.4.1201
[16] Liang Y, Zhang M, Wang M, et al. Freshwater cyanobacterium Synechococcus elongatus PCC 7942 adapts to an environment with salt stress via ion-induced enzymatic balance of compatible solutes [J]. Applied and Environmental Microbiology, 2020, 86(7): 1-14.
[17] Waditee R, Hibino T, Nakamura T, et al. Overexpression of a Na+/H+ antiporter confers salt tolerance on a freshwater cyanobacterium, making it capable of growth in sea water [J]. Proceedings of the National Academy of Sciences of the United States of America, 2002, 99(6): 4109-4114. doi: 10.1073/pnas.052576899
[18] Leganes F, Forchhammer K, Fernandezpinas F, et al. Role of calcium in acclimation of the cyanobacterium Synechococcus elongatus PCC 7942 to nitrogen starvation [J]. Microbiology, 2009, 155(1): 25-34. doi: 10.1099/mic.0.022251-0
[19] Yamaguchi T, Aharon G S, Sottosanto J B, et al. Vacuolar Na+/H+ antiporter cation selectivity is regulated by calmodulin from within the vacuole in a Ca2+- and pH-dependent manner [J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(44): 16107-16112. doi: 10.1073/pnas.0504437102



 下载:
下载: