EFFECTS OF TEMPERATURES AND MICROCYSTIS AERUGINOSA TOXICITY ON LIFE-TABLE PARAMETERS OF BRACHIONUS CALYCIFLORUS
-
摘要: 文章开展了25℃下两个品系铜绿微囊藻(有毒与无毒)不同浓度对萼花臂尾轮虫生活史的影响研究, 及在5个温度下不同浓度有毒铜绿微囊藻对萼花臂尾轮虫生活史影响的研究。结果表明铜绿微囊藻毒性、浓度及二者交互作用对轮虫生活史参数净生殖率(R0; F=31.83, P<0.01; F=30.36, P<0.01; F=13.51, P<0.01)、内禀增长率(rm; F=34.67, P<0.01; F=18.73, P<0.01; F=12.99, P<0.01)均有显著影响; 温度、铜绿微囊藻浓度及二者交互作用对轮虫生活史参数净生殖率、内禀增长率也均有显著影响。无毒铜绿微藻在低浓度(1×104 cells/mL)下对轮虫种群有促进作用, 可作为轮虫食物来源, 但缺乏脂肪酸等营养物质, 食物质量比蛋白核小球藻低; 在高浓度(1×105和5×105 cells/mL)下轮虫摄食无毒铜绿微囊藻机率变大, 整体食物品质下降, 对轮虫有抑制作用。有毒铜绿微囊藻对轮虫种群的抑制作用更加明显, 微囊藻浓度升高, 净生殖率和内禀增长率显著下降。研究结果还表明30℃和35℃高温下轮虫生长繁殖变快, 世代时间缩短。在高温(30℃和35℃)环境下, 铜绿微囊藻浓度升高对轮虫抑制作用更加明显。Abstract: To investigate the effects of two strains of Microcystis aeruginosa (microcystin-producing and microcystin-free) at different concentrations on the life table parameters of Brachionus calyciflorus, we conducted a life-table study at 25℃ and investigated the responses of life table parameters of B. calyciflorus to microcystin-producing M. aeruginosa concentrations at five temperature gradients. The results showed that both M. aeruginosa toxicity and concentration significantly mediated the net reproduction rate (R0; F=31.83, P<0.01; F=30.36, P<0.01) and intrinsic growth rate (rm; F=34.67, P<0.01; F=18.73, P<0.01) of B. calyciflorus with a significant interactive effect, and that temperature and microcystin-producing M. aeruginosa concentration had significant independent and interactive effects on the net reproduction rate (R0; F=13.51, P<0.01) and intrinsic growth rate (rm; F=12.99, P<0.01) of B. calyciflorus. Microcystin-free M. aeruginosa promoted the rotifer population and it could be used as a food source for rotifers at low concentration (1×104 cells/mL), but its food quality was low due to the lack of fatty acids and other nutrients. High concentration of Microcystin-free M. aeruginosa (1×105 cells/mL and 5×105 cells/mL) obviously inhibited the growth of rotifers because rotifers prefer microcystin-free M. aeruginosa. The net reproductive rate and intrinsic growth rate of B. calyciflorus increased significantly by increasing concentration of microcystin-producing M. aeruginosa. Moreover, high temperature (30℃ and 35℃) accelerated their reproduction and growth rate, shorten the generation time, and promoted inhibitory effect of microcystin-free M. aeruginosa on rotifers.
-
Keywords:
- Microcystis aeruginosa /
- Brachionus calyciflorus /
- Temperature /
- Life table parameters /
- Interaction
-
在水生态系统中, 浮游动物起着承上启下的枢纽作用[1]。轮虫是浮游动物的一大类群, 其丰度和群落组成是反应水质的一个重要指标[2]。萼花臂尾轮虫(Brachionus calyciflorus)是鱼类开口饵料, 也是浮游植物的牧食者[3], 因繁殖快、世代周期短、易培养等特点被作为生态毒理学研究的受试动物[4]。在自然环境中萼花臂尾轮虫种群数量庞大, 其种群动态受多种生物因子(如捕食、竞争、食物)和非生物因子(如光照、温度、pH等)的影响, 其中食物种类、浓度、质量以及培养温度是影响轮虫生长繁殖及其种群动态重要的生态因子。关于食物种类和浓度对轮虫生长繁殖的影响已有大量的研究[5, 6], 而食物质量对轮虫生长繁殖的影响研究相对较少, 且研究结果N和P限制对萼花臂尾轮虫的影响具有争议[7, 8]。
在蓝藻水华发生时, 浮游植物群落中95%是由微囊藻组成, 结果导致浮游动物群落丰度大量减少[9]。铜绿微囊藻(Microcystis aeruginosa)是最为常见的水华蓝藻[10], 有毒和无毒铜绿微囊藻共存于自然水体。大量的研究表明有毒微囊藻产生的内源性毒素可引起鱼类和无脊椎动物中毒死亡[11]。轮虫作为滤食性的浮游生物, 微囊藻也是其食物源之一, Rothhaupt[10]发现红臂尾轮虫(Brachionus rubens)摄取食物质量低的有毒铜绿微囊藻时, 轮虫种群存活率降低。Zhao等[12]和Huang等[13]的研究表明有毒微囊藻对轮虫的生长影响是不利的。但是目前已有研究却未能区分微囊藻对轮虫种群的影响是毒性还是食物质量。因此, 本研究的目的之一是探讨微囊藻毒性和食物质量对萼花臂尾轮虫的影响。
水体温度直接影响生物有机体的体温, 体温的高低又决定了浮游动物新陈代谢、生长、发育、繁殖和行为等, 从而影响浮游动物的丰度[14, 15]。尽管大量的研究表明温度对轮虫的个体大小、生长以及生活史特征有显著的影响[16, 17], 但是很少有研究关注温度与其他因子(例如食物质量、产毒蓝藻)的交互作用对轮虫生长繁殖影响。且少有的关于温度和食物浓度对轮虫种群增长及繁殖的研究结果存在不一致性[18, 19]。为了分析不同温度下铜绿微囊藻对萼花臂尾轮虫的影响, 我们研究了有毒铜绿微囊藻浓度、温度以及两者交互作用对轮虫的影响。旨在丰富浮游动物与蓝藻关系, 为以后的研究提供基础数据。
1. 材料与方法
1.1 轮虫的来源及培养
实验选取的萼花臂尾轮虫采自湖北省武汉市南湖水体, 在实验室培养半年以上。轮虫置于(25±1)℃光照培养箱100 mL烧杯中培养, 光照强度为2200 lx, 光照周期为12L: 12D。培养轮虫所用培养基为EPA培养基(NaHCO3 96 mg/L; CaSO4 60 mg/L; MgSO4 60 mg/L; KCl 4 mg/L)[20]。
1.2 藻种来源及培养
轮虫培养食物为蛋白核小球藻(Chlorella pyrenoidosa), 有毒铜绿微囊藻(Microcystin-producing M. aeruginosa FACHB905)和无毒铜绿微囊藻(Microcystin-free M. aeruginosa FACHB526), 均由中国科学院水生生物研究所藻种库提供。藻类培养条件为于(25±1)℃光照培养箱250 mL锥形瓶中进行培养, 光照强度为2500 lx, 周期为18L: 6D。藻类所用培养基为BG11[21], 121℃高压灭菌20min后冷却至室温, 在无菌环境下接种。取对数生长期的绿藻和蓝藻进行离心(7000 r/min, 10min), 浓缩富集后放置于4℃冰箱中备用。实验前, 在显微镜下计数浓缩过的绿藻和蓝藻, 并用EPA培养基稀释到实验所需浓度。
1.3 实验设计
本研究首先探讨在相同实验条件下, 两种不同品系的铜绿微囊藻(有毒和无毒)对萼花臂尾轮虫生活史的影响; 随后开展不同温度和不同浓度的有毒铜绿微囊藻对萼花臂尾轮虫生活史的影响。总有机碳总氮分析仪(Multi N/C 3100)测藻类碳含量, 结果如下: 蛋白核小球藻: 0.9×10–8 mg/cell; 无毒铜绿微囊藻: 0.545×10–8 mg/cell; 有毒铜绿微囊藻: 0.98×10–8 mg/cell。
实验一: 研究两个品系铜绿微囊藻(有毒与无毒)在不同浓度下对萼花臂尾轮虫生活史的影响, 在25℃温度下, 分别用100%无毒铜绿微囊藻+100%蛋白核小球藻(对照组碳含量为4.50 μg C/mL, 处理组1碳含量为4.55 μg C/mL, 处理组2碳含量为4.77 μg C/mL, 处理组3碳含量为5.05 μg C/mL, 处理组4碳含量为7.23 μg C/mL)和100%有毒铜绿微囊藻+100%蛋白核小球藻(对照组碳含量为4.50 μg C/mL, 处理组1碳含量为4.60 μg C/mL, 处理组2碳含量为4.99 μg C/mL, 处理组3碳含量为5.48 μg C/mL, 处理组4碳含量为9.40 μg C/mL)的组合作为食物, 其中蛋白核小球藻浓度为5×105 cells/mL(碳含量为4.50 μg C/mL), 铜绿微囊藻浓度有5个梯度, 共10组, 如表 1所示, 以萼花臂尾轮虫作为受试生物进行生命表实验。
表 1 实验一中不同处理组食物情况(浓度单位cells/mL)Table 1. Food concentration of different treatments in experiment 1 (cells/mL)组别Group 无毒铜绿微囊藻+蛋白核小球藻Microcystin-free M. aeruginosa+C. pyrenoidosa 有毒铜绿微囊藻+蛋白核小球藻Microcystin- producing M. aeruginosa+C. pyrenoidosa 对照组Control group 0+5×105 0+5×105 处理组1
Treatment group 11×104+5×105 1×104+5×105 处理组2
Treatment group 25×104+5×105 5×104+5×105 处理组3
Treatment group 31×105+5×105 1×105+5×105 处理组4
Treatment group 45×105+5×105 5×105+5×105 实验二: 研究不同温度和有毒铜绿微囊藻浓度以及它们的交互作用对萼花臂尾轮虫生活史的影响, 实验设计在5个温度梯度下进行, 食物是有毒铜绿微囊藻和蛋白核小球藻的组合, 其中小球藻浓度为5×105 cells/mL(碳含量为4.50 μg C/mL), 铜绿微囊藻有5个浓度梯度(对照组碳含量为4.50 μg C/mL, 处理组1碳含量为4.60 μg C/mL, 处理组2碳含量为4.99 μg C/mL, 处理组3碳含量为5.48 μg C/mL, 处理组4碳含量为9.40 μg C/mL), 实验共25组, 如表 2所示。
表 2 实验二中不同处理组食物情况(浓度单位cells/mL)Table 2. Food concentration of different treatments in experiment 2 (cells/mL)组别Group 15℃ 20℃ 25℃ 30℃ 35℃ 对照组Control group 0+5×105 0+5×105 0+5×105 0+5×105 0+5×105 处理组1Treatment group 1 1×104+5×105 1×104+5×105 1×104+5×105 1×104+5×105 1×104+5×105 处理组2Treatment group 2 5×104+5×105 5×104+5×105 5×104+5×105 5×104+5×105 5×104+5×105 处理组3Treatment group 3 1×105+5×105 1×105+5×105 1×105+5×105 1×105+5×105 1×105+5×105 处理组4Treatment group 4 5×105+5×105 5×105+5×105 5×105+5×105 5×105+5×105 5×105+5×105 1.4 动态生命表实验
实验一: 正式实验前, 将萼花臂尾轮虫置于25℃光照培养箱中进行一周预培养实验, 取带卵的非混交雌体, 放置烧杯中进行培养, 再取孵出的非混交后代(年龄≤6h)若干, 分别放置于24孔板中进行实验, 实验所用的食物浓度如表 1所示。每孔放一只轮虫。每12h观察一次, 记录轮虫带卵数量、母体存活数量以及新生幼体数, 并将新生幼体从培养体系中移除, 每24h更换一次食物和EPA培养液, 实验至全部母体死亡为止。
实验二: 实验开始前, 将萼花臂尾轮虫分别置于15℃、20℃、25℃、30℃和35℃光照培养箱中进行1周预培养实验, 其他操作同实验一, 实验所用的食物浓度如表 2所示。
1.5 实验参数与统计分析
轮虫生活史参数计算方法参照Hu和Xi[22]:
This page contains the following errors:
error on line 1 at column 1: Start tag expected, '<' not foundBelow is a rendering of the page up to the first error.
This page contains the following errors:
error on line 1 at column 1: Start tag expected, '<' not foundBelow is a rendering of the page up to the first error.
This page contains the following errors:
error on line 1 at column 1: Start tag expected, '<' not foundBelow is a rendering of the page up to the first error.
实验一中的铜绿微囊藻品系和浓度及实验二中铜绿微囊藻浓度和培养温度对萼花臂尾轮虫3个生活史参数的影响均采用非参数双因素方差分析(Scheirer-Ray-Hare test)进行检验。该数据分析在R软件中完成[23]。
2. 结果
2.1 两种品系铜绿微囊藻对萼花臂尾轮虫生命表参数的影响
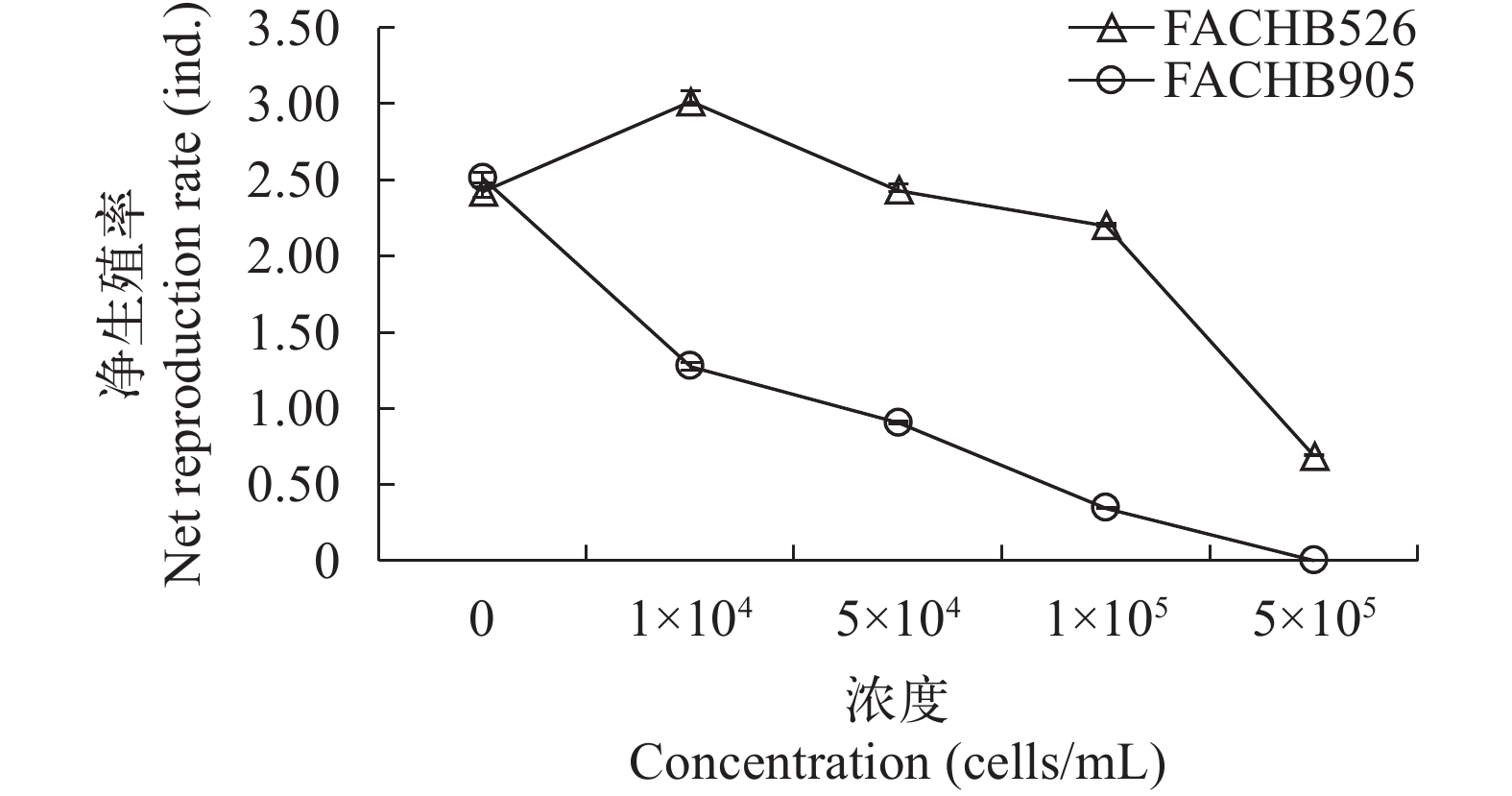
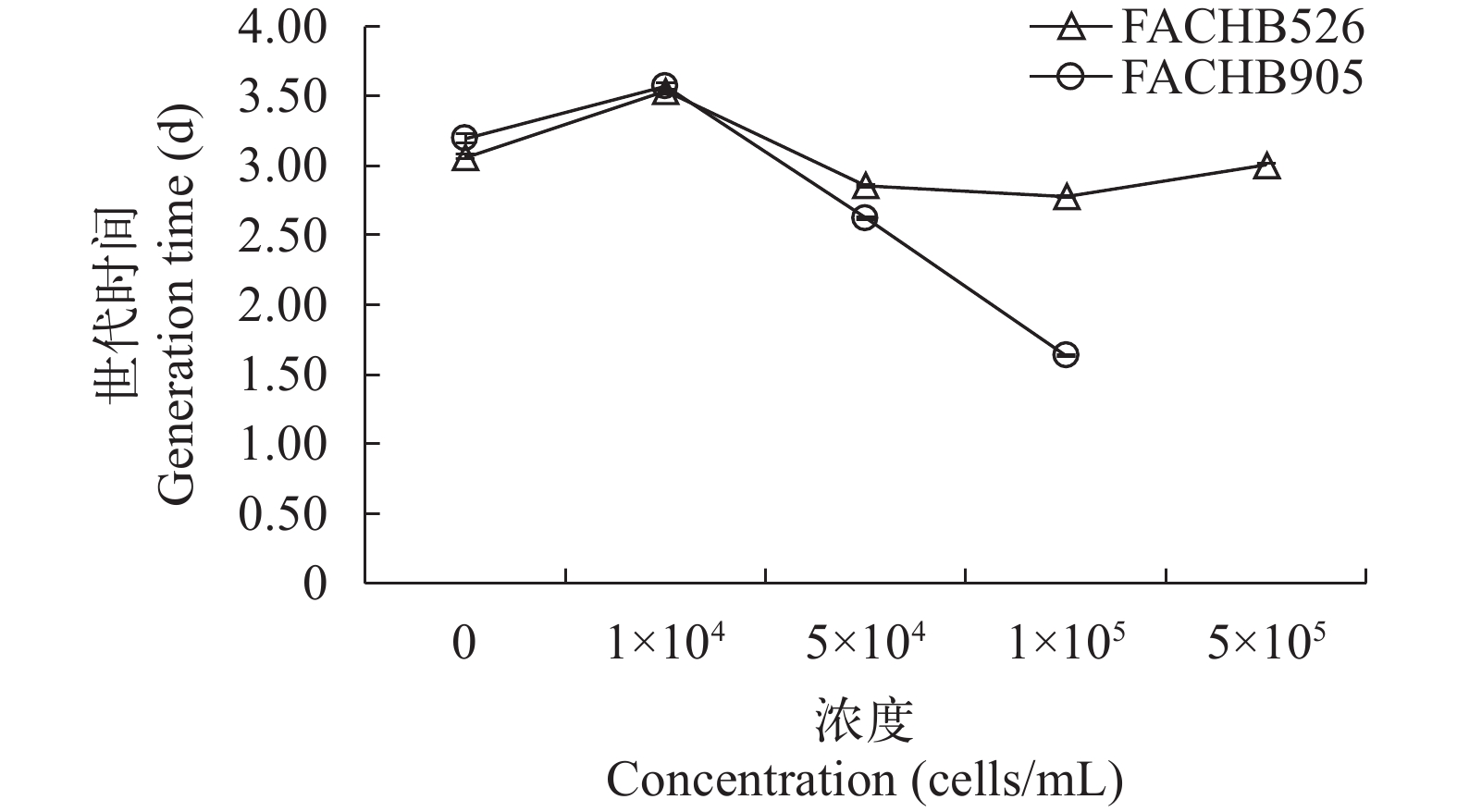
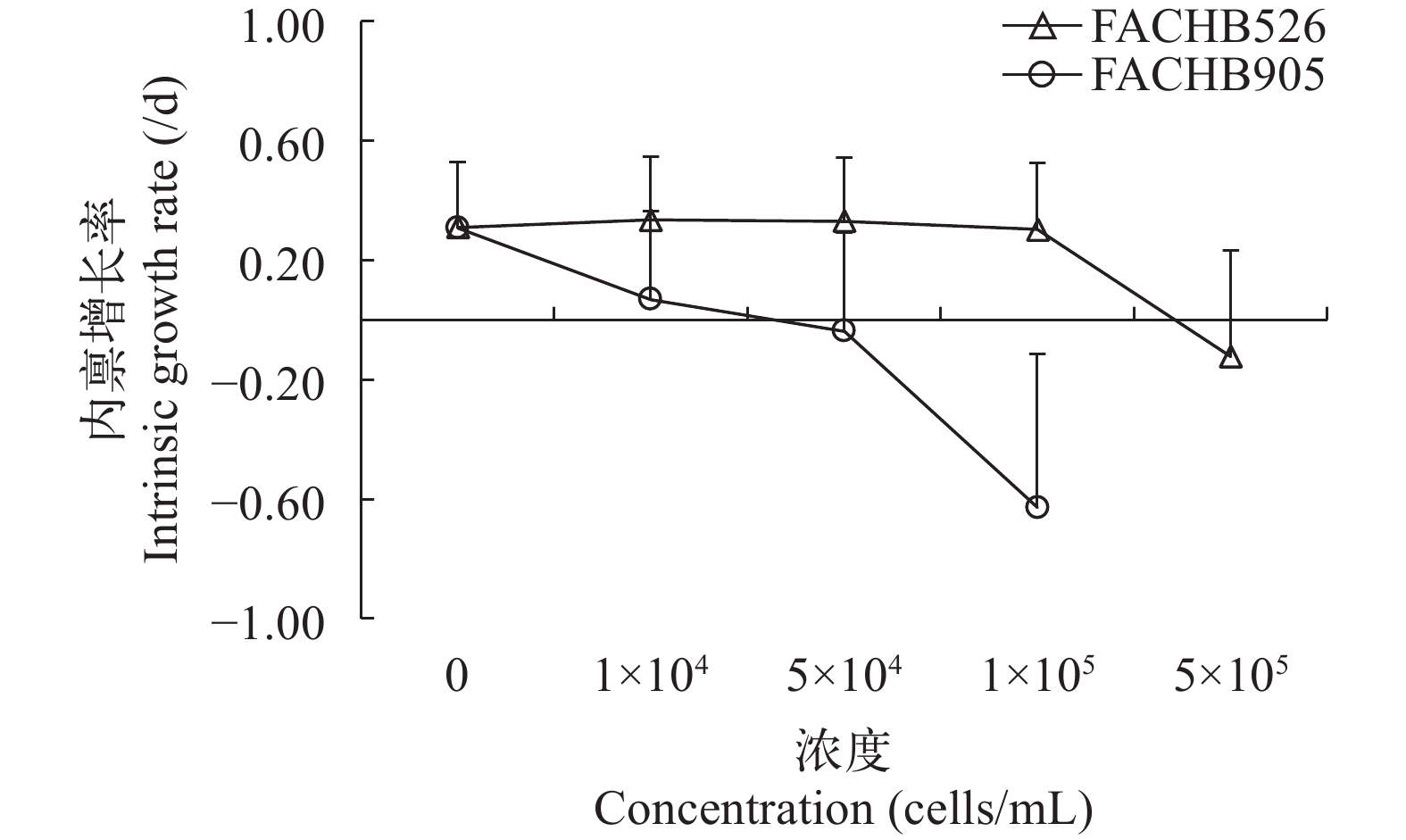
结果分析得出随着无毒铜绿微囊藻浓度升高, 轮虫生活史参数净生殖率(R0)下降(图 1), 世代时间(T)先上升后下降(图 2), 内禀增长率(rm)呈现下降趋势(图 3)。与对照组相比较, 当无毒铜绿微囊藻浓度为104 cells/mL时, 轮虫净生殖率上升19.9%, 世代时间上升13.6%, 内禀增长率上升6.1%, 无毒铜绿微囊藻浓度为5×105 cells/mL时, 轮虫内禀增长率为负值。
有毒铜绿微囊藻浓度升高, 轮虫生活史参数净生殖率显著下降, 世代时间缩短, 内禀增长率明显下降。并且有毒铜绿微囊藻浓度升高, 微囊藻毒性会增强, 轮虫摄食微囊藻机率变大, 食物品质下降, 有毒铜绿微囊藻浓度为5×104和1×105 cells/mL轮虫内禀增长率为负值, 而铜绿微囊藻浓度为5×105 cells/mL内禀增长率和世代时间无法计算。与对照组相比较, 当铜绿微囊藻浓度为1×105 cells/mL时, 在无毒铜绿微囊藻中轮虫净生殖率下降9.1%, 有毒铜绿微囊藻中下降86.5%; 在无毒铜绿微囊藻中轮虫世代时间下降9.2%, 而在有毒铜绿微囊藻中下降48.9%, 无毒铜绿微囊藻中轮虫内禀增长率下降2.0%, 而在有毒铜绿微囊藻中下降303.2%。方差分析结果显示铜绿微囊藻毒性与食物浓度对轮虫净生殖率和内禀增长率的影响具有显著性交互作用(表 3)。
表 3 铜绿微囊藻毒性和浓度对轮虫生活史参数R0及rm影响的非参数双因素方差分析的结果Table 3. Effects of toxicity and concentrations of Microcystis aeruginosa on the R0 and rm of Brachionus calyciflorus by the Scheirer-Ray-Hare test参数Parameter R0 rm F P F P 毒性Toxicity 31.83 0.000* 34.67 0.000* 浓度Concentration 30.36 0.000* 18.73 0.001* 毒性×浓度Toxicity×Concentration 13.51 0.004* 12.99 0.005* 注: *表示极显著P<0.01Note: *Represents extremely significant P<0.01 2.2 温度与有毒铜绿微囊藻浓度对萼花臂尾轮虫生命表参数的影响
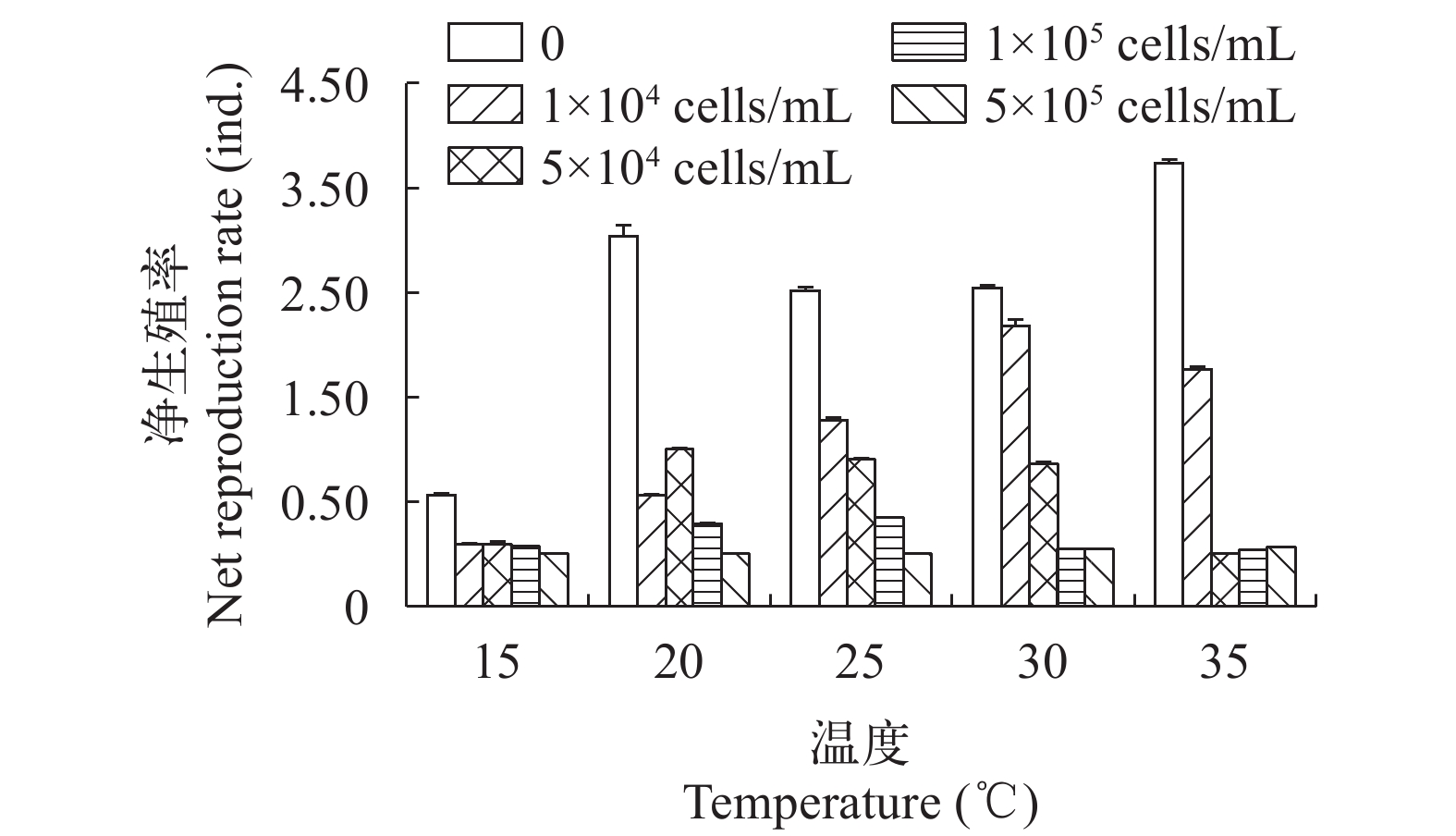
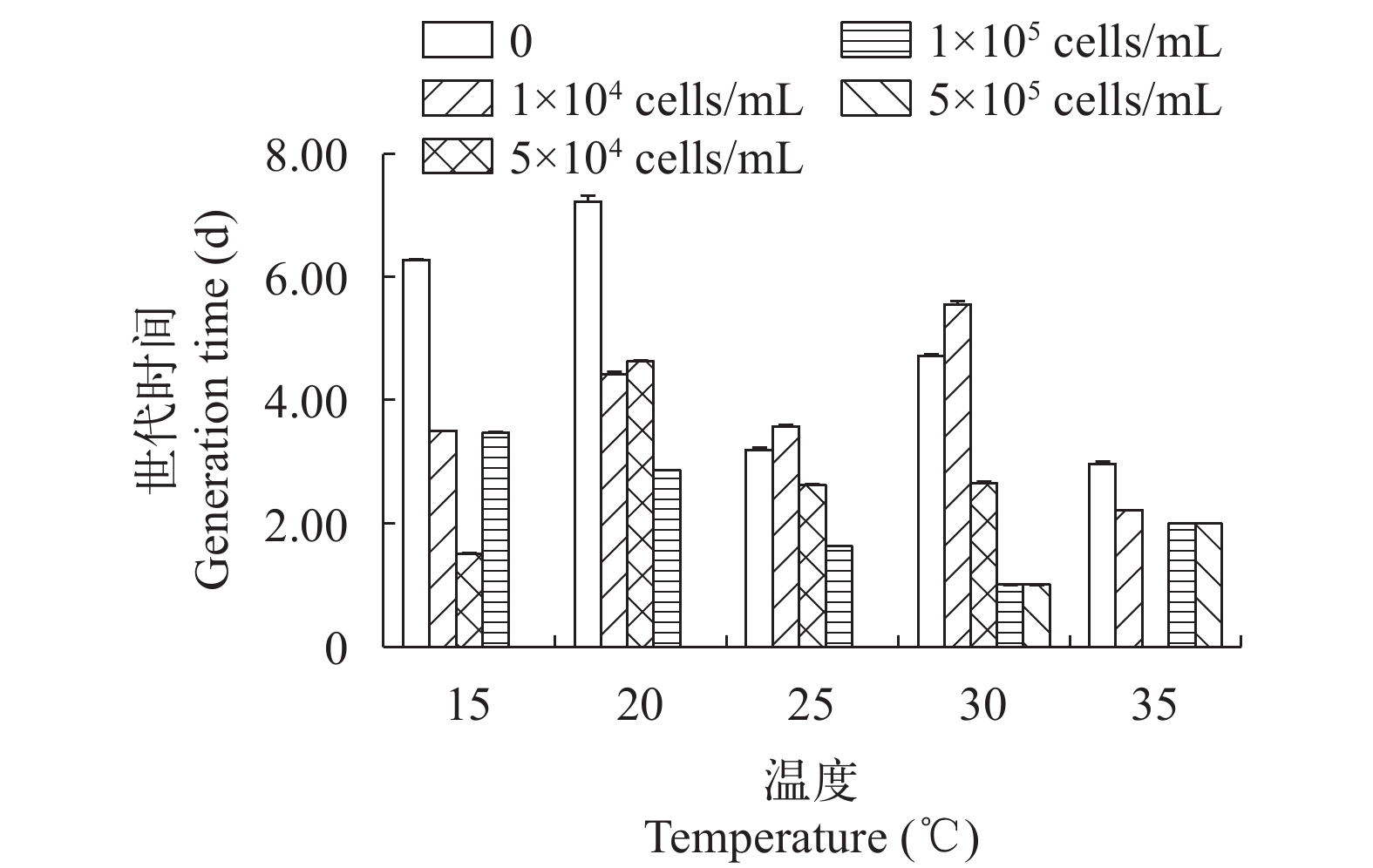
在五个温度下不同浓度的有毒铜绿微囊藻对萼花臂尾轮虫净生殖率的影响的研究结果显示, 在不添加有毒铜绿微囊藻的情况下, 即有毒铜绿微囊藻浓度为0时, 随着温度升高, 轮虫净生殖率总体呈上升趋势(图 4), 与最低温15℃相比较, 20℃净生殖率上升81.6%, 25℃净生殖率上升77.7%, 30℃净生殖率上升80.0%, 温度为35℃时, 净生殖率最高。因为在高温条件下, 轮虫新陈代谢加速, 生长繁殖变快。处理组则随温度和有毒铜绿微囊藻浓度变化而有所不同, 有毒微囊藻浓度为1×104、5×104和1×105 cells/mL, 随着温度升高净生殖率也呈现出上升趋势, 但是在高浓度(5×105 cells/mL)下轮虫的净生殖率基本为0, 在高温(30℃和35℃)作用下高浓度有毒铜绿微囊藻抑制轮虫生长繁殖的作用更加显著。图 5实验结果显示, 世代时间随着温度的升高整体呈下降趋势, 随着有毒铜绿微囊藻浓度增加, 世代时间逐渐下降。
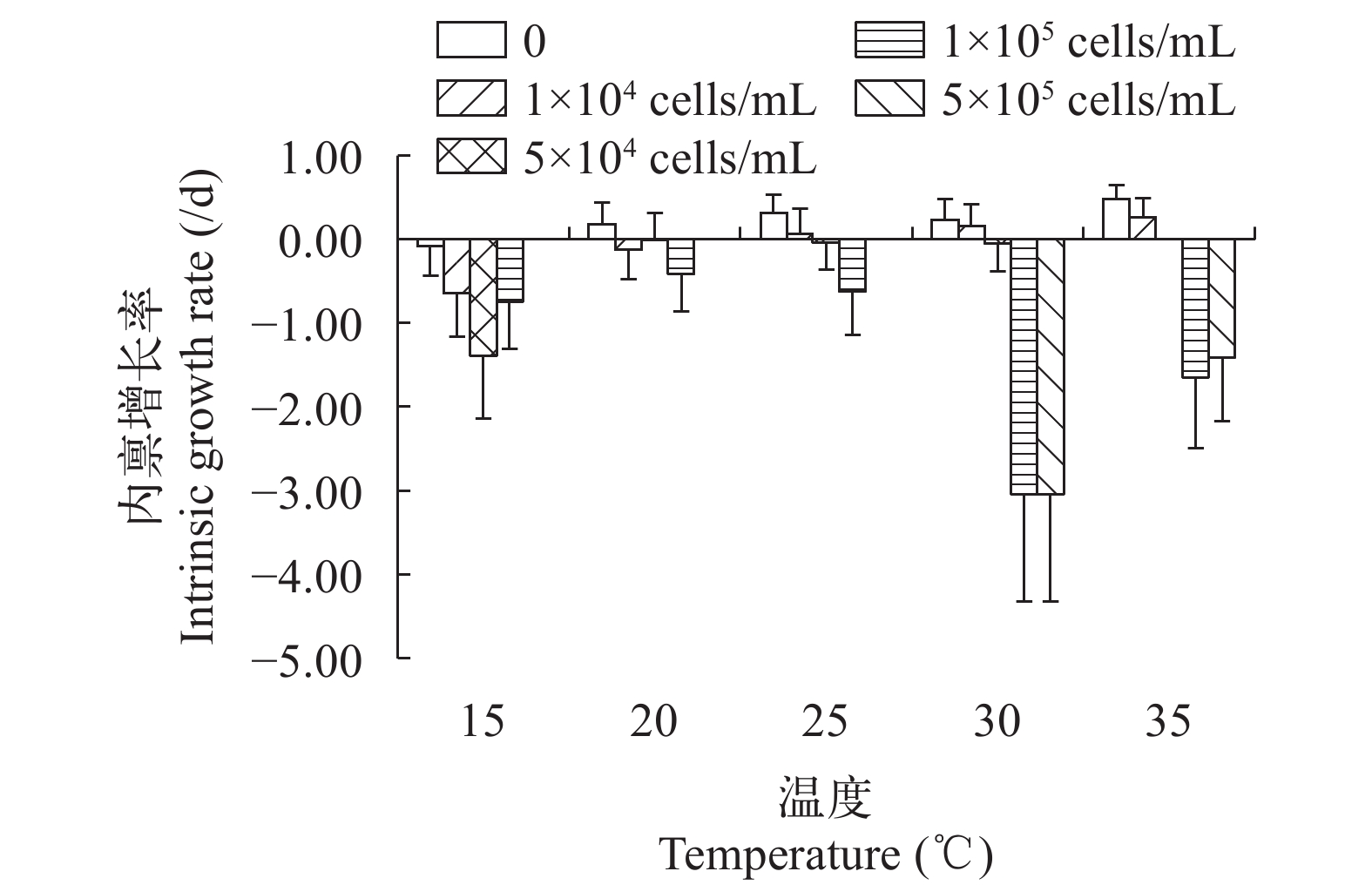
温度与有毒铜绿微囊藻浓度对萼花臂尾轮虫内禀增长率的影响的实验结果表明, 温度升高, 内禀增长率变化显著(图 6和表 4)。在15℃下内禀增长率为负值说明低温环境下不利于轮虫的生长繁殖。有毒铜绿微囊藻低浓度(1×104 cells/mL)时, 轮虫种群的内禀增长率随着温度的升高而增加。与对照组相比, 低浓度微囊藻对轮虫有抑制作用, 但是这种抑制作用并不总是随温度的升高而加强。铜绿微囊藻在较高浓度(1×105 cells/mL)时, 内禀增长率为负值, 且从20℃、25℃和30℃得出温度升高内禀增长率变化幅度变大, 所以随着温度升高有毒铜绿微囊藻对萼花臂尾轮虫抑制作用更加明显。有毒铜绿微囊藻高浓度(5×105 cells/mL)下轮虫种群的内禀增长率有些组无法计算, 因为轮虫个体只存活了2d, 没有产子代。
表 4 有毒铜绿微囊藻浓度和温度对轮虫生活史参数R0及rm影响的非参数双因素方差分析的结果Table 4. Effects of temperatures and concentrations of microcystin-producing Microcystis aeruginosa on the R0 and rm of Brachionus calyciflorus based on the Scheirer-Ray-Hare test参数Parameter R0 rm F P F P 浓度Concentration 148.29 0.000* 143.87 0.000* 温度Temperature 30.46 0.000* 29.71 0.000* 浓度×温度Concentration×
Temperature28.00 0.006* 33.94 0.001* 注: *表示极显著P<0.01Note: *Represents extremely significant P<0.01 经低温或高温胁迫后的轮虫生活史参数均变化显著, 且有毒铜绿微囊藻浓度升高轮虫生活史参数显著下降。方差分析结果表明浓度和温度的交互作用对轮虫种群的净生殖率和内禀增长率变化极显著(F=28.00, P<0.01; F=33.94, P<0.01; 表 4), 实验结果表明在高温30℃和35℃环境下有毒铜绿微囊藻浓度升高对轮虫抑制作用更加明显, 有毒铜绿微囊藻对轮虫的抑制作用随着温度的升高而加强。
3. 讨论
无毒铜绿微囊藻在低浓度下对萼花臂尾轮虫的生长和繁殖有促进作用, 表明无毒铜绿微囊藻可作为轮虫食物来源, 无毒铜绿微囊藻缺乏脂肪酸等营养物质, 且食物质量没有蛋白核小球藻食物质量高, 高浓度下轮虫摄食无毒铜绿微囊藻机率变大, 整体食物品质下降, 臂尾轮虫是滤食性动物, 无法根据颗粒物的质量来选择食物[24], 只能根据颗粒物的大小来选择食物, 轮虫不可避免地摄食铜绿微囊藻[10], 所以无毒铜绿微囊藻高浓度下对轮虫有抑制作用。与无毒铜绿微囊藻相比, 有毒铜绿微囊藻对轮虫种群的抑制作用更加明显, 微囊藻浓度升高净生殖率和内禀增长率显著下降, 表明有毒铜绿微囊藻不利于轮虫的生长繁殖。有毒铜绿微囊藻需要考虑食物质量和微囊藻毒素两个方面, 以微囊藻毒素-LR为例, MC-LR能够在浮游动物体内产生生物富集作用[25]。微囊藻与绿藻混合作为轮虫食物, 微囊藻不能被认为是轮虫致命的有毒物质, 尽管在细胞中存在MC, 但它仅是一个营养不足的食物来源, 但是当微囊藻作为轮虫唯一的食物, 微囊藻不支持轮虫生长, 高浓度时甚至在2d内全部死亡[26, 27], 这与本实验中高浓度下轮虫只存活两天结果一致。不同种类的轮虫也会有类似的结果, 褶皱臂尾轮虫(Brachionus plicatilis)在铜绿微囊藻(PCC7820)低浓度(1×104 cells/mL)时, 能够从中摄取一定营养以供其生长繁殖, 在铜绿微囊藻高浓度(1×106 cells/mL)时, 抑制轮虫种群密度的增长[28]。不仅是生活史参数会受铜绿微囊藻的影响, 轮虫的表型和摄食率都会受到微囊藻的影响。有研究发现高浓度的MC-LR对低温下萼花臂尾轮虫的形态学特征产生显著抑制作用并且轮虫会通过改变表型特征抵御不良环境[29, 30], 还有研究表明在无MC-LR和低MC-LR浓度组中, 温度升高会刺激萼花臂尾轮虫的摄食行为[15]。不论无毒还是有毒铜绿微囊藻, 对于萼花臂尾轮虫都是质量不佳的食物, 且有毒铜绿微囊藻还会产生毒素抑制萼花臂尾轮虫的生长繁殖及其表型特征。
有毒铜绿微囊藻对轮虫有抑制作用, 温度和微囊藻浓度以及二者之间的交互作用对轮虫生活史参数净生殖率和内禀增长率均有显著性影响, 铜绿微囊藻浓度升高对轮虫的抑制作用加强, 且这种抑制作用随着温度的升高而加剧, 这与Zhang和Geng[31]的研究结果一致。温度是影响每一个生命周期中由单个雌性产生后代总数的一个因素, 且高温下的繁殖力高于低温下的繁殖力[24], 同时温度的升高提高轮虫对微囊藻毒素的吸收能力[32], 在本实验中温度能够显著影响轮虫生活史参数净生殖率和内禀增长率。温度加强有毒铜绿微囊藻对轮虫的抑制作用部分是因为温度升高加剧藻类的磷限制, 有研究结果表明藻类的氮磷限制都会抑制轮虫的生长速度, 磷限制会随温度的升高而增强[8]。温度升高会导致微囊藻产生更高浓度的MC-LR并导致更高毒性的MC-LR变异比例增加, 从而加剧微囊藻对轮虫生长繁殖的影响[33]。裂足臂尾轮虫在3个食物密度下, 温度对其净生殖率均有显著影响, 对其种群内禀增长率均无显著的影响[18]。轮虫对微囊藻表现出不同的耐受性, 是由于轮虫对微囊藻毒素的敏感性存在种间差异造成的[32]。温度升高能够加强有毒铜绿微囊藻对萼花臂尾轮虫的抑制作用。
综上, 铜绿微囊藻毒性, 铜绿微囊藻浓度, 温度以及毒性×浓度与温度×浓度之间的相互作用显著影响了萼花臂尾轮虫的生活史参数净生殖率和内禀增长率。藻类的营养限制比温度效应更重要[7], 本实验通过无毒微囊藻与有毒铜绿微囊藻在不同浓度下各生活史参数整体比较, 得出食物质量与微囊藻毒性对轮虫均有影响。在以后的研究中应结合野外实验, 利用化学计量学方法探讨影响轮虫生长繁殖的主要因素, 重点分析各种因素之间的相互联系。
-
表 1 实验一中不同处理组食物情况(浓度单位cells/mL)
Table 1 Food concentration of different treatments in experiment 1 (cells/mL)
组别Group 无毒铜绿微囊藻+蛋白核小球藻Microcystin-free M. aeruginosa+C. pyrenoidosa 有毒铜绿微囊藻+蛋白核小球藻Microcystin- producing M. aeruginosa+C. pyrenoidosa 对照组Control group 0+5×105 0+5×105 处理组1
Treatment group 11×104+5×105 1×104+5×105 处理组2
Treatment group 25×104+5×105 5×104+5×105 处理组3
Treatment group 31×105+5×105 1×105+5×105 处理组4
Treatment group 45×105+5×105 5×105+5×105 表 2 实验二中不同处理组食物情况(浓度单位cells/mL)
Table 2 Food concentration of different treatments in experiment 2 (cells/mL)
组别Group 15℃ 20℃ 25℃ 30℃ 35℃ 对照组Control group 0+5×105 0+5×105 0+5×105 0+5×105 0+5×105 处理组1Treatment group 1 1×104+5×105 1×104+5×105 1×104+5×105 1×104+5×105 1×104+5×105 处理组2Treatment group 2 5×104+5×105 5×104+5×105 5×104+5×105 5×104+5×105 5×104+5×105 处理组3Treatment group 3 1×105+5×105 1×105+5×105 1×105+5×105 1×105+5×105 1×105+5×105 处理组4Treatment group 4 5×105+5×105 5×105+5×105 5×105+5×105 5×105+5×105 5×105+5×105 表 3 铜绿微囊藻毒性和浓度对轮虫生活史参数R0及rm影响的非参数双因素方差分析的结果
Table 3 Effects of toxicity and concentrations of Microcystis aeruginosa on the R0 and rm of Brachionus calyciflorus by the Scheirer-Ray-Hare test
参数Parameter R0 rm F P F P 毒性Toxicity 31.83 0.000* 34.67 0.000* 浓度Concentration 30.36 0.000* 18.73 0.001* 毒性×浓度Toxicity×Concentration 13.51 0.004* 12.99 0.005* 注: *表示极显著P<0.01Note: *Represents extremely significant P<0.01 表 4 有毒铜绿微囊藻浓度和温度对轮虫生活史参数R0及rm影响的非参数双因素方差分析的结果
Table 4 Effects of temperatures and concentrations of microcystin-producing Microcystis aeruginosa on the R0 and rm of Brachionus calyciflorus based on the Scheirer-Ray-Hare test
参数Parameter R0 rm F P F P 浓度Concentration 148.29 0.000* 143.87 0.000* 温度Temperature 30.46 0.000* 29.71 0.000* 浓度×温度Concentration×
Temperature28.00 0.006* 33.94 0.001* 注: *表示极显著P<0.01Note: *Represents extremely significant P<0.01 -
[1] Majagi S, Vijaykumar K. Ecology and abundance of zooplankton in Karanja reservoir [J]. Environmental Monitoring and Assessment, 2009, 152(1-4): 451-458. doi: 10.1007/s10661-008-0329-z
[2] Dahms H U, Hagiwara A, Lee J S. Ecotoxicology, ecophysiology, and mechanistic studies with rotifers [J]. Aquatic Toxicology, 2011, 101(1): 1-12. doi: 10.1016/j.aquatox.2010.09.006
[3] 杨家新, 黄祥飞. 藻类食物对萼花臂尾轮虫繁殖的影响 [J]. 湖泊科学, 1998, 10: 42-48. doi: 10.18307/1998.0107 Yang J X, Huang X F. The effect of algae on the reproduction of rotifer Brachionus calyciflorus (Rotatoria) [J]. Journal of Lake Sciences, 1998, 10: 42-48. doi: 10.18307/1998.0107
[4] Snell T W, Janssen C R. Rotifers in ecotoxicology: a review [J]. Hydrobiologia, 1995, 313-314(1): 231-247. doi: 10.1007/BF00025956
[5] Lürling M, Beekman W. Influnence of food-type on the population growth rate of the rotifer Brachinus calyciflorus in short-chronic assays [J]. Acta Zoologica Sinica, 2006, 52(1): 70-78.
[6] 邓平, 张生元, 艾桃山, 等. 食物浓度和温度对萼花臂尾轮虫种群动态的影响 [J]. 江苏农业科学, 2016, 44(1): 251-253. Deng P, Zhang S Y, Ai T S, et al. Effects of food concentration and temperature on population dynamics of freshwater rotifer Brachionus calyciflorus [J]. Jiangsu Agricultural Sciences, 2016, 44(1): 251-253.
[7] Jensen T C, Verschoor A M. Effects of food quality on life history of the rotifer Brachionus calyciflorus Pallas [J]. Freshwater Biology, 2010, 49(9): 1138-1151.
[8] Wojewodzic M W, Rachamim T, Andersen T, et al. Effect of temperature and dietary elemental composition on RNA/protein ratio in a rotifer [J]. Functional Ecology, 2011, 25(5): 1154-1160. doi: 10.1111/j.1365-2435.2011.01864.x
[9] Soares M, Lürling M, Huszar V L M, et al. Changes in species composition during annual cyanobacterial dominance in a tropical reservoir: physical factors, nutrients and grazing effects [J]. Aquatic Microbial Ecology, 2009, 57(2): 137-149.
[10] Rothhaupt K O. Differences in particle size-dependent feeding efficiencies of closely related rotifer species [J]. Limnology and Oceanography, 1990, 35(1): 16-23. doi: 10.4319/lo.1990.35.1.0016
[11] 金丽娜, 徐小清. 微囊藻毒素对鱼类毒性影响的研究进展 [J]. 水生生物学报, 2003, 27(6): 644-647. doi: 10.3321/j.issn:1000-3207.2003.06.016 Jin L N, Xu X Q. A reviow of the toxic effect of microcystin on fish [J]. Acta Hydrobiologia Sinica, 2003, 27(6): 644-647. doi: 10.3321/j.issn:1000-3207.2003.06.016
[12] Zhao S Y, Wang Y, Li D J. Effects of toxic and non-toxic Microcystis aeruginosa in different mixtures with Scenedesmus obliquus on growth of Brachionus calyciflorus [J]. Journal of Freshwater Ecology, 2014, 29(3): 377-386. doi: 10.1080/02705060.2014.895435
[13] Huang L, Xi Y L, Xu X P, et al. Responses in population growth and reproduction of the freshwater rotifer Brachionus calyciflorus to microcystin-LR at different temperatures [J]. Annales de Limnologie-International Journal of Limnology, 2012, 48(4): 383-390. doi: 10.1051/limn/2012029
[14] Lenz P H, Hower A E, Hartline D K. Temperature compensation in the escape response of a marine copepod, Calanus finmarchicus (Crustacea) [J]. Biological Bulletin, 2005, 209(1): 75-85. doi: 10.2307/3593143
[15] Xiang X L, Chen Y Y, Xu Q L, et al. Combined effects of temperature and the microcystin MC-LR on the feeding behavior of the rotifer Brachionus calyciflorus [J]. Bulletin of Environmental Contamination and Toxicology, 2017, 99(4): 493-499. doi: 10.1007/s00128-017-2172-9
[16] 鲍蕾, 马蕊, 牛翠娟, 等. 温度对方形臂尾轮虫(Brachionus quadridentatus)种群增长与生活史参数的影响 [J]. 北京师范大学学报(自然科学版), 2006, 42(5): 518-521. doi: 10.3321/j.issn:0476-0301.2006.05.020 Bao L, Ma R, Nui C J, et al. Effects of temperature on life history and population growth of the rotifer Brachionus quadridentatus [J]. Journal of Beijing Normal University (
Natural Science ) , 2006, 42(5): 518-521. doi: 10.3321/j.issn:0476-0301.2006.05.020 [17] 温新利, 席贻龙. 镜湖常见臂尾轮虫(Brachionus)种群周年动态及生活史对策 [J]. 生态学报, 2007, 27(10): 3956-3963. doi: 10.3321/j.issn:1000-0933.2007.10.002 Wen X L, Xi Y L. Population dynamics and life history strategy of the common Brachionus species (rotifera) in lake Jinghu [J]. Acta Ecologica Sinica, 2007, 27(10): 3956-3963. doi: 10.3321/j.issn:1000-0933.2007.10.002
[18] 宁乐锋, 席贻龙, 孙强, 等. 温度和食物密度对裂足臂尾轮虫(Brachionus diversicornis)生命表统计学参数的影响 [J]. 湖泊科学, 2013, 25(2): 295-301. doi: 10.3969/j.issn.1003-5427.2013.02.018 Ning L F, Xi Y L, Sun Q, et al. Combined effects of temperature and algal food density on life table demography of Brachionus diversicornis (Rotifera) [J]. Journal of Lake Sciences, 2013, 25(2): 295-301. doi: 10.3969/j.issn.1003-5427.2013.02.018
[19] 耿红, 孟希, 贺萌. 不同绿藻浓度下铜绿微囊藻对轮虫生活史的影响 [J]. 中南民族大学学报, 2016, 35(1): 44-49. Geng H, Meng X, He M. Effect of Microcystis aeruginosa on the rotifer life history at different concentrations of green algae [J]. Journal of South-Central University for Nationalities, 2016, 35(1): 44-49.
[20] Agency U S E P. Methods for measuring the acute toxicity of effluents and receiving waters to freshwater and marine organisms [J]. United States Environmental Protection Agency, 2002: 1-266.
[21] Stanier R Y, Kunisawa R, Mandel M, et al. Purification and properties of unicellular blue-green algae (order Chroococcales) [J]. Bacteriological Reviews, 1971, 35(2): 171-205.
[22] Hu H Y, Xi Y L. Demographic parameters and mixis of three Brachionus angularis Gosse (rotatoria) strains fed on different algae [J]. Limnologica, 2008, 38(1): 56-62. doi: 10.1016/j.limno.2007.08.002
[23] R Development Core Team (2017). R: A Language and Environment for Statistical Computing. Version 3.1. 2. R Foundation for Statistical
[24] Demott W R. The role of taste in food selection by freshwater zooplankton [J]. Oecologia, 1986, 69(3): 334-340. doi: 10.1007/BF00377053
[25] Ferrão-Filho A S, Kozlowsky-Suzuki B. Cyanotoxins: bioaccumulation and effects on aquatic animals [J]. Marine Drugs, 2011, 9(12): 2729-2772. doi: 10.3390/md9122729
[26] Liang Y, Ouyang K, Chen X, et al. Life strategy and grazing intensity responses of Brachionus calyciflorus fed on different concentrations of microcystin-producing and microcystin-free Microcystis aeruginosa [J]. Scientific Reports, 2017, 7(1): 43127. doi: 10.1038/srep43127
[27] Soares M C S, Lürling M, Huszar V L M. Responses of the rotifer Brachionus calyciflorus to two tropical toxic cyanobacteria (Cylindrospermopsis raciborskii and Microcystis aeruginosa) in pure and mixed diets with green algae [J]. Journal of Plankton Research, 2010, 32(7): 999-1008. doi: 10.1093/plankt/fbq042
[28] 谢钦铭, 骆和东, 魏施, 等. 铜绿微囊藻对褶皱臂尾轮虫种群生长的影响 [J]. 安徽农业科学, 2016, 44(35): 11-13. doi: 10.3969/j.issn.0517-6611.2016.35.004 Xie Q M, Luo H D, Wei S, et al. Effects of Microcysis aeruginosa on the population growth of Brachionus plicatilis [J]. Journal of Anhui Agricultural Sciences, 2016, 44(35): 11-13. doi: 10.3969/j.issn.0517-6611.2016.35.004
[29] 梁叶, 欧阳凯, 许欢欢, 等. 铜绿微囊藻对轮虫生命表参数和表型特征的影响 [J]. 水生生物学报, 2016, 41(6): 1362-1368. Liang Y, Ouyang K, Xu H H, et al. Effects of Microcystic aeruginosa on the life-table papameters and phenotypic traits of rotifers [J]. Acta Hydbobiologica Sinica, 2016, 41(6): 1362-1368.
[30] 项贤领, 朱凌云, 陈莹莹, 等. 微囊藻毒素和温度对萼花臂尾轮虫形态学特征的影响 [J]. 湖泊科学, 2018, 30(4): 1027-1040. doi: 10.18307/2018.0416 Xiang X L, Zhu L Y, Chen Y Y, et al. Combined effects of the microcystin MC-LR and temperature on the morphological features of Brachionus calyciflorus [J]. Journal of Lake Sciences, 2018, 30(4): 1027-1040. doi: 10.18307/2018.0416
[31] Zhang X, Geng H. Effect of Microcystis aeruginosa on the rotifer Brachionus calyciflorus at different temperatures [J]. Bulletin of Environmental Contamination and Toxicology, 2012, 88(1): 20-24. doi: 10.1007/s00128-011-0450-5
[32] 朱永津, 陆开宏, 潘洁慧. 微囊藻水华对淡水浮游动物轮虫和枝角类影响的研究进展 [J]. 中国水产科学, 2008, 15(2): 367-375. doi: 10.3321/j.issn:1005-8737.2008.02.024 Zhu Y J, Lu K H, Pan J H. Progress in the effect of Microcystis bloom on freshwater zooplankton rotifer and cladoceran [J]. Journal of Fishery Sciences of China, 2008, 15(2): 367-375. doi: 10.3321/j.issn:1005-8737.2008.02.024
[33] Giannuzzi L, Krock B, Minaglia M C C, et al. Growth, toxin production, active oxygen species and catalase activity of Microcystis aeruginosa (Cyanophyceae) exposed to temperature stress [J]. Comparative Biochemistry and Physiology Part C: Toxicology and Pharmacology, 2016(189): 22-30.
-
期刊类型引用(5)
1. 王鹏,梁叶. 网状原角藻与微塑料对典型浮游动物的联合毒性效应. 生态毒理学报. 2024(05): 368-382 .  百度学术
百度学术
2. 葛雅丽,张峰,曹漫漫,罗彤,席贻龙. 大型和小型萼花臂尾轮虫的遗传和生活史特征比较研究. 生态学报. 2023(13): 5491-5504 .  百度学术
百度学术
3. 张根,陈宝锐. 轮虫生态毒理学测试指标的敏感性研究进展. 应用生态学报. 2022(03): 855-864 .  百度学术
百度学术
4. 崔宇翔,张树林,刘毅,罗颖,祁洪芳,杨建新,吴洪芳,张清靖. 温度对低盐驯化褶皱臂尾轮虫生活史参数的影响. 大连海洋大学学报. 2022(06): 968-976 .  百度学术
百度学术
5. 卫向东,郭匿春,杨利源,李静. 温度和铜绿微囊藻浓度对萼花臂尾轮虫生活史参数的影响. 安徽农业科学. 2021(22): 74-79+91 .  百度学术
百度学术
其他类型引用(7)



 下载:
下载: