MORPHOLOGICAL DEVELOPMENT AND ALLOMETRIC GROWTH PATTERN OF KONOSIRUS PUNCTATUS AT LARVAE AND JUVENILE STAGES
-
摘要: 运用光学显微镜技术和实验生态学方法, 对斑鰶(Konosirus punctatus)早期形态发育观察、异速生长模式及其生态学意义进行了研究。结果表明: 在水温(21.5±0.5)℃下, 初孵仔鱼全长(3.18±0.52) mm, 斑鰶仔鱼期从孵化出膜到43日龄棱鳞开始出现前, 稚鱼期从44日龄棱鳞出现到55日龄全身覆满鳞片。斑鰶的形态变化和器官分化主要发生在仔鱼期。斑鰶的吻长、躯干长、肠道长、胸鳍长、腹鳍长等重要形态学指标均存在异速生长现象, 其生长拐点依次为 42日龄(TL: 26.41 mm)、24日龄(TL: 15.57 mm)、31日龄(TL: 21.41 mm)、41日龄(TL: 25.47 mm)、42日龄(TL: 26.41 mm)。相对于全长、吻长和胸鳍长在拐点前后由正异速生长变为等速生长, 腹鳍长由正异速生长转为负异速生长, 这为呼吸、摄食和成功逃避捕食者提供有利条件; 而肠道长由负异速生长变为等速生长, 这可能与斑鰶的食性转化有关。综上所述, 为适应复杂多变的生存环境, 斑鰶在早期发育阶段优先发育对生长生存起关键作用的器官, 这对提高仔、稚鱼的存活率具有重要的生态学意义。研究将为今后进一步人工繁育和苗种培育提供理论依据。Abstract: This study investigated the morphological development and allometric growth pattern in early life cycle of Konosirus punctatus and illustrated their crucial ecological meanings for survival. Results showed that the average total length of larvae fish was (3.18±0.52) mm with water temperature at (21.5±0.5)℃. The morphological development of K. punctatus was divided into larvae stage (0—43 day age, from hatching to keeled scales appearing) and fry stage (44—55 day age, from keeled scales appearing to scales covering the body). Morphological changes and organ diffe-rentiations mainly occurred in the larval stage. Key morphological characteristics including rostrum length, trunk length, intestinal length, pectoral length and pelvic fin length exhibited allometric growth patterns, in which the growth infle-xion point were 42 day age (TL: 25.47 mm), 24 day age (TL: 15.57 mm), 31 day age (TL: 21.41 mm), 41 day age (TL: 25.47 mm), 42 day age (26.41 mm), respectively. The growth rate in rostrum length and pectoral length changed from the positive allometry (before inflexion point) to the same rate (after inflexion point); the growth rate in pelvic fin length changed from the positive allometry to the negative allometry. These variations could enhance the capacities of breathing, feeding and escaping. The growth rate in intestinal length changed from negative allometry to the same rate, which is related to the dietary conversion of K. punctatus. To adapt to the complex environments, key organs involved in growth and survival were preferentially developed at the early stage, which facilitated the survival rate of K. punctatus. All the findings provide a fundamental evidence for artificial breeding and seedling cultivation in the future.
-
Keywords:
- Konosirus punctatus /
- Larvael fish /
- Juvenile fish /
- Morphological development /
- Allometric growth
-
异速生长是指生物体某一类功能器官的相对生长速率不同于身体其他部分的相对生长速率的现象, 是动植物长期适应外界环境所进化保留下来的发育特征[1]。在鱼类早期生长阶段, 由于个体发育受生理、环境条件(温度、盐度、光照、饵料等)的影响, 仔、稚鱼各器官的生长并不同步[2], 从而某些功能器官相对于整体的生长速度要快, 但相应功能完善后, 其生长会减缓或等速于整体生长。这种发育策略保证了仔、稚鱼如摄食、呼吸和运动等重要器官优先发育, 从而提高了其逃避敌害和主动摄食的能力, 为适应复杂多变的生活环境提供了保障。
目前我国海水鱼类养殖的主导品种多为肉食性鱼类, 但随着养殖集约化开展, 动物蛋白饵料需求进一步增大, 加之动物饵料资源和水域资源有限, 从而导致养殖成本不断攀升。因此, 调整和优化养殖品种结构和养殖模式将是促进我国海水鱼类养殖经济和生态效益协调发展的重要途径[3, 4]。因此, 开发以植物食性为主又兼具海鲜品质特征的养殖品种, 对我国鱼类养殖业健康可持续发展具有重要意义。斑鰶(Konosirus punctatus)隶属硬骨鱼纲(Osteichthyes)、鲱形目(Clupeiformes)、鲱科(Clupeidae)、斑鰶属(Konosirus), 俗称窝斑鰶、扁鰶、海鲫、斑点水滑。在我国黄渤海、东海、南海均有分布, 主要栖息在内湾浅海区, 以海湾和河口比较多, 是我国沿海常见的小型经济鱼类。斑鰶适盐范围广, 肉质鲜美, 生长速度快, 食物链短, 当年就可以达到商品鱼规格, 具有很高的经济价值[5]。斑鰶蛋白质含量高, 是制作明胶、生物活性肽及调味料等的优质原料[6]。斑鰶是食物网中生态位最低的鱼类之一, 成鱼主要以浮游生物和有机碎屑为食[7—9]。斑鰶独特的生态位和摄食习性, 促使其成为海水池塘混养和增殖放流的绝佳品种。目前, 关于斑鰶的研究主要集中在群体遗传[10]、营养价值[11]及摄食习性[8, 12]。日本学者研究表明斑鰶1龄就可以部分达到性成熟, 雌性鱼体长达到15 cm性成熟[13]。虽已有报道海水鲱科鱼类早期生长发育方面的研究[14, 15], 但鲜有关斑鰶仔、稚鱼发育的研究报道。
本文主要对人工繁育的斑鰶仔、稚鱼的形态特征、生长及器官发育等方面进行了详尽地形态学观察和测量, 分析了仔、稚鱼各功能器官的异速生长过程, 描述了不同功能器官的发育时序, 阐释了斑鰶早期生长发育与生态环境相适应的机制, 并建立了异速生长模型。研究结果将更好地了解斑鰶仔、稚鱼发育过程, 为斑鰶人工繁育技术提供理论基础和实践指导, 尤其对指导生产和提高仔、稚鱼早期发育过程中的成活率具有重要意义。
1. 材料与方法
1.1 实验材料
2017年4月20日在浙江省海洋水产研究所试验场基地养殖池塘里选择体质健壮、性成熟特征明显的斑鰶亲鱼, 采用干法人工授精获得受精卵。取同一批次的受精卵立即转移到玻璃钢孵化桶装置中, 微充气, 孵化水温维持在(20.0±0.5)℃。移入4h后, 采用虹吸法吸出沉底的坏死卵。孵出仔鱼后转移入800 L玻璃钢培养桶中, 每桶鱼苗密度为80尾/L, 培育水温为(21.5±0.5)℃, 连续充气, 溶解氧量>6.5 mg/L, 总氨氮含量<0.05 mg/L, pH=7.5。采用微流水式底排污的方式, 用300 μm孔径纱网防止幼苗逃逸。调节流水阀门大小保证日换水量达到桶含水量的50%。采用虹吸的方法, 每日将育苗桶中的残饵、排泄物及死去的仔、稚鱼苗清除干净, 保证育苗期间水质清洁。
初孵仔鱼的营养来自于卵黄囊; 3日龄仔鱼可以开口进食, 3—16日投喂轮虫(Brachionus rotundiformis), 轮虫密度保持在15—25个/mL; 8—35日龄投喂丰年虫无节幼体, 初始投喂密度为2个/mL, 以后逐日增加投喂量。30日龄开始驯化投喂颗粒饲料, 并根据鱼苗进食颗粒饲料情况, 逐渐减少丰年虫无节幼体的投喂量, 直至完全被颗粒饲料替代。生物饵料投喂之前需进行营养强化, 轮虫和丰年虫无节幼体使用强化剂Spresso (INVE Aquaculture, Salt Lake City, UT, USA)进行12h营养强化。为保证育苗桶中轮虫能够有足够饵料及为仔、稚鱼提供绿色水体环境, 在投喂轮虫期间同时向育苗桶中加入微量小球藻。颗粒配合饲料品牌: New Love Larva Yu Bao No.1 (Hayashikane Sangyo Co., Ltd., Feed Business Division Chofu Plant)。
1.2 研究方法
使用体视显微镜(SteREO Discovery. V8)和解剖镜(Nikon SMZ-800)观察仔、稚鱼早期形态发育并拍照记录。仔、稚鱼发育阶段的划分参照陈真然等[16]的方法, 即: 从出膜到卵黄囊被完全吸收再到黑色素增加身体不透明、棱鳞开始出现前, 视作仔鱼期; 自棱鳞出现到全身覆满鳞片, 视作稚鱼期。以60%以上的观察样本出现阶段性特征时作为该发育阶段的起始时间。刚孵出仔鱼当天记为0日龄, 从第0日龄开始每天随机抽取10尾仔、稚鱼作为观察材料, 用MS-222麻醉后, 在体视显微镜下观察仔、稚鱼的外部形态变化并拍照记录。如图 1所示斑鰶个体的各测量指标, 以平行或垂直于鱼体水平轴为基准, 使用ZEN 2011 (Blue edition)软件进行测量全长、吻长、头长等13个形态指标; 肠道长度的测量在仔、稚鱼期采用不同的方法: 在仔鱼期身体透明, 肠道没有弯曲, 直接拍照测量; 而稚鱼期肠道开始弯曲采用解剖的方法将肠道伸展开测量图 2中a到b直线距离, 即为肠道长度。长度指标均精确到0.01 mm。然后用10%的中性福尔马林溶液固定全部样本, 避光保存以备查用。
![]() 图 1 斑鰶形态特征测量直观图1. 头长; 2. 头高; 3.上颌长; 4. 眼径; 5. 吻长; 6. 躯干长; 7. 体高; 8. 尾柄长; 9. 背鳍长; 10. 背鳍最后一枚鳍条长; 11. 胸鳍长; 12. 尾鳍; 13. 全长Figure 1. Illustration measurement for K. punctatus1. Head length; 2. Head height; 3. Upper jaw length; 4. Eye diameter; 5. Rostrum; 6. Trunk length; 7. Body height; 8. Caudal peduncle length; 9. Dorsal fin length; 10. The last dorsal fin long; 11. Pectoral length; 12. Tail fin length; 13. Total length
图 1 斑鰶形态特征测量直观图1. 头长; 2. 头高; 3.上颌长; 4. 眼径; 5. 吻长; 6. 躯干长; 7. 体高; 8. 尾柄长; 9. 背鳍长; 10. 背鳍最后一枚鳍条长; 11. 胸鳍长; 12. 尾鳍; 13. 全长Figure 1. Illustration measurement for K. punctatus1. Head length; 2. Head height; 3. Upper jaw length; 4. Eye diameter; 5. Rostrum; 6. Trunk length; 7. Body height; 8. Caudal peduncle length; 9. Dorsal fin length; 10. The last dorsal fin long; 11. Pectoral length; 12. Tail fin length; 13. Total length1.3 数据处理
用SPSS19.0软件分析日龄与全长的关系, 以R2值最大的函数关系式作为最佳拟合生长模式。异速生长模型以幂函数形式即y=axb表示[17], 其中, 自变量x为仔、稚鱼全长, y为与自变量x相对应的各种器官的长度, a为在y轴上截距, b为异速生长指数; 当b值为1时, 表现出等速生长; 当b值大于1时, 表现出快速增长(正异速生长); 当b值小于1时, 表现出慢速增长(负异速生长)。生长拐点按照Snik等[18]的方法确定: 若幂函数生长模型中含有不同生长阶段, 则以拐点分开, 不同生长阶段由不同生长方程表达: y=a1xb1, y=a2xb2。对b1、b2进行t检验, 检测2个b值是否存在差异显著性, 同时对b1、b2是否等于1做t检验。应用SPSS 17.0统计软件对模型进行非线性回归参数拟合, 并应用EXCEL 2010进行分段回归模型拟合, 以决定系数R2最大和残差平方和最小为曲线拟合标准, 用SPSS 17.0统计软件进行显著性检测。
2. 结果
2.1 斑鰶胚后发育的形态特征
根据形态特征、器官发育的变化情况[19], 可将斑鰶的早期发育过程划分为仔鱼期(0—43d)和稚鱼期(44—55d)。其中仔鱼期根据卵黄囊的消失与否以及尾椎的弯曲变化程度又可分为卵黄囊期仔鱼(0—6d)、尾椎弯曲前期(7—16d)、尾椎弯曲期(17—20d)、尾椎弯曲后期(21—43d) 4个时期(图 3)。
卵黄囊期(从孵化出膜至卵黄囊消失, 0—6d, 图版I-1—3) 初孵仔鱼刚出膜的仔鱼全长(3.18±0.52) mm, 腹部下方具有椭圆形的大卵黄囊, 长径长(0.72±0.09) mm, 短径长(0.55±0.06) mm, 具有一个油球(图版II-1-OB), 位于腹侧卵黄囊下缘, 油球半径长(0.07±0.01) mm, 体色透明, 色素较少, 只有头顶及背部可见少量黑色素点, 未开口, 可见明显的心跳(图版II-1-H), 可观察到52个肌节。初孵仔鱼多浮在水面, 在受到外界惊动时便迅速窜游(图版I-1)。
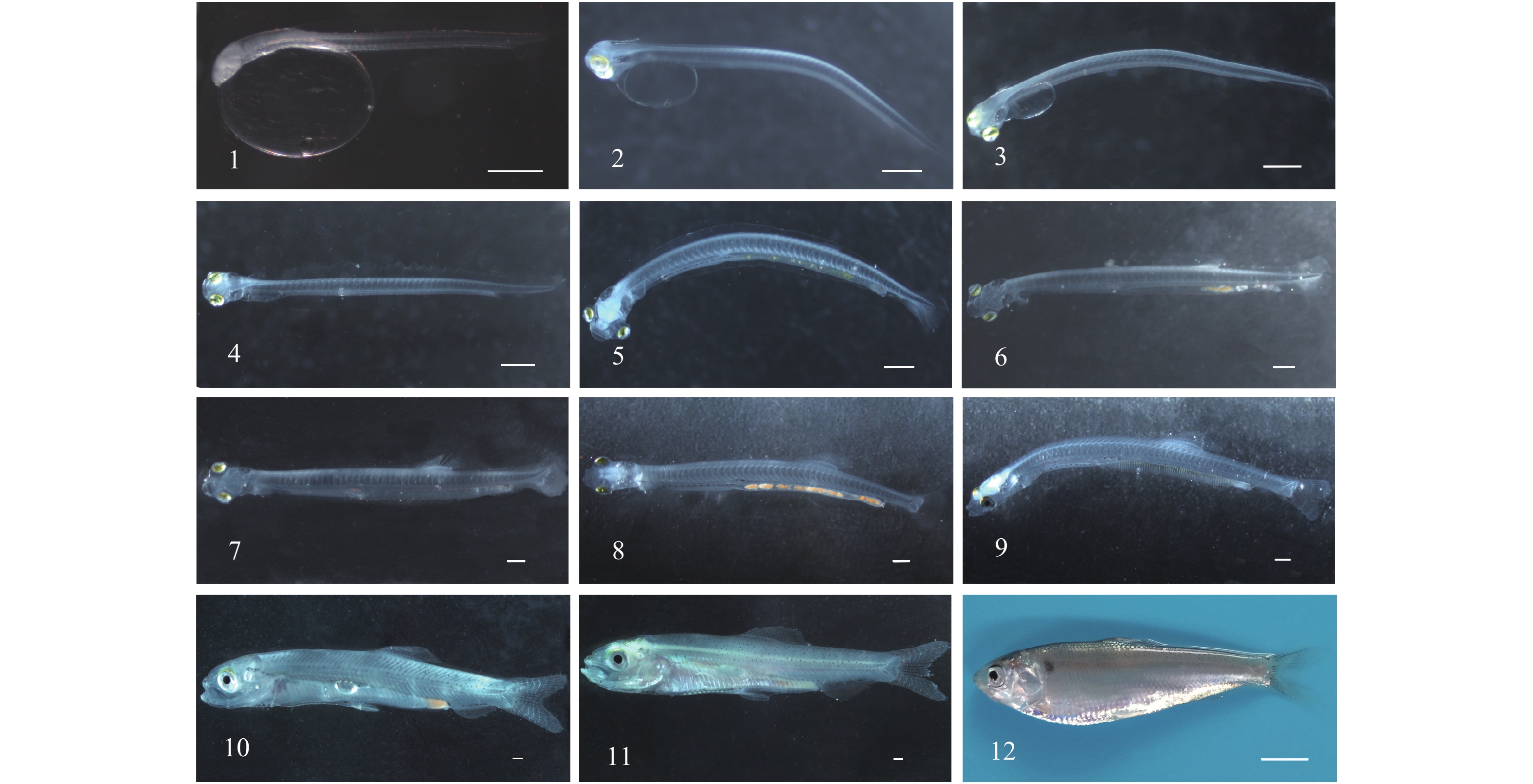
![]() 图版 I 斑鰶仔、稚鱼形态发育1. 初孵仔鱼; 2. 1日龄仔鱼; 3. 3日龄仔鱼; 4. 6日龄仔鱼; 5. 9日龄仔鱼; 6. 14日龄仔鱼; 7. 17日龄仔鱼; 8. 19日龄仔鱼; 9. 23日龄仔鱼; 10. 39日龄仔鱼; 11. 44日龄稚鱼; 12. 55日龄稚鱼。图1—11标尺为500 μm; 图12标尺为5 mm图版 I. Morphological development on larvae and juveniles of K. punctatus1. Newly hatched larva; 2. 1-day old larva; 3. 3-day old larva; 4. 6-day old larva; 5. 9-day old larva; 6. 14-day old larva; 7. 17-day old larva; 8. 19-day old larva; 9. 23-day old larva; 10. 39-day old larva; 11. 44-day old juvenile; 12. 55-day old juvenile. Bar=500 μm for figure 1—11; Bar=5 mm for figure 12
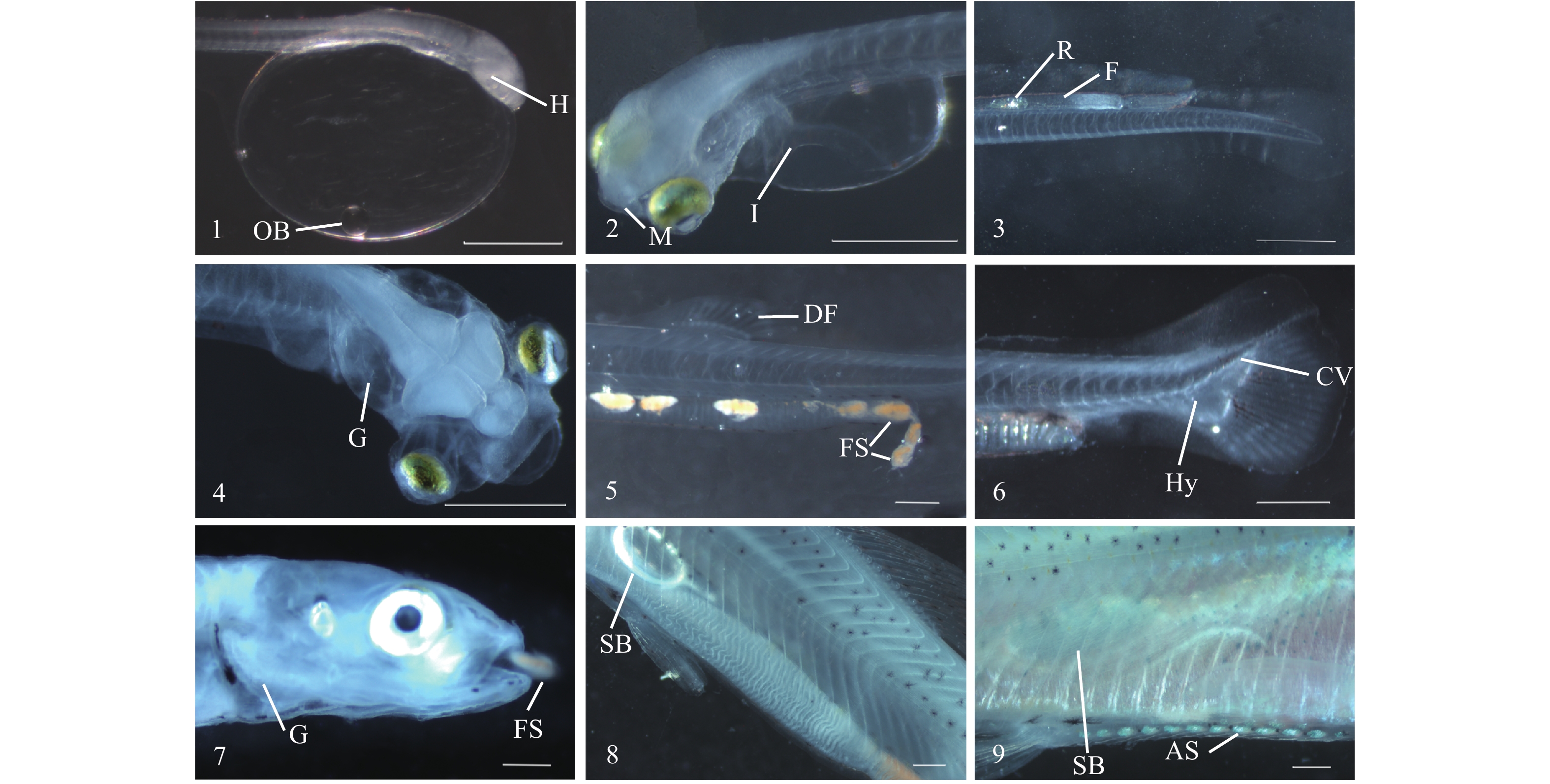
图版 I 斑鰶仔、稚鱼形态发育1. 初孵仔鱼; 2. 1日龄仔鱼; 3. 3日龄仔鱼; 4. 6日龄仔鱼; 5. 9日龄仔鱼; 6. 14日龄仔鱼; 7. 17日龄仔鱼; 8. 19日龄仔鱼; 9. 23日龄仔鱼; 10. 39日龄仔鱼; 11. 44日龄稚鱼; 12. 55日龄稚鱼。图1—11标尺为500 μm; 图12标尺为5 mm图版 I. Morphological development on larvae and juveniles of K. punctatus1. Newly hatched larva; 2. 1-day old larva; 3. 3-day old larva; 4. 6-day old larva; 5. 9-day old larva; 6. 14-day old larva; 7. 17-day old larva; 8. 19-day old larva; 9. 23-day old larva; 10. 39-day old larva; 11. 44-day old juvenile; 12. 55-day old juvenile. Bar=500 μm for figure 1—11; Bar=5 mm for figure 12![]() 图版 II 斑鰶仔、稚鱼局部特征1. 初孵仔鱼的卵黄囊; 2. 3日龄仔鱼的头部; 3. 6日龄仔鱼的消化道; 4. 9日龄仔鱼的头部; 5. 14日龄仔鱼的消化道; 6. 17日龄仔鱼的尾部; 7. 23日龄仔鱼的头部; 8. 39日龄仔鱼的躯干; 9. 44日龄稚鱼的腹部; OB: 油球; H: 心脏; M: 口; I: 肠道; F: 肠壁褶皱; R: 轮虫; G: 鳃丝; FS: 丰年虫; DF: 背鳍; Hy: 尾下骨; CV: 尾椎骨; SB: 鱼鳔; AS: 棱鳞; 图中标尺500 μm图版 II. Local character on larvae and juveniles of K. punctatus1. The yolk sac of the newly hatched larva; 2. Head of 3-day old larva; 3. Intestine of 6-day old larva; 4. Head of 9-day old larva; 5. Intestine of 14-day old larva; 6. Caudal fin of 17-day old larva; 7. Head of 23-day old larva; 8. Trunk of 39-day old larva; 9. Abdomen of 44-day old juvenile. OB: oil ball; H: heart; M: mouth; I: Intestine; F: Intestinal wall fold; R: rotifer; G: gill; FS: fairy shrimp; DF: dorsal fin; Hy: hypural; CV: caudal vertebra; SB: swim bladder; AS: abdominal scale; Bar=500 μm
图版 II 斑鰶仔、稚鱼局部特征1. 初孵仔鱼的卵黄囊; 2. 3日龄仔鱼的头部; 3. 6日龄仔鱼的消化道; 4. 9日龄仔鱼的头部; 5. 14日龄仔鱼的消化道; 6. 17日龄仔鱼的尾部; 7. 23日龄仔鱼的头部; 8. 39日龄仔鱼的躯干; 9. 44日龄稚鱼的腹部; OB: 油球; H: 心脏; M: 口; I: 肠道; F: 肠壁褶皱; R: 轮虫; G: 鳃丝; FS: 丰年虫; DF: 背鳍; Hy: 尾下骨; CV: 尾椎骨; SB: 鱼鳔; AS: 棱鳞; 图中标尺500 μm图版 II. Local character on larvae and juveniles of K. punctatus1. The yolk sac of the newly hatched larva; 2. Head of 3-day old larva; 3. Intestine of 6-day old larva; 4. Head of 9-day old larva; 5. Intestine of 14-day old larva; 6. Caudal fin of 17-day old larva; 7. Head of 23-day old larva; 8. Trunk of 39-day old larva; 9. Abdomen of 44-day old juvenile. OB: oil ball; H: heart; M: mouth; I: Intestine; F: Intestinal wall fold; R: rotifer; G: gill; FS: fairy shrimp; DF: dorsal fin; Hy: hypural; CV: caudal vertebra; SB: swim bladder; AS: abdominal scale; Bar=500 μm1日龄仔鱼全长(3.82±0.71) mm, 卵黄囊显著缩小, 长径长(0.49±0.05) mm, 短径长(0.32±0.02) mm, 油球也明显缩小, 仍位于腹侧卵黄囊下缘; 仔鱼体型较为细长, 头部离开卵黄囊, 卵黄囊上方长出胸鳍, 背部黑色素消失, 眼睛呈淡黄色, 所有鳍褶均明显增大。此时期的仔鱼游泳能力较弱, 多悬浮于水体的中层, 体质较差的仔鱼沉到池底容易死亡(图版I-2)。
3日龄仔鱼全长(5.04±0.68) mm, 卵黄囊进一步缩小, 头部快速发育, 眼睛较为突出, 呈黄绿色, 口开始张开(图版II-2-M), 肠道已有分化(图版II-2-I)。胸鳍变大呈明显的扇状薄片, 尾部鳍褶较为明显(图版I-3)。
6日龄仔鱼全长(5.64±0.82) mm, 卵黄囊已完全消失, 眼睛的色素增加, 晶体变黑, 听囊增大, 口已完全张开, 消化系统进一步发育完善, 消化道可以分为食道和肠道两部分, 肠道可见肠壁褶皱(图版II-3-F), 可以吞食轮虫(图版II-3-R), 消化道两侧的黑色素增多。在仔鱼的背部和腹部各有一道皮褶, 可以沿水平方向波浪形摆动, 起到游泳的作用, 仔鱼就呈柔软的波浪形弯曲向前游动, 这种波浪形弯曲的游泳方式一直保持到偶鳍形成之前。斑鰶后期仔鱼的这种独特的游动方式也是区分其他仔鱼的重要特征之一。
尾椎弯曲前期(卵黄囊消失至尾椎末端呈直线形, 7—16d) 9日龄仔鱼全长(6.64±0.79) mm, 下颌长度长于上颌, 鳃部结构开始发育, 鳃弧后缘出现鳃丝(图版II-4-G)。除尾部第1至第16肌节的皮褶增长形成尾鳍原基外, 第17肌节至肛门部的背腹部皮褶均退化。在第29至第34肌节处出现背鳍原基, 食道两侧排列呈虚线状的黑色素段, 肠道透明, 可以清晰地看到食物残渣在肠道内蠕动(图版I-5)。
14日龄仔鱼全长(10.35±1.06) mm, 背鳍和尾鳍的鳍条出现, 背鳍发育较快, 出现7—8个鳍条, 尾鳍上生长出黑色素, 臀鳍原基出现, 位于肛门后, 肠管上黑色素显著, 此时期主要摄食丰年虫无节幼体(图版II-5-FS), 肠道较为发达, 经常可见消化道内充塞着多只无节幼体, 而且在靠近肛门排泄孔可见未完全消化的无节幼体(图版I-6)。
尾椎弯曲期(尾椎末端开始向上弯曲, 尾下骨出现, 后缘与尾椎倾斜, 17—20d) 17日龄仔鱼全长(12.15±1.28) mm, 肌节数51—52, 尾椎末端明显开始向上弯曲(图版II-6-CV), 出现尾下骨(图版II-6-Hy), 尾鳍鳍条数17, 此时尾鳍的尾形还是圆形尾, 肠管上黑色素进一步加深, 此时期还是以摄食丰年虫无节幼体为主, 虽然肠管进一步发育, 但是消化吸收功能还不完善, 仍有部分未完全消化的无节幼体直接排除从肛门排出(图版I-7)。
19日龄仔鱼全长(13.25±1.82) mm, 背鳍鳍条数为13, 尾鳍鳍条数18, 尾鳍鳍条开始分节, 尾鳍的中央第9—11鳍条开始比其他鳍条短, 尾鳍边缘形成内凹, 肠道结构和功能进一步完善, 消化和吸收食物的能力加强(图版I-8)。
尾椎弯曲后期(尾下骨与尾椎末端垂直, 21—43d) 23日龄仔鱼全长(14.82±1.15) mm, 鳃丝形成鳃小叶(图版II-7-G), 背鳍进一步发育, 形成14枚鳍条。尾鳍后缘分叉呈典型的叉形尾, 每一叶呈扇形, 尾鳍黑色素较多, 尾鳍鳍条数20条。鱼鳔已经形成, 位于食道上方, 鳔有两条管, 前管往前, 后管同食道末端相连。鱼体透明, 在仔鱼腹部肠道管周围的体色为淡黄色。此时期仔鱼在水体的中上层呈曲线型快速游动(图版I-9)。
39日龄仔鱼全长(25.10±2.43) mm, 鱼鳔充气明显可见(图版II-8-SB), 位于腹鳍上方的消化管和脊柱之间。体侧黑色素增加明显, 身体的透明度降低, 消化管变的膨大, 增加消化和吸收食物空间, 后期仔鱼的奇、偶鳍逐渐发育完善, 运动能力也明显加强, 弯曲的波浪形游动方式也逐渐改变, 游泳速度加快。随着游泳能力的加强, 摄取食物的能力和需求也明显增加(图版I-10)。
稚鱼期(各鳍条数与成鱼相同, 棱鳞开始出现至全身被鳞, 44—55d) 44日龄稚鱼全长(27.01±3.27) mm, 奇偶鳍的鳍条数已与成鱼完全一致, 棱鳞开始出现(图版II-9-AS), 首先是从胸鳍处开始形成, 逐渐向后发展。棱鳞开始形成时, 胸鳍附近的腹侧开始出现原始的鳞片, 体表的黑色素增加, 身体已不透明, 外观呈银白色, 内脏器官也逐渐看不清楚(图版I-11)。
2.2 斑鰶仔、稚鱼全长与日龄的关系
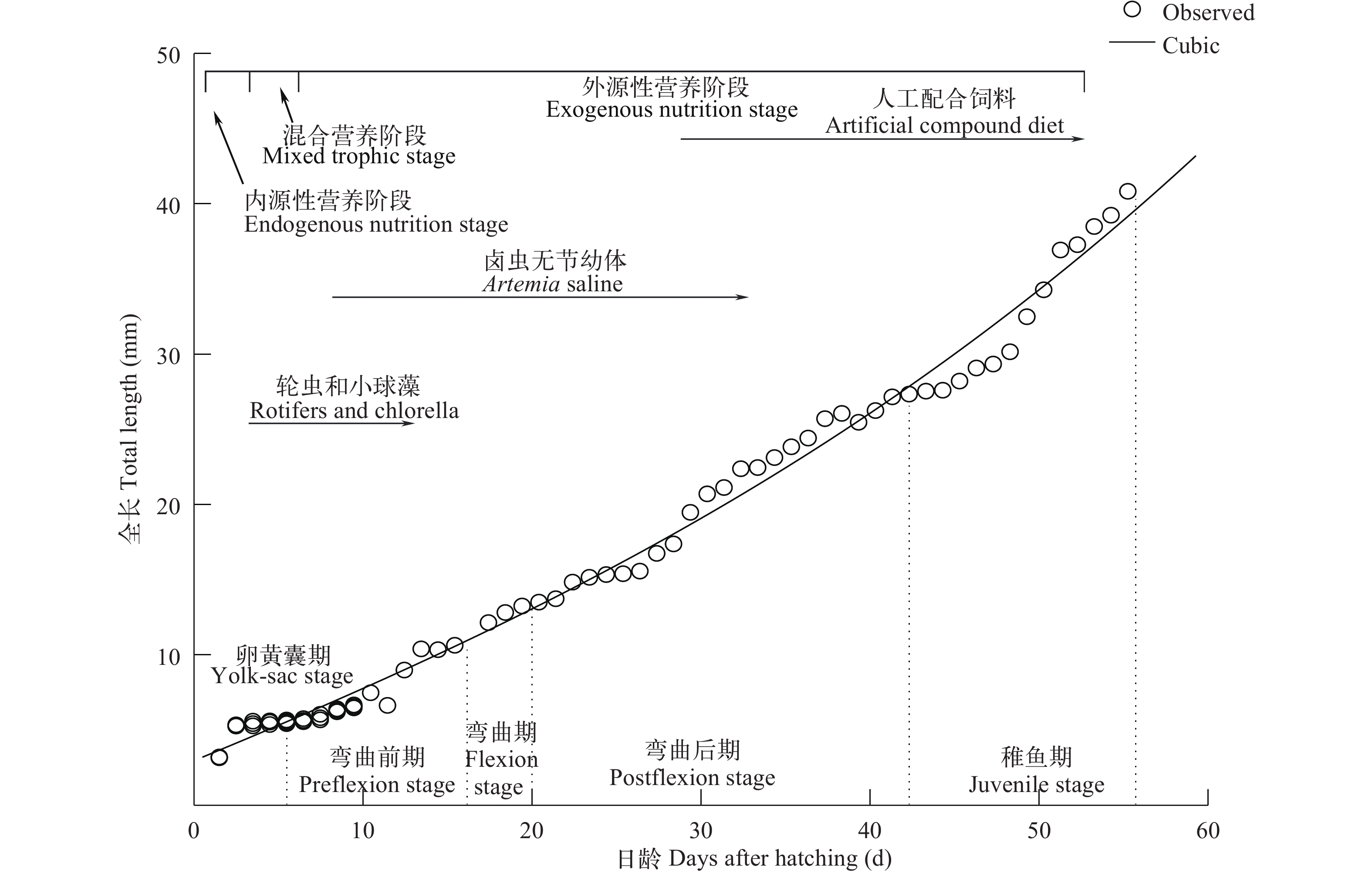
斑鰶3日龄仔鱼即开口摄食, 为混合营养阶段, 采用投喂“轮虫+小球藻”, 投放小球藻可以确保轮虫营养充足, 投喂轮虫密度为6—9 ind./mL, 确保开口顺利; 8日龄投喂卤虫无节幼体, 投喂前进行营养强化, 投放卤虫无节幼体的密度为8—10 ind./mL; 30日龄稚鱼开始驯化投喂人工配合饲料, 这是生物饵料向配合饲料转化的关键期, 驯化1周左右即可完全实现食性的转化, 可以全部投喂人工配合饲料。在斑鰶仔、稚鱼发育到30日龄食性转化的关键期, 替换两种饵料的前后一定要有交叉重叠时间, 使斑鰶能够逐渐适应食性转变的过程。
以SPSS 17.0软件中的Curve Estimation 对全长和日龄的关系进行曲线模型拟合分析及参数估计(表 1), 以R2=0.995值最大的Cubic函数作为最佳模型。
表 1 斑鰶全长与日龄的模型分析与参数估计Table 1. The summary and parameters between total length and age in days of K. punctatus模型Model 模型分析Model summary 参数估计Parameter estimate R2 F df1 df2 Sig. Constant b1 b2 b3 线性模型Linear 0.974 3081.99 1 251 0.000 1.067 0.684 对数曲线模型Logarithmic 0.740 230.184 1 251 0.000 –10.191 10.380 反函数曲线模型Inverse 0.277 31.048 1 251 0.000 23.111 –35.594 二次曲线模型Quadratic 0.993 5960.771 2 250 0.000 3.915 0.315 0.006 三次曲线模型Cubic 0.995 4924.753 3 249 0.000 2.860 0.559 –0.004 0 复合曲线模型Compound 0.962 2072.284 1 251 0.000 4.873 1.041 幂函数模型Power 0.920 930.665 1 251 0.000 2.042 0.687 S曲线模型S curve model 0.465 70.454 1 251 0.000 2.967 –2.736 增长曲线模型Growth 0.962 2072.284 1 251 0.000 1.584 0.040 指数曲线模型Exponential 0.962 2072.284 1 251 0.000 4.873 0.040 逻辑斯蒂曲线模型Logistic 0.986 5540.437 1 251 0.000 0.219 0.943 函数关系式为: y=–0.004x2+0.559x+2.86。
斑鰶初孵仔鱼的全长为(3.18±0.54) mm, 经55d生长, 全长达到(40.83±2.46) mm。
2.3 斑鰶仔、稚鱼发育过程中各功能器官的异速生长
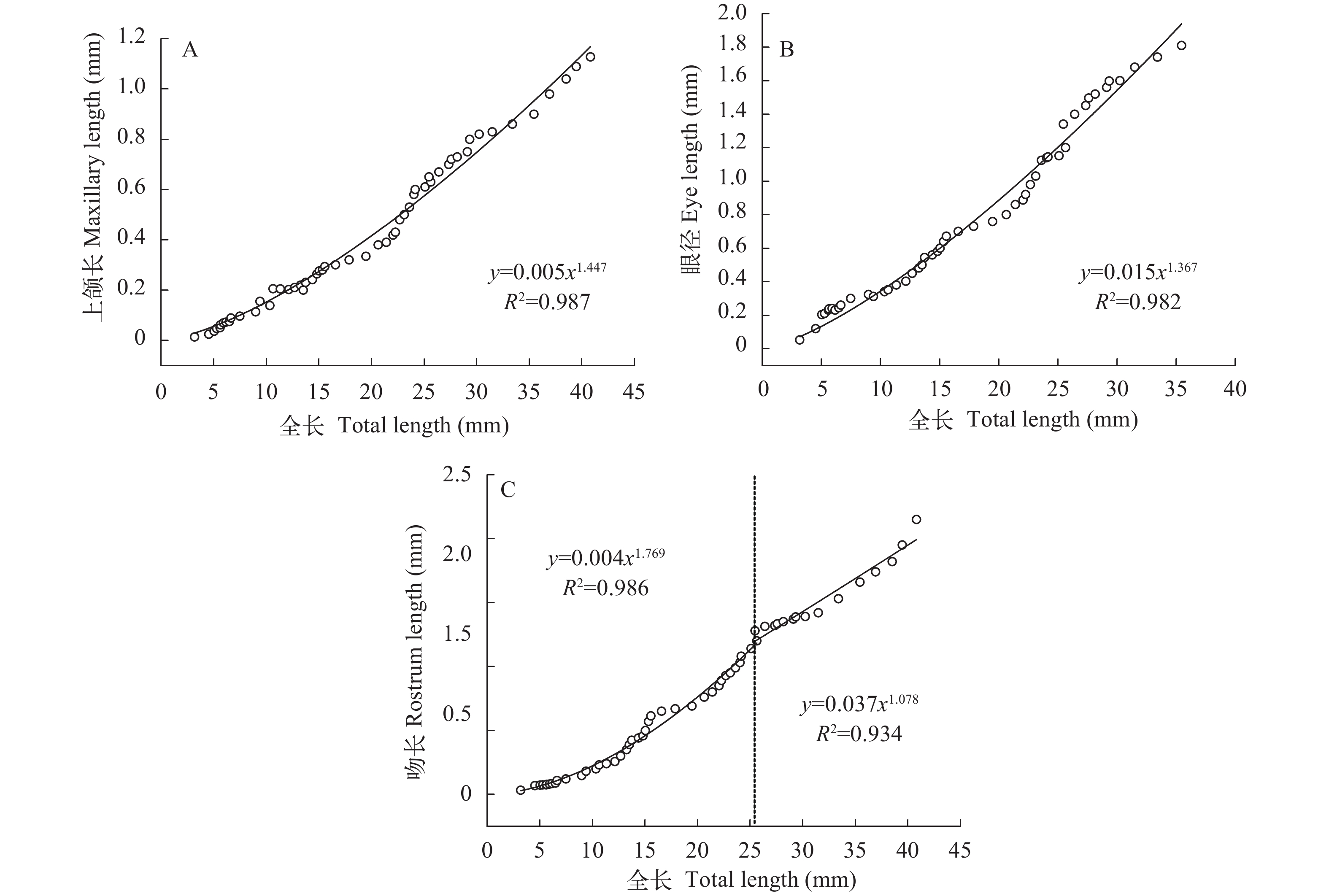
斑鰶头部器官异速生长 上颌长(图 4A)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.456, 显著大于1 (P<0.05), 即上颌长相对于全长表现出正异速生长。
眼径(图 4B)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.367, 显著大于1 (P<0.05), 即眼径相对于全长表现出正异速生长。
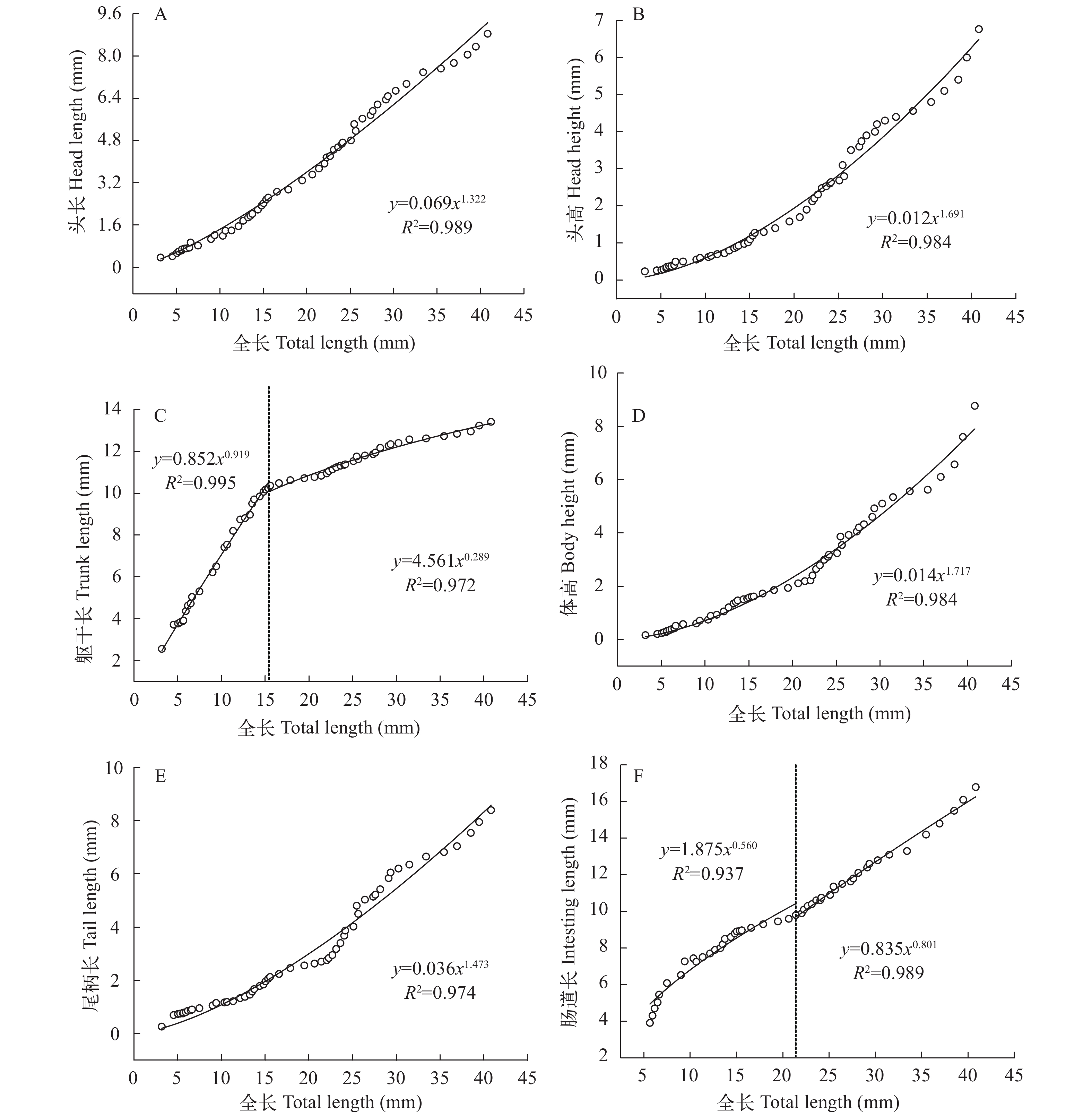
吻长(图 4C)的生长拐点出现在42日龄(TL: 25.47 mm), 异速生长指数b1=1.768, 显著大于1 (P<0.05), 吻长相对于全长呈正异速生长; 自42日龄到55日龄(TL: 40.83 mm), 异速生长指数b2=1.078 (P>0.05), 表现为等速生长。
斑鰶身体部分的异速生长 头长(图 5A)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.322, 显著大于1 (P<0.05), 即头长相对于全长表现出正异速生长。
头高(图 5B)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.690, 显著大于1 (P<0.05), 即头高相对于全长表现出正异速生长。
躯干长(图 5C)的生长拐点出现在24日龄(TL: 15.57 mm), 异速生长指数b1=0.918 (P>0.05), 躯干长相对于全长呈等速生长; 自24日龄到55日龄(TL: 40.83 mm), 异速生长指数b2=0.289, 显著小于1 (P<0.05), 即躯干长相对于全长表现出负异速生长。
体高(图 5D)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.717, 显著大于1 (P<0.05), 即体高相对于全长表现出正异速生长。
尾柄长(图 5E)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.473, 显著大于1 (P<0.05), 即尾柄长相对于全长表现出正异速生长。
肠道长(图 5F)的生长拐点出现在31日龄(TL: 21.41 mm), 异速生长指数b1=0.560, 显著小于1 (P<0.05), 肠道长相对于全长呈现负异速生长; 自31日龄到55日龄(TL: 40.83 mm), 异速生长指数b2=0.865 (P>0.05), 即肠道长相对于全长表现出等速生长。
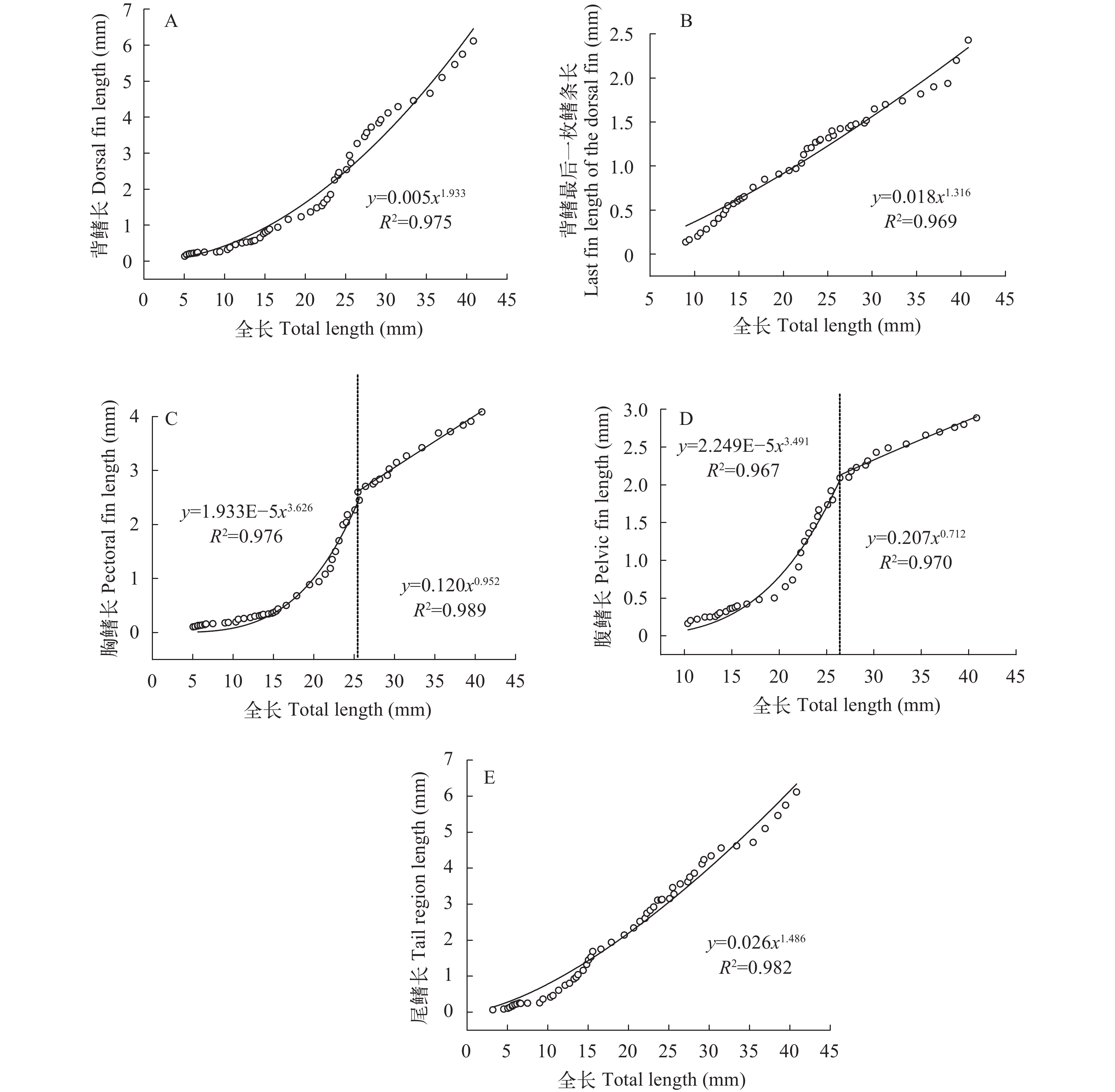
斑鰶游泳器官的异速生长 背鳍长(图 6A)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.933, 显著大于1 (P<0.05), 即背鳍长相对于全长表现出正异速生长。
背鳍最后一枚鳍条长(图 6B)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.316, 显著大于1 (P<0.05), 即背鳍最后一枚鳍条长相对于全长表现出正异速生长。
胸鳍长(图 6C)的生长拐点出现在41日龄(TL: 25.47 mm), 异速生长指数b1=3.626, 显著大于1 (P<0.05), 胸鳍长相对于全长呈正异速生长; 自41日龄到55日龄(TL: 40.83 mm), 异速生长指数b2=0.952 (P>0.05), 表现为等速生长。
腹鳍长(图 6D)的生长拐点出现在42日龄(TL: 26.41 mm), 异速生长指数b1=3.491, 显著大于1 (P<0.05), 胸鳍长相对于全长呈正异速生长; 自42日龄到55日龄(TL: 40.83 mm), 异速生长指数b2=0.711, 显著小于1 (P<0.05), 即腹鳍长相对于全长表现出负异速生长。
尾鳍长(图 6E)的生长自初孵仔鱼(TL: 3.18 mm)到55日龄(TL: 40.83 mm)并没有出现生长拐点, 异速生长指数b=1.486, 显著大于1 (P<0.05), 即尾鳍长相对于全长表现出正异速生长。
3. 讨论
仔稚鱼阶段是鱼类整个生命过程中高死亡率的阶段, 也是其对外界压力和环境因子最敏感的时期[20]。由于受到自身生理因素和环境因子的共同作用, 早期鱼类的各关键器官在形态学、生理学等方面都会经历显著的变化[21]。通常对早期存活发挥重要作用的器官被选择性地优先发育, 使其在适应环境方面表现出最佳状态, 并且这种优先发育的状态会随生长发育阶段的不同而做出改变。斑鰶仔、稚鱼的发育符合硬骨鱼类发育的一般规律, 即刚孵化出的初孵仔鱼许多功能器官多处于未分化或发育不完善阶段[22], 随后早期仔鱼的形态学变化和重要功能器官的分化比稚鱼更明显。在仔鱼阶段, 通常与呼吸、摄食、消化和游泳能力相关的功能器官优先发育[23], 这些变化会影响到仔鱼对外界环境的适应性。
3.1 斑鰶仔、稚鱼阶段的发育特征
在本试验中, 斑鰶仔、稚鱼全长随日龄的变化符合Cubic函数式, 生长曲线呈“S”型。斑鰶初孵仔鱼全长3.18 mm, 与鲱科鱼类中国鲥(Macrura reevesii, 2.75 mm)相似[24], 但是短于美洲鲥(Alosa sapidissima)[15]和太平洋鲱鱼(Clupea pallasi)[25]; 初孵仔鱼的消化道和肛门已分化出来, 这与美洲鲥一致。不同于太平洋鲱鱼[25], 斑鰶初孵仔鱼具有油球, 这与陈大刚等[26]观察到的结果一致。斑鰶仔鱼出膜第3天开口, 开始摄食轮虫, 此时营养物质一部分来自于卵黄囊, 但仍处于混合营养阶段。随着生长发育卵黄囊被逐渐吸收, 直至第6天完全消失, 此后开始营外源性营养阶段。而美洲鲥[12]和中国鲥[21]的卵黄囊消失的时间分别为第4天和第5天, 卵黄囊消失时间的不同可能是由于培育水温的不同。鳔的作用与鱼类的游泳和摄食密切相关, 是仔鱼开始开口摄食的标志之一[27]。斑鰶在孵出第3天便开口摄食, 然而鱼鳔在孵化后20d左右才充气, 位于肠道上方, 具有2条管, 前段与听囊相连, 后端与食道末端相连。这说明鳔在斑鰶早期仔鱼阶段并没有起到辅助摄食和运动的作用, 而斑鰶的运动和摄食主要依靠鳍褶带动身体的蛇形摆动。本文中斑鰶仔鱼在20℃水温下, 在第44天棱鳞出现进入稚鱼阶段, 而陈大刚等[26]在(18—28)℃培育的仔鱼在第28天出现棱鳞进入稚鱼期, 说明温度变化对斑鰶仔、稚的发育影响较大。斑鰶易于区分其他鲱科鱼类的形态特征出现的时间较晚, 如背鳍后端鳍条延长的鳍条、棱鳞的出现以及鳃盖后方的半月形黑斑均没有在仔鱼阶段发育, 这为在自然海域区分斑鰶与青鳞鱼仔稚带来了困难[16]。孔立波等[28]用数学方法对早期发育阶段的形态进行比较, 分析结果表明卵黄吸收殆尽前后体形均有较大变化。结合本研究在实验室条件下观察到6日龄斑鰶仔鱼卵黄已完全吸收, 消化道可区分为食道和肠道, 出现肠壁褶皱; 仔鱼背部和腹部各有皮褶, 采用典型的水平波浪形摆动游泳方式, 这些形态特征和游泳方式可为青鳞鱼和斑鰶仔鱼的鉴定提供借鉴。
3.2 头部器官异速生长
头长和头高都对鱼头部容积大小密切相关, 而容积的大小又直接决定着头内部其他器官的发育, 如口咽腔、鳃及脑的发育可能受到头部大小的限制[18]。而这些器官大小又直接影响到消化、呼吸及神经系统的能力。在鱼类的长期进化过程中, 大部分鱼类的头部都具最优先发育的现象[23, 29, 30]。斑鰶的仔、稚鱼发育也符合上述规律, 即头长和头高均与全长呈正异速生长, 通过头部的形态观察也发现口咽腔和鳃的快速发育。
仔、稚鱼的摄食能力与口的发育和完善密切相关。Gisbert等[31]研究表明西伯利亚鲟(Acipenser baeri)仔鱼的吻长在开口后还会继续快速生长, 进一步完善口部的发育, 促进仔鱼主动摄食和获得充足能量的能力。日本七鳃鳗(Lampetra japonica)仔鱼期吻长的快速生长为口笠的发育提供必要空间, 为仔鱼开启外源营养期的摄食外源食物具有重要意义[32]。在本研究中, 斑鰶仔、稚鱼上颌长一直处于快速生长阶段, 而吻长拐点出现在42日龄, 拐点前处于快速生长期, 口的快速发育是为了摄食更大的食物, 而在拐点之后则表现出等速生长, 口部的快速生长以便摄食不同大小食物[33, 34]; 可见, 斑鰶在42日龄即将发育为稚鱼期时, 口的发育已经较为完善, 为满足稚鱼的快速生长提供摄食较大规格的食物提供可能。视觉对仔、稚鱼的摄食和躲避敌害的捕食发挥重要作用。斑鰶生活在海洋中上层, 其眼径的发育表现出快速生长状态, 这与许氏平鲉(Sebastes schlegelii)[35]、西伯利亚鲟[31]及条石鲷(Oplegnathus fasciatus)[30]的早期发育一致, 但不同于生活在暗环境和被动摄食方式的日本七鳃鳗仔鱼(其眼径为等速生长)[32]。
3.3 躯干部分异速生长
多数鱼类仔、稚鱼的相对生长表现为“U”型模式, 即头长和尾长呈正异速生长, 而躯干长呈负异速生长[17]。本实验研究发现, 斑鰶的仔、稚鱼各功能器官的发育也表现为“U”型生长模式, 其头长和尾柄长在整个仔、稚鱼阶段(0—55日龄)均处于正异速生长状态, 而躯干长在24日龄之前处于等速生长阶段, 之后转变成慢速生长阶段。这可能有利于控制鱼体全长, 减少头尾之间的距离, 保证仔、稚鱼的运动更协调, 对于游泳器官尚未完善的初期仔、稚鱼具有重要的生理学意义。而体高的生长保持快速生长状态, 这可能与仔、稚鱼内部器官的发育有关。在23日龄时, 斑鰶的鱼鳔开始充气, 位于食道上方, 鱼鳔充气时需要更大的空间, 因此体高的快速生长为脏器的快速发育提供充足的生长空间。这与在许氏平鲉[36]和条石鲷[30]中观察到的结果一致。仔、稚鱼的快速生长与消化系统功能的完善和运动捕食能力的提升息息相关[37], 与这些系统相关的各器官快速发育, 如消化道结构与功能的划分、胃膨胀、肠道的盘曲折叠、鳔的充气等, 都会促进体高的快速生长[36, 38]。
一般动物增加能量摄入的方式有2种[39]: (1)提高摄食频率, 无胃结构的鱼类单次摄入的食物量有限, 因此提高摄食频率能显著增加能量摄入; (2)改变摄食食物的种类, 如通过食性转化来获得更高能量的需求[40]。在本实验中, 斑鰶肠道长的生长拐点出现在31日龄, 由慢速生长转变为等速生长。肠道生长的加快提高了斑鰶的消化吸收能力, 为生命体生长提供更多的营养来源。虽然本研究并未发现肠道长的快速生长阶段, 但笔者认为在斑鰶仔、稚鱼阶段, 主要采用提高摄食频率和食性转化的策略来获得充足能量。斑鰶在仔、稚鱼阶段幽门胃并不发达, 不具备大量储存和消化食物的功能, 故主要摄食轮虫、丰年虫无节幼体及桡足类[16]; 而斑鰶成鱼具有发达的幽门胃肌肉[7], 而以摄食沉积碎屑[7]为主。这在对斑鰶仔、稚鱼肠道形态的观察中也得到了验证: 肠道内始终积聚丰年虫无节幼体, 肛门排泄孔可见未完全消化的无节幼体, 这说明斑鰶在此阶段通过不断进食来增加能量摄入。此外, 鱼类的摄食策略会随着消化系统的发育和食性的转化而改变。
肠道长的生长拐点出现在31日龄, 在31日龄之前肠道生长表现出慢速生长, 我们在30日龄开始驯化投喂人工配合饲料。这意味着在人工开始投喂配合饲料之前肠道结构发育较慢, 消化与吸收的功能尚未发育完善, 这与观察到未消化完全的丰年虫无节幼体就直接排出体外的现象相一致。在31至55日龄肠道生长表现出等速生长, 在31日龄前后正是斑鰶由摄食生物饵料向配合饲料转化的时期。这提示我们在斑鰶食性转化的关键期, 其消化系统得到快速发育, 要及时进行饵料种类的变化, 以保障其快速生长的能量需求。
3.4 游泳器官的异速生长
鱼类的游泳器官主要有胸鳍、腹鳍及尾鳍等鱼鳍, 其中最重要的是尾鳍[30]。鱼鳍的生长发育对提高仔、稚鱼的游泳能力、摄食能力及躲避敌害能力具有重要作用[35]。在初孵仔鱼阶段的游泳能力主要靠尾部摆动和鳍褶的平衡作用, 但游泳能力相对较弱[18], 随着仔鱼的生长鳍褶逐渐退化消失[41], 胸鳍的出现大大提高了仔鱼的游泳和平衡能力[23]。本研究观察发现, 斑鰶刚出膜时具有鳍褶, 但是不明显, 游泳能力较弱, 初孵仔鱼多静止浮于水面。胸鳍和沿背部分布的鳍褶在1日龄时便快速生长发育, 这表明胸鳍和鳍褶是斑鰶仔鱼最早期的重要游泳器官。在游泳器官发育不完善的早期仔鱼的阶段, 斑鰶依靠鳍褶左右摆动, 形成独特的“蛇形”运动方式, 这种独特的游动方式也是区分其他仔鱼的重要特征之一。直至9日龄时, 鳍褶开始退化消失, 背鳍、尾鳍原基开始形成, 极大地提高了仔鱼的游泳能力, 这对仔鱼的摄食和躲避敌害等生态作用具有重要意义[35]。
综上所述, 斑鰶存在异速生长现象, 主要优先发育与摄食、运动和呼吸代谢有关的器官。
-
图 1 斑鰶形态特征测量直观图
1. 头长; 2. 头高; 3.上颌长; 4. 眼径; 5. 吻长; 6. 躯干长; 7. 体高; 8. 尾柄长; 9. 背鳍长; 10. 背鳍最后一枚鳍条长; 11. 胸鳍长; 12. 尾鳍; 13. 全长
Figure 1. Illustration measurement for K. punctatus
1. Head length; 2. Head height; 3. Upper jaw length; 4. Eye diameter; 5. Rostrum; 6. Trunk length; 7. Body height; 8. Caudal peduncle length; 9. Dorsal fin length; 10. The last dorsal fin long; 11. Pectoral length; 12. Tail fin length; 13. Total length
图版 I 斑鰶仔、稚鱼形态发育
1. 初孵仔鱼; 2. 1日龄仔鱼; 3. 3日龄仔鱼; 4. 6日龄仔鱼; 5. 9日龄仔鱼; 6. 14日龄仔鱼; 7. 17日龄仔鱼; 8. 19日龄仔鱼; 9. 23日龄仔鱼; 10. 39日龄仔鱼; 11. 44日龄稚鱼; 12. 55日龄稚鱼。图1—11标尺为500 μm; 图12标尺为5 mm
图版 I. Morphological development on larvae and juveniles of K. punctatus
1. Newly hatched larva; 2. 1-day old larva; 3. 3-day old larva; 4. 6-day old larva; 5. 9-day old larva; 6. 14-day old larva; 7. 17-day old larva; 8. 19-day old larva; 9. 23-day old larva; 10. 39-day old larva; 11. 44-day old juvenile; 12. 55-day old juvenile. Bar=500 μm for figure 1—11; Bar=5 mm for figure 12
图版 II 斑鰶仔、稚鱼局部特征
1. 初孵仔鱼的卵黄囊; 2. 3日龄仔鱼的头部; 3. 6日龄仔鱼的消化道; 4. 9日龄仔鱼的头部; 5. 14日龄仔鱼的消化道; 6. 17日龄仔鱼的尾部; 7. 23日龄仔鱼的头部; 8. 39日龄仔鱼的躯干; 9. 44日龄稚鱼的腹部; OB: 油球; H: 心脏; M: 口; I: 肠道; F: 肠壁褶皱; R: 轮虫; G: 鳃丝; FS: 丰年虫; DF: 背鳍; Hy: 尾下骨; CV: 尾椎骨; SB: 鱼鳔; AS: 棱鳞; 图中标尺500 μm
图版 II. Local character on larvae and juveniles of K. punctatus
1. The yolk sac of the newly hatched larva; 2. Head of 3-day old larva; 3. Intestine of 6-day old larva; 4. Head of 9-day old larva; 5. Intestine of 14-day old larva; 6. Caudal fin of 17-day old larva; 7. Head of 23-day old larva; 8. Trunk of 39-day old larva; 9. Abdomen of 44-day old juvenile. OB: oil ball; H: heart; M: mouth; I: Intestine; F: Intestinal wall fold; R: rotifer; G: gill; FS: fairy shrimp; DF: dorsal fin; Hy: hypural; CV: caudal vertebra; SB: swim bladder; AS: abdominal scale; Bar=500 μm
表 1 斑鰶全长与日龄的模型分析与参数估计
Table 1 The summary and parameters between total length and age in days of K. punctatus
模型Model 模型分析Model summary 参数估计Parameter estimate R2 F df1 df2 Sig. Constant b1 b2 b3 线性模型Linear 0.974 3081.99 1 251 0.000 1.067 0.684 对数曲线模型Logarithmic 0.740 230.184 1 251 0.000 –10.191 10.380 反函数曲线模型Inverse 0.277 31.048 1 251 0.000 23.111 –35.594 二次曲线模型Quadratic 0.993 5960.771 2 250 0.000 3.915 0.315 0.006 三次曲线模型Cubic 0.995 4924.753 3 249 0.000 2.860 0.559 –0.004 0 复合曲线模型Compound 0.962 2072.284 1 251 0.000 4.873 1.041 幂函数模型Power 0.920 930.665 1 251 0.000 2.042 0.687 S曲线模型S curve model 0.465 70.454 1 251 0.000 2.967 –2.736 增长曲线模型Growth 0.962 2072.284 1 251 0.000 1.584 0.040 指数曲线模型Exponential 0.962 2072.284 1 251 0.000 4.873 0.040 逻辑斯蒂曲线模型Logistic 0.986 5540.437 1 251 0.000 0.219 0.943 -
[1] Niklas K J. Plant Allometry: The Scaling of Plant Form and Process [M]. Chicago: University of Chicago Press. 1994, 274—290
[2] 王雨福, 肖志忠, 刘清华, 等. 斑石鲷早期发育的异速生长模式. 海洋科学, 2016, 40(5): 43—48 doi: 10.11759//hykx20141216005 Wang Y F, Xiao Z Z, Liu Q H, et al. Allometric growth pattern during early ontogeny of spotted knifejaw (Oplegnathus punctatus) [J]. Marine Sciences, 2016, 40(5): 43—48 doi: 10.11759//hykx20141216005
[3] 雷霁霖. 中国海水养殖大产业架构的战略思考. 中国水产科学, 2010, 17(3): 600—609 Lei Q L. Strategy consideration for industry construction of Chinese marine culture [J]. Journal of Fishery Science of China, 2010, 17(3): 600—609
[4] 丁福红, 毛守康, 雷霁霖, 等. 我国植物食性海水鱼类养殖发展前景. 海洋科学, 2014, 38(11): 131—137 doi: 10.11759/hykx20140424001 Ding F H, Mao S K, Lei Q L, et al. Prospect of herbivorous fish in marine aquaculture of China [J]. Marine Sciences, 2014, 38(11): 131—137 doi: 10.11759/hykx20140424001
[5] 金彬明, 张其永. 福建省东山岛西埔湾港养斑鰶的繁殖生物学. 水产学报, 1993, 17(2): 126—136 Jin B M, Zhang Q Y. The reproductive biology of gizzard shad Clupanodon punctatus in xipu bay [J]. Journal of Fisheries of China, 1993, 17(2): 126—136
[6] 肖月娟, 李润丰, 郑立红. 斑鰶鱼肉蛋白质氨基酸组成分析及评价. 营养学报, 2011, 33(4): 413—415 Xiao Y J, Li R F, Zheng L H. Analysis and evaluation of protein and amino acids composition of fish meat for Clupanodom punchtatus[J]. Acta Nutrimenta Sinica, 2011, 33(4): 413—415
[7] 郭学武, 唐启升, 孙耀, 等. 斑鰶的摄食与生态转换效率. 海洋水产研究, 1999, 20(2): 17—25 Guo X W, Tang Q S, Sun Y, et al. The consumption and ecological conversion efficiency of dotted gizzard shad (Clupanodon punctatus) [J]. Marine Fisheries Research, 1999, 20(2): 17—25
[8] 吕末晓. 鮻、斑鰶幼鱼食物组成及其与环境浮游植物的关系研究. 硕士学位论文, 上海海洋大学, 上海. 2016 Lü M X. Study on the diet composition of juvenile of Liza haematocheila and Konosirus punctatus and itsrelationship with ambient phytoplankton [D]. Shanghai Ocean University, Shanghai. 2016
[9] 陈大刚. 黄渤海渔业生态学. 北京: 海洋出版社. 1991, 179—183 Chen D G. Fishery ecology in the Yellow Sea and Bohai Sea [M]. Beijing: Ocean Press. 1991, 179—183
[10] 李渊, 张丽艳, 王良明, 等. 台湾海峡斑鰶群体遗传学研究. 应用海洋学学报, 2016, 35(4): 522—528 doi: 10.3969/J.ISSN.2095-4972.2016.04.009 Li Y, Zhang L Y, Wang L M, et al. Population genetics of Konosirus punctatus in Taiwan Strait [J]. Journal of Applied Oceanography, 2016, 35(4): 522—528 doi: 10.3969/J.ISSN.2095-4972.2016.04.009
[11] 肖月娟, 李润丰, 郑立红, 等. 斑鰶鱼蛋白控制酶解及其酶解物抗氧化活性研究. 中国食品学报, 2010, 10(5): 91—97 doi: 10.3969/j.issn.1009-7848.2010.05.014 Xiao Y J, Li R F, Zheng L H, et al. Studies on controlled enzymolysis of Clupanodom punchtatus protein and antioxidant activity of its hydrolysates [J]. Journal of Chinese Institute of Food Science and Technology, 2010, 10(5): 91—97 doi: 10.3969/j.issn.1009-7848.2010.05.014
[12] Yamada U, Tokimura M, Horikawa H, et al. Fishes and fisheries of the East China and Yellow Seas [M]. Kanagawa: Tokai University Press. 2007, 206-211
[13] Katsumi M, Yukio N. On the spawning season and spawning ground of the Japanese gizzard shad konosirus punctatus in Lake Hamana [J]. Bulletin of the Japanese of Scientific Fisheries, 1974, 40(1): 35—42 doi: 10.2331/suisan.40.35
[14] 高小强, 洪磊, 刘志峰, 等. 美洲鲥仔稚鱼异速生长模式研究. 水生生物学报, 2015, 39(3): 638—644 doi: 10.7541/2015.85 Gao X Q, Hong L, Liu Z F, et al. The study of allometric growth pattern of American shad larvae and juvenile (Alosa sapidissima) [J]. Acta Hydrobiologica Sinica, 2015, 39(3): 638—644 doi: 10.7541/2015.85
[15] 张呈祥, 徐钢春, 徐跑, 等. 美洲鲥仔、稚、幼鱼的形态发育与生长特征. 中国水产科学, 2010, 17(6): 1227—1235 Zhang C X, Xu G C, Xu P, et al. Morphological development andgrowth of American shad (Alosa sapidissima) at larvae, fry and juvenile stages [J]. Journal of Fishery Sciences of China, 2010, 17(6): 1227—1235
[16] 陈真然, 张孝威. 斑鰶卵子和仔、稚、幼鱼的形态特征. 海洋与湖沼, 1965, 7(3): 205—219 Chen Z R, Zhang X W. A description of the morphological characters of the eggs, larvae and young of Clupanodon punctatus [J]. Oceanologia et Limnologia Sinica, 1965, 7(3): 205—219
[17] Fuiman L A. Growth gradients in fish larvae [J]. Journal of Fish Biology, 1983, 23(1): 117—123 doi: 10.1111/jfb.1983.23.issue-1
[18] Snik G M J, Osse J W M. Larval growth patterns in Cyprinus carpio and Clarias gariepinus with attention to the finfold [J]. Journal of Fish Biology, 1997, 50(6): 1339—1352
[19] 杨培民, 骆小年, 金广海, 等. 鸭绿江唇䱻仔、稚鱼形态发育与早期生长. 水生生物学报, 2014, 38(1): 1—9 Yang P M, Luo X N, Jin G H, et al. Morphological development and early growth on larvae and juveniles of Hemibarbus labeo in Yalü River [J]. Acta Hydrobiologica Sinica, 2014, 38(1): 1—9
[20] 殷名称. 鱼类早期生活史研究与其进展. 水产学报, 1991, 15(4): 348—358 Yin M C. Advance and studies of early life history of fish [J]. Journal of Fisheries of China, 1991, 15(4): 348—358
[21] Gluckmann I, Huriaux F, Focant B, et al. Postembryonic development of the cephalic skeleton in Dicentrarchus labrax (Pisces, Perciformes, Serranidae) [J]. Bulletin of Marine Science, 1999, 65(1): 11—36
[22] Choo C K, Liew H C. Morphological development and allometric growth patterns in the juvenile seahorse Hippocampus kuda Bleeker [J]. Journal of Fish Biology, 2006, 69(2): 426—445 doi: 10.1111/jfb.2006.69.issue-2
[23] 马境, 章龙珍, 庄平, 等. 施氏鲟仔鱼发育及异速生长模型. 应用生态学报, 2007, 18(12): 2875—2882 Ma J, Zhang L Z, Zhuang P, et al. Development and allometric growth patters of larval Acipenser schrenckii [J]. Chinese Journal of Applied Ecology, 2007, 18(12): 2875—2882
[24] 邱顺林, 刘琳, 王鸿泰. 鲥鱼的早期发育. 水产学报, 1987, 11(1): 45—52 Qiu S L, Liu L, Wang H T. Observation on the early development of reeves shad [J]. Journal of Fisheries of China, 1987, 11(1): 45—52
[25] 杨东莱, 吴光宗. 太平洋鲱鱼的胚胎发育及初孵仔鱼的形态. 水产学报, 1982, 6(1): 25—31 Yang D L, Wu G Z. Observations on the embryonic development and pre-larvae of pacific herring [J]. Journal of Fisheries of China, 1982, 6(1): 25—31
[26] 陈大刚, 刘国祥, 董广君, 等. 斑鰶人工繁殖与鱼苗培育的初步试验. 动物学报, 1977, 23(1): 22—29 Chen D G, Liu G X, Dong G J, et al. Preliminary experiments on the artificial breeding and fry rearing of gizzardshads Clupanodon punctatus (Temminck et Schlegel, 1846) [J]. Current Zoology, 1977, 23(1): 22—29
[27] 门强, 雷霁霖, 武云飞. 鳔器官的发育对人工培育鱼苗的影响. 海洋水产研究, 2003, 24(1): 80—84 Men Q, Lei J L, Wu Y F. Influence of abnormal development of swimbladder on the larvae rearing of marine fish [J]. Marine Fishery Research, 2003, 24(1): 80—84
[28] 孔立波, 孙继仁, 杨东莱, 等. 渤海湾青鳞鱼和斑鰶两种鱼卵及仔鱼的比较研究. 海洋与湖沼, 1996, 27(2): 169—178 doi: 10.3321/j.issn:0029-814X.1996.02.009 Kong L B, Sun J R, Yang D L, et al. Comparison research on eggs and larvae of Harengula zunasi bleeker and Clupanodon punctatus in Bohai bay [J]. Oceanologia et Limnologia Sinica, 1996, 27(2): 169—178 doi: 10.3321/j.issn:0029-814X.1996.02.009
[29] Peña R, Dumas S. Development and allometric growth patterns during early larval stages of the spotted sand bass Paralabrax maculatofasciatus (Percoidei: Serranidae) [J]. Scientia Marina, 2009, 73(1): 183—189
[30] 何滔, 肖志忠, 刘清华, 等. 条石鲷早期发育阶段的生长模式. 水产学报, 2012, 36(8): 1242—1248 He T, Xiao Z Z, Liu Q H, et al. Allometric growth in rock bream larvae (Oplegnathus fasciatus Temminck et Schlegel 1844) [J]. Journal of Fisheries of China, 2012, 36(8): 1242—1248
[31] Gisbert E. Early development and allometric growth patterns in Siberian sturgeon and their ecological significance [J]. Journal of Fish Biology, 1999, 54(4): 852—862 doi: 10.1111/jfb.1999.54.issue-4
[32] 李军, 韩英伦, 徐磊, 等. 日本七鳃鳗胚胎发育及卵黄囊期仔鱼的异速生长. 水生生物学报, 2017, 41(6): 1207—1217 doi: 10.7541/2017.150 Li J, Han Y L, Xu L, et al. Embryological stages and allometric growth during yolksac larvae of Lampetra japonica (Martens) [J]. Acta Hydrobiologica Sinica, 2017, 41(6): 1207—1217 doi: 10.7541/2017.150
[33] 庄平, 宋超, 章龙珍, 等. 全人工繁殖西伯利亚鲟仔、稚鱼发育的异速生长. 生态学杂志, 2009, 28(4): 681—687 Zhuang P, Song C, Zhang L Z, et al. Allometric growth of artificial bred Siberian sturgeon Acipenser baeri larvae and juveniles [J]. Chinese Journal of Ecology, 2009, 28(4): 681—687
[34] Osse J W M, Boogaart J G M V, Snik G M J V, et al. Priorities during early growth of fish larvae [J]. Aquaculture, 1997, 155(14): 249—258
[35] 席丹, 张秀梅, 吕红健, 等. 许氏平鲉早期异速生长模式的研究. 中国海洋大学学报(自然科学版), 2014, 44(12): 28—34 Xi D, Zhang X M, Lü H J, et al. Studies on early allometric growth pattern of black rockfish Sebastes schlegelii [J]. Periodical of Ocean University of China (
Natural Science ) , 2014, 44(12): 28—34 [36] 席丹. 许氏平鲉(Sebastes schlegelii)早期发育生长模式与自残行为研究. 硕士学位论文, 中国海洋大学, 青岛. 2014 Xi D. Growth pattern and cannibalism in black rockfish (Sebastes schlegelii) during early development stage [D]. Ocean University of China, Qingdao. 2014
[37] 程大川, 马振华, 江世贵. 红鳍笛鲷仔、稚鱼异速生长. 水生生物学报, 2017, 41(1): 206—213 doi: 10.7541/2017.26 Cheng D C, Ma Z H, Jiang S G, et al. Allometric growth in larval and juvenile crimson snapper Lutjanus erythopterus [J]. Acta Hydrobiologica Sinica, 2017, 41(1): 206—213 doi: 10.7541/2017.26
[38] 单秀娟, 窦硕增. 鮸鱼(Miichthys miiuy)仔、稚鱼发育生长方式及其生态学意义. 海洋与湖沼, 2009, 40(6): 714—719 doi: 10.3321/j.issn:0029-814X.2009.06.007 Shan X J, Dou S Z. Allometric growth of croaker Miichthys miiuy larvae and juveniles and its ecological implication [J]. Oceanologia et Limnologia Sinica, 2009, 40(6): 714—719 doi: 10.3321/j.issn:0029-814X.2009.06.007
[39] 张臣, 曾燏, 彭艳, 等. 嘉陵江下游蛇肠道形态结构及其异速生长模式. 水产学报, 2018, 42(4): 503—512 Zhang C, Zeng Y, Peng Y, et al. Morphological structure and allometric growth pattern of Saurogobio dabryi intestine in the lower reaches of Jialing River [J]. Journal of Fisheries of China, 2018, 42(4): 503—512
[40] 高亚辉, 傅万里, 徐境波, 等. 真鲷早期仔鱼食性转变研究. 台湾海峡, 2000, 19(3): 344—349 doi: 10.3969/j.issn.1000-8160.2000.03.014 Gao Y H, Fu W L, Xu J B, et al. Feeding switching of Pagrosomus major earlier larvae [J]. Journal of Oceanography in Taiwan Strait, 2000, 19(3): 344—349 doi: 10.3969/j.issn.1000-8160.2000.03.014
[41] 宋洪建, 刘伟, 王继隆, 等. 大麻哈鱼卵黄囊期仔鱼异速生长及其生态学意义. 水生生物学报, 2013, 37(2): 329—335 doi: 10.7541/2013.23 Song H J, Liu W, Wang J L, et al. Allometric growth during yolk-sac larvae of chum salmon (Oncorhynchus keta Walabaum) and consequent ecological significance [J]. Acta Hydrobiological Sinica, 2013, 37(2): 329—335 doi: 10.7541/2013.23
-
期刊类型引用(5)
1. 文浩,徐林,吴志强,黄亮亮,高明慧,宋琦亮,何佳洋,刘昊,孙扬言. 西江伍氏华吸鳅仔、稚鱼的异速生长研究. 四川动物. 2024(02): 146-153 .  百度学术
百度学术
2. 谢敏,吴浩,宋锐,向劲,周洁,李鸿,曾国清,李绍明,向建国. 芙蓉鲤鲫仔稚鱼的异速生长模式及饥饿不可逆点研究. 南方农业学报. 2023(04): 1253-1262 .  百度学术
百度学术
3. 韩莎,胡炜,李成林,李文文,赵斌,曲红霞,王琦,姚琳琳. 刺参选育群体F_5代形态性状与体质量相关性及通径分析. 浙江大学学报(农业与生命科学版). 2022(05): 653-659+670 .  百度学术
百度学术
4. 韩莎,胡炜,李成林,吴鹏,赵洪友,赵斌,姚琳琳. 12月龄刺参养殖群体生长特性的研究. 西北农林科技大学学报(自然科学版). 2021(11): 31-37+52 .  百度学术
百度学术
5. 周胜杰,胡静,杨蕊,杨其彬,马振华. 三斑海马早期发育观察. 南方农业学报. 2021(08): 2302-2310 .  百度学术
百度学术
其他类型引用(4)




 下载:
下载: