ANALYSIS OF THE PYRAMIDING EFFECT OF GROWTH-RELATED MOLECULAR MARKERS IN LARGEMOUTH BASS (MICROPTERUS SALMOIDES)
-
摘要: 为了解与大口黑鲈(Micropterus salmoides)生长性状相关分子标记优势基因型的聚合效果, 研究选择先前已获得的13个与生长性状相关的分子标记, 位于PCK1、HSBP1、FOXO3b、MYH、HSC70-1、CTSB、HBP、POU1F1、PACAP、IGF-I、ghrelin、ApoproteinA1和MSTN基因上。在40尾亲本群体中对各标记的基因型进行检测, 选择可聚合优势基因型最多的2对亲本分别构建家系。在9月龄时, 从2个家系子代中分别采集305尾和266尾个体进行生长性状测量和各标记的基因型分析。家系1子代个体中含生长相关优势基因型的数量为0—6个, 对应的个体数依次为8、26、75、74、76、35和11, 对应的平均体质量依次为185.03、196.46、198.73、212.59、222.66、235.54和261.27 g。家系2子代个体中含生长相关优势基因型的数量为1—6个, 对应的平均体质量依次为184.43、213.17、243.77、249.98、252.11和266.00 g。个体中生长相关优势基因型聚合数量多少与生长性状呈正相关, 提示通过对生长相关优势基因型进行聚合可获得生长性状优良的大口黑鲈, 为大口黑鲈分子标记辅助育种的应用提供科学依据。Abstract: Growth traits are controlled by multiple genes to cause minor phenotypic effect. To understand the pyra-miding effect of advantage genotypes of growth-related molecular markers in largemouth bass (Micropterus salmoides), thirteen molecular markers related to growth traits were selected obtained on previous studies, which were loca-ted in PCK1, HSBP1, FOXO3b, MYH, HSC70-1, CTSB, HBP, POU1F1, PACAP, IGF-I, ghrelin, ApoproteinA and MSTN. The genotype of each marker in forty largemouth bass parents was analyzed and 2 families were constructed basing on pyramiding advantage genotypes. 305 and 266 individuals were sampled randomly from second filial generation of two families at nine month old, respectively. The results showed that the number of advantage genotypes was various in all offspring of family 1 with the number of individuals of each group 8, 26, 75, 74, 76, 35 and 11, respecti-vely. The average weight of advantage genotypes group was 185.03, 196.46, 198.73, 212.59, 222.66, 235.54 and 261.27 g, respectively. In the offspring of family 2, the number of advantage genotype ranged from one to six with the average weight of 184.43, 213.17, 243.77, 249.98, 252.11 and 266.00 g, respectively. Correlation analysis showed that the pyramiding number of advantage genotype was correlated with growth traits. Our results present evidence to improve the growth trait of largemouth bass by utilizing the limited advantage genotypes. This study provided scientific basis for the application of molecular marker assisted breeding in largemouth bass.
-
Keywords:
- Micropterus salmoides /
- Growth traits /
- Molecular marker /
- Advantage genotype /
- Pyramiding
-
多基因聚合育种是目前分子标记辅助育种研究中常用的技术方法, 通过传统的回交、杂交、复交等手段将多个有利的基因聚合到一起, 将分散在不同亲本中的优异基因聚合到同一基因组, 从而达到育种目标的一种手段[1—3]。多基因聚合育种在农作物、畜牧、家禽等中均有报道。在棉花(Gossypium spp)纤维品质性状改良研究中, 聚合与纤维长度相关的QTL个数越多, 单株平均纤维长度值越大[4]。9个与小麦(Triticeae dumort)株高相关联位点的聚合效果分析显示, 株高与主效基因型的聚合数目多少呈正相关性[5]。将多个控制水稻(Oryza sativa)不同经济性状的基因或QTL同时杂交导入亲本受体, 实现多个位点有利等位基因的聚合, 改良了水稻多个重要的经济性状[6—8]。刘轩等[9]在促卵泡素β亚基(FSHβ)、雌激素受体(ESR)和促乳素受体基因上各找出1个与藏猪(Sus scrofa)繁殖性状相关的标记, 这3个标记的优势基因型聚合效应高于单个优势基因型效应。陈克飞等[10]发现ESR和FSHβ基因的聚合基因型BBBB母猪比ABAA母猪总产仔数平均每胎多1.85—3.01头, 产活仔数平均每胎多2.0—3.0头。但是目前关于水产动物多基因聚合研究的报道还比较少。孙效文等[11]对镜鲤(Cyprinus carpio)优势基因型进行聚合及培育优良品系, 发现优势基因型平均数量为1.7的群体在生长速度方面比平均数量为0.7的群体显著提高。
大口黑鲈(Micropterus salmoides)是一种从北美洲引进的广温性鱼类, 在分类学上隶属鲈形目(Perciformes)太阳鱼科(Cehtrachidae)。因大口黑鲈肉质鲜美, 不含肌间剌, 适合高密度养殖和活鱼长途运输, 深受养殖者和消费者欢迎。大口黑鲈在我国大多数省份都有规模化养殖, 年产量超35×107 kg[12], 成为我国重要的淡水养殖经济品种之一。生长性状是决定生产成本和经济效益的重要经济性状, 它是由众多基因调控的数量性状, 遗传基础复杂, 单个基因对性状的影响有限[13]。针对大口黑鲈养殖产业中出现的种质退化现象, 笔者所在的实验室开展了大口黑鲈生长性状的分子标记辅助育种研究, 利用候选基因方法从磷酸烯醇丙酮酸羧激酶(PCK1)[13]、热休克因子结合蛋白(HSBP1)[13]、FOXO3b[13]、肌球蛋白重链基因(MYH)[14]、热休克蛋白HSC70-1(待发表)、组织蛋白酶B(CTSB)[15]、高密度脂蛋白结合蛋白(HBP)[16]、垂体特异性转录因子(POU1F1)[17]、垂体腺苷酸环化激酶多肽(PACAP)[18]、胰岛素样生长因子-1 (IGF-I)[19]、生长激素促分泌素基因(ghrelin)[20]、载脂蛋白A1 (ApoproteinA1)[21]和肌肉生长抑制素(MSTN)[22]基因中分别筛选到1个与生长性状相关的SNP标记。在这些工作基础之上, 本研究构建了用于与生长相关标记聚合研究的家系, 分析了家系中与生长性状相关的优势基因型的聚合对表型性状的影响效果, 以期为大口黑鲈生长性状相关分子标记在育种中的应用提供理论参考。
1. 材料与方法
1.1 大口黑鲈亲本的挑选和养殖
实验用大口黑鲈亲鱼来自于佛山市三水白金水产种苗有限公司, 从养殖池塘中挑选40尾大口黑鲈“优鲈1号”体质量大的个体(828.5±21.2) g, 其中雌鱼和雄鱼各20尾, 在水泥池中进行养殖, 将每尾鱼注射电子芯片标记, 并剪取少量尾鳍, 用于提取DNA和基因型分析。
1.2 生长性状相关分子标记的选择
本实验室先前所获得的13个与生长性状相关的分子标记(Unigene33789_All-658、Unigene19479_All-121、CL1689.Contig2_All-302、C-6811T、C-821G、C-598G、G-2782T、C-18T、A-2282C、S1、A-642C、A-489C和C-1453T)分别位于PCK1[13]、HSBP1[13]、FOXO3b[13]、MYH[14]、HSC70-1、CTSB[15]、HBP[16]、POU1F1[17]、PACAP[18]、IGF-I[19]、ghrelin[20]、ApoproteinA1[21]和MSTN[22]基因上, 这些标记均与体质量显著相关。上述13个分子标记在进行基因型检测中所用的引物序列见表 1, 所有引物由上海捷瑞生物工程有限公司合成, 其中S1位点扩增用的引物采用荧光进行标记。
表 1 所用大口黑鲈生长性状相关分子标记的相关信息Table 1. Primers of growth-associated markers of largemouth bass分子标记
Molecular marker标记所处基因名称
Gene name引物Primer (5′-3′) 延伸引物Extension primer(5′-3′) S1[ATTTTT(GTTT/-)TT] IGF-1 ACAAACCTTAATGTACTG
TTCTTCCTCTATGTCACCA-2282C PACAPA ATCACTGTCTGTCACTTCATG
ATAAATGATTCATTTGCAGCCTGTTTTTATCTCTCTCTCTCT Unigene33789_All-658 PCK CTGAAAGAGGAGCAATTCTC TTTTTTTTTTTTTTTTGAGCAATTCTCCTCTGATAATT Unigene19479_All-121 HSBP1 GGAGGACAGCATTTATAATAG
GTTATGAGTGGTCTTATCAAAGAACACCTCAGGTTTTTAGTCTA C-6811T MYH AGAGGAGGAAATCAAGGTATC
GCTCCTCCTCATACTGCTCCCTCAAATTACCGTGAATTCAG CL1689.Contig2_All-302 FOXO3b GTACAGACATGTATGATGCAG
CATGGTGTAAATCTGATCCAGTTTTTTTTTACAGAAAATCCAGTAAACAGAC C-598G CTSB TGAGTCATATGAAAGCATTAC
ACACTTTGTGTATGCAGGCTGTTTTTTTTATGCATTGGGGTGTGTCTCCAC G-2782T HBP CTCTTACAAGACGGCCTACTC
GAACAGGCACTGCTGGTACAGCTTTTTTTTTTTTTTAGCTCTTTGGGCTGCGGCTCAG C-18T POU1F1 GCAGCAGGGAGAAAGACAAG
CGTACACTGAAGGTTGACGTTAAAGTAAGACTAAACACAAGA A-642C Ghrelin AACCCTTGAATAAACATAACGT
TGGAGGAACCATATCGATGTCATC-1453T MSTN TACATCAAAGGAATAGTCTGC
ATGTCTCATAGTGGGTCAAATTTTTTTTTTGGAWATACTAAGGTAAACTTTC C-821G HSC70-1 TGAAGCCTACCTCGGAAAAGT
AGCATCCTTAGTGGCCTGGCGCTTACTTAGCATAGCTCTGGACA A-489C ApoproteinA1 ATTGAGCCCATCGTCACAGA
AGCAGCCAGTGTCTTCAGATTTTTTTTTTTTTTTTTTTTTTTTGTCTGAAGGCCAAGGTGGAGCC 1.3 基因组DNA的提取
取保存的亲本和子代鳍条样品, 按照天根生化科技(北京)有限公司试剂盒中的操作方法提取组织DNA, 用0.7%琼脂糖凝胶电泳和分光光度计检测提取的DNA质量和浓度, 保存于–20℃备用。
1.4 生长相关标记的基因型检测
Ghrelin基因上的SNP标记采用直接测序法进行基因型的分析, 对大口黑鲈基因组进行PCR扩增, PCR扩增反应总体积为50 μL: 10 μL 5×Taq PCR master mix, 上下游引物各1 μL (20 μmol/L), 模板DNA 1 μL (50—80 ng), 加ddH2O至50 μL。PCR扩增程序: 94℃预变性3min; 32个循环(94℃, 30s; 55℃, 1min; 72℃, 30s); 72℃再延伸7min, 委托上海捷瑞生物工程有限公司完成测序。IGF-I基因上的片段缺失突变位点直接用STR基因分型技术分析基因型, PCR扩增程序同上, 采用毛细管电泳检测PCR扩增产物, 根据片段大小差异区分标记的基因型, 委托上海捷瑞生物工程有限公司完成基因型分析。采用SNaPshot SNP分型方法分析其余位点在每尾大口黑鲈中的基因型, 委托上海捷瑞生物工程有限公司完成, 实验流程为: 根据SNP标记两端附近序列设计扩增引物(表 1), 然后对每个样品的DNA进行多重PCR扩增。PCR扩增后取3 μL PCR产物用ExoⅠ和FastAP纯化, 主要是用ExoⅠ去除反应产物中的剩余引物, 用FastAP去除反应中剩余的DNTP, 在37℃条件下15min, 80℃高温灭活ExoⅠ和FastAP酶15min。根据ABI公司提供的SNaPshot试剂盒, 用延伸引物进行延伸反应, 使用ABI公司的PRISM 3730测序仪进行基因分型。
1.5 家系构建及子代培育
首先分析每个生长关联标记在40尾大口黑鲈亲本中的基因型分布情况, 然后依据家系2个亲本中至少一个为杂合子基因型且子代中存在优势基因型, 选择可聚合优势基因型最多的2对亲本分别进行繁殖及构建全同胞家系。采用人工注射催产剂的方法促进产卵, 收取的受精卵分别放置于室内孵化箱孵化。孵化时水温为23℃左右, 将孵出的鱼苗都转入到面积为12 m2的水泥池中进行饲养。开始投喂小型浮游动物和丰年虫, 每天投喂多次, 其后改投喂红虫, 等长至2.5 cm左右时驯食投喂饲料, 每天投喂3次。当大口黑鲈为3月龄时, 将2个家系分别采用CWT标记, 然后放入佛山市三水白金水产种苗有限公司的1333.3 m2养殖池塘中进行养殖。9月龄时, 从2个家系子代中分别采集305尾和266尾实验鱼进行体质量、全长、体高、头长和尾柄长测量, 同时采集少量尾鳍, 用于提取DNA和基因型分析。
1.6 数据统计分析
分别对家系1中305尾子代和家系2中266尾子代中的7个标记的基因型进行检测, 然后统计家系子代个体中所含有的优势基因型的数量, 根据所含优势基因型数量的不同将大口黑鲈进行分组, 分析不同数量的优势基因型组在生长性状上的差异, 不同组间生长性状均值比较采用SPSS19软件中的One-way ANOVA进行分析。
2. 结果
2.1 大口黑鲈亲本基因型分析
为尽可能聚合优势基因型, 依据亲本基因型的分布情况, 构建了家系1和家系2用于生长标记聚合效果分析。2个家系的亲本的基因型见表 2。对于家系1, 因为S1、CL1689.Contig2_All-302、G-2782T、C-821G位点在亲本中的基因型为纯合子, 所产生的子代全部为杂合基因型, Unigene33789_All-658和C-18T位点在家系子代中都不存在优势基因型, 在后续分析中仅统计其余7个分子标记在305尾子代中的优势基因型分布情况。对于家系2, 因为Unigene19479_All-121、S1、C-6811T、C-821G位点在亲本中的基因型为纯合子, 所产生的子代全部为相同的基因型, C-598G和C-18T位点在家系子代中都不存在优势基因型, 在后续分析中仅统计其余7个分子标记在266尾子代中的优势基因型分布情况。
表 2 13个生长标记在大口黑鲈亲本中的基因型Table 2. Genotype of 13 growth related markers in largemouth bass parents分子标记Molecular marker 优势基因型Dominant genotype 家系1亲本Parents of family 1 家系2亲本Parents of family 2 雄Male 雌Female 雄Male 雌Female S1 AA AA BB BB BB A-2282C AC CC AC AC AC Unigene33789_All-658 CC AA AC CC AC Unigene19479_All-121 AA AG AG AA AA C-6811T CC GG CG CC CC CL1689.Contig2_All-302 AA GG GG AG AG C-598G CC CT CT CT TT G-2782T TT TT GG GT GT C-18T CC TT CT CT TT A-642C AC CC AC CC AC C-1453T CT CT CT CT CT C-821G CC GG GG GG CC A-489C AC AC CC AC AC 2.2 大口黑鲈子代中优势基因型的频率分布
对家系1中305尾大口黑鲈子代中的优势基因型进行了统计, 单个个体中聚合优势基因型的数量最多为6个, 一共有11尾, 在子代中所占的比例为3.6%, 8个个体不含有优势基因型, 所占比例为2.6%。A-642C位点中优势基因型在子代群体中的分布频率最高, 为55.4%, C-598G位点对应的优势基因型的分布频率最低, 为26.9% (表 3)。
表 3 不同标记中优势基因型的分布频率Table 3. The frequency of dominant genotypes of different markers分子标记
Molecular marker优势基因型频率Frequency of dominant genotypes (%) 家系1 Family 1 家系2 Family 2 A-2282C 47.5 76.6 Unigene33789_All-658 — 55.3 Unigene19479_All-121 27.5 — C-6811T 50.5 — CL1689.Contig2_All-302 — 43.6 C-598G 26.9 — G-2782T — 54.1 A-642C 55.4 3.0 C-1453T 52.5 49.6 A+489C 48.9 45.1 对家系2中266尾大口黑鲈子代中的优势基因型进行了统计, 7尾大口黑鲈中含有最多的优势基因型, 所含数量都为6个, 在子代中所占的比例为2.6%。7个个体都只含有1个优势基因型, 所占比例为2.6%。A-2282C位点中优势基因型在子代群体中的分布频率最高, 为76.6%, A-642C中的优势基因型的分布频率最低, 为3.0% (表 3)。
2.3 生长性状相关优势基因型聚合分析
将家系1中大口黑鲈含有的优势基因型数量的不同组间的生长性状进行比较分析(表 4), 结果显示, 没有含优势基因型的个体组的生长性状值最小, 平均体质量为185.03 g, 而含6个优势基因型的个体组的生长性能最佳, 平均体质量为261.27 g, 比没有含优势基因型的个体组的平均体质量高41.2%。6个、5个、2个和0个优势基因型组相互之间在体质量方面均存在显著性差异(P<0.05), 且4个和2个优势基因型组间在体质量方面存在显著性差异(P<0.05)。家系2中所含优势基因型数量的不同大口黑鲈组间的生长性状的比较分析结果见表 5, 结果表明, 含1个优势基因型的个体的生长性状平均值最小, 平均体质量为184.43 g, 而含6个优势基因型的个体的生长性状平均值最大, 平均体质量为266.00 g, 且比没有含优势基因型的个体组的平均体质量高44.2%。6个、5个、4个和3个优势基因型组均分别与2个和1个优势基因型组的平均体质量差异显著(P<0.05)。家系1和家系2个体中生长相关基因优势基因型聚合数量多少与其表型性状呈正相关, 反映出通过对生长相关的优势基因型进行聚合可以获得具有优良生长性状的大口黑鲈。
表 4 家系1子代中所含不同优势基因型数量的个体的生长比较Table 4. Growth traits of largemouth bass with different pyramiding number of dominant genotypes in family 1优势基因型数量(样本数)
Number of dominant genotype体质量Body weight (g) 体长Body length (cm) 头长Head length (cm) 体高Body depth (cm) 尾柄长Caudal peduncle length (cm) 0 (8) 185.03±38.60e 20.38±1.77cd 6.25±0.43cd 6.21±0.35ce 3.91±0.47ad 1 (26) 196.46±61.68ce 20.29±1.95cd 6.40±0.69c 6.28±0.58ce 3.80±0.52cd 2 (75) 198.73±55.12ce 20.66±1.84cd 6.42±0.68cd 6.40±0.57de 3.86±0.46cd 3 (74) 212.59±56.77bce 21.12±1.83bc 6.64±0.61bd 6.59±0.58bce 3.95±0.45cd 4 (76) 222.66±64.00bd 21.46±2.03ab 6.70±0.71b 6.63±0.66bc 3.98±0.54cd 5 (35) 235.54±56.66b 21.90±2.16ab 6.85±0.77ab 6.79±0.77b 4.18±0.64a 6 (11) 261.27±46.96a 22.63±1.77a 7.40±0.72a 7.16±0.86a 4.35±0.61a 注: 表中数值为X±SD, 同列中上标字母不同表示差异显著(P<0.05); 下同Notes: Data in the table are $\bar X \pm {\rm{SD}}$ , different superscripts within the same column denote significant differences (P<0.05); the same applies below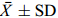 表 5 家系2子代中所含不同优势基因型数量的个体的生长比较Table 5. Growth traits of largemouth bass with different pyramiding number of dominant genotypes in family 2
表 5 家系2子代中所含不同优势基因型数量的个体的生长比较Table 5. Growth traits of largemouth bass with different pyramiding number of dominant genotypes in family 2优势基因型数量(样本数)
Number of dominant genotype体质量Body weight (g) 体长Body length (cm) 头长Head length (cm) 体高Body depth (cm) 尾柄长Caudal peduncle length (cm) 1 (7) 184.43±80.51b 21.04±2.97ab 6.38±0.75 6.41±1.06ab 4.01±0.46ab 2 (55) 213.17±71.94b 21.64±2.18b 6.86±2.3 6.43±0.90b 4.15±0.67b 3 (71) 243.77±83.48a 22.60±2.39a 6.94±0.75 6.74±0.99a 4.45±0.71a 4 (78) 249.98±68.85a 22.69±2.09a 6.85±0.66 6.76±0.75a 4.30±0.64ab 5 (48) 252.11±83.81a 22.73±2.23a 6.92±0.71 6.79±0.81a 4.30±0.69ab 6 (7) 266.00±85.24a 22.91±2.22ab 6.85±0.69 6.95±0.77ab 4.50±0.49ab 3. 讨论
基因聚合是将分散在不同的个体、品种或品系中的理想基因聚合到同一个基因组中。基因聚合是实现分子育种的重要技术手段[23]。多基因聚合在部分动植物上取得良好的效果, 如在鲁西牛的研究中, 优势基因型的数量随着生长性状改良的进行而增加[24], 在大口黑鲈“优鲈1号”和翘嘴鳜“华康1号”(Siniperca chuatsi Basilewsky)不同世代选育群体中, 优势基因型的平均含量随选育世代的增加均呈现递增趋势[25, 26]。李红霞等[27]发现了7个与建鲤增重相关的SNPs分子标记, 富集4个优势基因型的个体平均增重显著快于富集3个以下的个体的增重, 且比不含优势基因型的个体快约14%。本研究依据13个生长相关分子标记在大口黑鲈亲本中的基因型分布情况, 构建了2个优势基因型聚合家系, 分析子代中优势基因型聚合与生长性状的相关性, 结果显示, 个体中生长相关基因优势基因型聚合数量越多, 其所表现的生长性状表型值越高。这提示了利用生长性状相关优势基因型的聚合可实现生长表型性状的改良, 优势基因型聚合技术在大口黑鲈育种和生产实践中有着较好的应用前景。
家系1中含有2个优势基因型的个体的平均体质量为198.73 g, 稍高于含有1个优势基因型个体的平均体质量(196.46 g), 家系2中含有5个优势基因型的个体的平均体质量稍高于含有4个优势基因型个体的平均体质量。这与猪繁殖性状相关标记的聚合基因型的效应分析研究结果相类似[28, 29], 表明了在多基因聚合过程中并不是各优势基因型的效应简单地累加[9], 可能与相同调控网络中不同基因或位点之间会存在相互作用有关, 如颉抗作用和上位效应等。建鲤ODC1s基因上与增重相关的主效SNP位点之间存在着一定的颉抗作用[27]。张成锋等[30]分析黄河鲤生长相关优势基因型的富集效果, 发现D-Loop253和Koi42位点的加性效应间的互作达到显著水平, 是影响生长性状的重要因素。户国等[31]研究发现肉鸡(Gallus gallus)高脂品系中ApoB基因T123G位点与UCP基因C1197A位点间存在上位效应, 对腹脂率产生显著影响。
家系1中7个生长相关分子标记中的优势基因型群体平均体质量均高于相对应的劣势基因型群体, Unigene19479_All-121位点的优势与劣势基因型个体的平均体质量差异最大: 优势基因型个体的平均体质量为226.87 g, 劣势基因型个体的平均体质量为209.08 g, 而A-2282C位点中的优势与劣势基因型个体的平均体质量差异最小(11.2 g)。不同优势基因型对性状的影响作用不同, 加之各优势基因型之间可能存在的相互作用, 提示在今后的分子标记辅助选育过程中, 在富集多标记优势基因型的同时要考虑各优势基因型的组合, 选择互为协同作用的优势基因型前提下, 尽可能富集多的SNP标记优势基因型。该研究获得了聚合6个标记优势基因型聚合的个体, 后续是否可以筛选到聚合更多的优势基因型的个体?今后我们将继续进一步探讨, 该研究工作提供的聚合思路具有充分的可行性。
在本研究中所用的生长相关功能基因的作用均已在水产动物中得到了验证。从研究较为深入的经济性状相关功能基因上去筛选功能性分子标记, 然后利用功能性标记开展分子标记辅助选择, 选择的就是基因本身, 从而保证了选择的准确性和高效性[32]。通过人工选育出具有显著表型性状的群体是一个复杂的过程, 可将群体选育和功能性分子标记筛选与应用两者结合, 相互印证。本实验先前的研究结果显示, 在大口黑鲈“优鲈1号”不同世代选育群体中, 优势基因型的平均含量随选育世代的增加均呈现递增趋势, 反映出人工选育在一定程度上富集了优势基因[25]。在选育出表型显著的群体, 可为筛选到更多可用于分子标记辅助育种的功能性标记提供可靠的实验材料, 同时, 应用功能性分子标记开展类似本实验的研究, 并在选育中加以应用, 可以大大减少育种的工作量, 提高育种的效率。
-
表 1 所用大口黑鲈生长性状相关分子标记的相关信息
Table 1 Primers of growth-associated markers of largemouth bass
分子标记
Molecular marker标记所处基因名称
Gene name引物Primer (5′-3′) 延伸引物Extension primer(5′-3′) S1[ATTTTT(GTTT/-)TT] IGF-1 ACAAACCTTAATGTACTG
TTCTTCCTCTATGTCACCA-2282C PACAPA ATCACTGTCTGTCACTTCATG
ATAAATGATTCATTTGCAGCCTGTTTTTATCTCTCTCTCTCT Unigene33789_All-658 PCK CTGAAAGAGGAGCAATTCTC TTTTTTTTTTTTTTTTGAGCAATTCTCCTCTGATAATT Unigene19479_All-121 HSBP1 GGAGGACAGCATTTATAATAG
GTTATGAGTGGTCTTATCAAAGAACACCTCAGGTTTTTAGTCTA C-6811T MYH AGAGGAGGAAATCAAGGTATC
GCTCCTCCTCATACTGCTCCCTCAAATTACCGTGAATTCAG CL1689.Contig2_All-302 FOXO3b GTACAGACATGTATGATGCAG
CATGGTGTAAATCTGATCCAGTTTTTTTTTACAGAAAATCCAGTAAACAGAC C-598G CTSB TGAGTCATATGAAAGCATTAC
ACACTTTGTGTATGCAGGCTGTTTTTTTTATGCATTGGGGTGTGTCTCCAC G-2782T HBP CTCTTACAAGACGGCCTACTC
GAACAGGCACTGCTGGTACAGCTTTTTTTTTTTTTTAGCTCTTTGGGCTGCGGCTCAG C-18T POU1F1 GCAGCAGGGAGAAAGACAAG
CGTACACTGAAGGTTGACGTTAAAGTAAGACTAAACACAAGA A-642C Ghrelin AACCCTTGAATAAACATAACGT
TGGAGGAACCATATCGATGTCATC-1453T MSTN TACATCAAAGGAATAGTCTGC
ATGTCTCATAGTGGGTCAAATTTTTTTTTTGGAWATACTAAGGTAAACTTTC C-821G HSC70-1 TGAAGCCTACCTCGGAAAAGT
AGCATCCTTAGTGGCCTGGCGCTTACTTAGCATAGCTCTGGACA A-489C ApoproteinA1 ATTGAGCCCATCGTCACAGA
AGCAGCCAGTGTCTTCAGATTTTTTTTTTTTTTTTTTTTTTTTGTCTGAAGGCCAAGGTGGAGCC 表 2 13个生长标记在大口黑鲈亲本中的基因型
Table 2 Genotype of 13 growth related markers in largemouth bass parents
分子标记Molecular marker 优势基因型Dominant genotype 家系1亲本Parents of family 1 家系2亲本Parents of family 2 雄Male 雌Female 雄Male 雌Female S1 AA AA BB BB BB A-2282C AC CC AC AC AC Unigene33789_All-658 CC AA AC CC AC Unigene19479_All-121 AA AG AG AA AA C-6811T CC GG CG CC CC CL1689.Contig2_All-302 AA GG GG AG AG C-598G CC CT CT CT TT G-2782T TT TT GG GT GT C-18T CC TT CT CT TT A-642C AC CC AC CC AC C-1453T CT CT CT CT CT C-821G CC GG GG GG CC A-489C AC AC CC AC AC 表 3 不同标记中优势基因型的分布频率
Table 3 The frequency of dominant genotypes of different markers
分子标记
Molecular marker优势基因型频率Frequency of dominant genotypes (%) 家系1 Family 1 家系2 Family 2 A-2282C 47.5 76.6 Unigene33789_All-658 — 55.3 Unigene19479_All-121 27.5 — C-6811T 50.5 — CL1689.Contig2_All-302 — 43.6 C-598G 26.9 — G-2782T — 54.1 A-642C 55.4 3.0 C-1453T 52.5 49.6 A+489C 48.9 45.1 表 4 家系1子代中所含不同优势基因型数量的个体的生长比较
Table 4 Growth traits of largemouth bass with different pyramiding number of dominant genotypes in family 1
优势基因型数量(样本数)
Number of dominant genotype体质量Body weight (g) 体长Body length (cm) 头长Head length (cm) 体高Body depth (cm) 尾柄长Caudal peduncle length (cm) 0 (8) 185.03±38.60e 20.38±1.77cd 6.25±0.43cd 6.21±0.35ce 3.91±0.47ad 1 (26) 196.46±61.68ce 20.29±1.95cd 6.40±0.69c 6.28±0.58ce 3.80±0.52cd 2 (75) 198.73±55.12ce 20.66±1.84cd 6.42±0.68cd 6.40±0.57de 3.86±0.46cd 3 (74) 212.59±56.77bce 21.12±1.83bc 6.64±0.61bd 6.59±0.58bce 3.95±0.45cd 4 (76) 222.66±64.00bd 21.46±2.03ab 6.70±0.71b 6.63±0.66bc 3.98±0.54cd 5 (35) 235.54±56.66b 21.90±2.16ab 6.85±0.77ab 6.79±0.77b 4.18±0.64a 6 (11) 261.27±46.96a 22.63±1.77a 7.40±0.72a 7.16±0.86a 4.35±0.61a 注: 表中数值为X±SD, 同列中上标字母不同表示差异显著(P<0.05); 下同Notes: Data in the table are $\bar X \pm {\rm{SD}}$ , different superscripts within the same column denote significant differences (P<0.05); the same applies below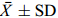
表 5 家系2子代中所含不同优势基因型数量的个体的生长比较
Table 5 Growth traits of largemouth bass with different pyramiding number of dominant genotypes in family 2
优势基因型数量(样本数)
Number of dominant genotype体质量Body weight (g) 体长Body length (cm) 头长Head length (cm) 体高Body depth (cm) 尾柄长Caudal peduncle length (cm) 1 (7) 184.43±80.51b 21.04±2.97ab 6.38±0.75 6.41±1.06ab 4.01±0.46ab 2 (55) 213.17±71.94b 21.64±2.18b 6.86±2.3 6.43±0.90b 4.15±0.67b 3 (71) 243.77±83.48a 22.60±2.39a 6.94±0.75 6.74±0.99a 4.45±0.71a 4 (78) 249.98±68.85a 22.69±2.09a 6.85±0.66 6.76±0.75a 4.30±0.64ab 5 (48) 252.11±83.81a 22.73±2.23a 6.92±0.71 6.79±0.81a 4.30±0.69ab 6 (7) 266.00±85.24a 22.91±2.22ab 6.85±0.69 6.95±0.77ab 4.50±0.49ab -
[1] 秦钢, 李杨瑞, 陈彩虹. 分子标记聚合育种在作物新品种选育中的应用. 广西农业科学, 2006, 37(4): 345—349 doi: 10.3969/j.issn.2095-1191.2006.04.002 Qin G, Li Y R, Chen C H. Application of gene pyra-miding in selection of crop new varieties [J]. Guangxi Agricultural Sciences, 2006, 37(4): 345—349 doi: 10.3969/j.issn.2095-1191.2006.04.002
[2] 鲁秀梅, 张宁, 陈劲枫, 等. 作物基因聚合育种的研究进展. 分子植物育种, 2017, 15(4): 1445—1454 Lu X M, Zhang N, Chen J F, et al. The research progress in crops pyramiding breeding [J]. Molecular Plant Breeding, 2017, 15(4): 1445—1454
[3] Chen T, Wu H, Zhang Y D, et al. Genetic improvement of Japonica rice variety Wuyujing 3 for stripe disease resi-stance and eating quality by pyramiding Stv-B i and Wx-mq [J]. Rice Science, 2016, 23(2): 69—77 doi: 10.1016/j.rsci.2016.02.002
[4] 董章辉, 石玉真, 张建宏, 等. 棉花纤维长度主效QTLs的分子标记辅助选择及聚合效果研究. 棉花学报, 2009, 21(4): 279—283 doi: 10.3969/j.issn.1002-7807.2009.04.005 Dong Z H, Shi Y Z, Zhang J H, et al. Molecular marker-assisted selection and pyramiding breeding of major QTLs for cotton fiber length [J]. Cotton Science, 2009, 21(4): 279—283 doi: 10.3969/j.issn.1002-7807.2009.04.005
[5] Zhang B, Shi W, Li W, et al. Efficacy of pyramiding elite alleles for dynamic development of plant height in common wheat [J]. Molecular Breeding, 2013, 32(2): 327—338 doi: 10.1007/s11032-013-9873-5
[6] 陈立凯, 郭涛, 刘永柱, 等. 基于" 多基因聚合-早世代组配”策略的水稻分子改良研究. 华北农学报, 2017, 32(3): 77—84 doi: 10.7668/hbnxb.2017.03.012 Chen L K, Guo T, Liu Y Z, et al. Molecular improvement based on the strategy of " multiple genes pyramiding-early-generation hybridized combination” in rice [J]. Acta Agriculturae Boreali-Sinica, 2017, 32(3): 77—84 doi: 10.7668/hbnxb.2017.03.012
[7] Kurokawa Y, Noda T, Yamagata Y, et al. Construction of a versatile SNP array for pyramiding useful genes of rice [J]. Plant Science, 2016, 242: 131—139 doi: 10.1016/j.plantsci.2015.09.008
[8] Korinsak S, Siangliw M, Kotcharerk J, et al. Improvement of the submergence tolerance and the brown planthopper resistance of the Thai jasmine rice cultivar KDML105 by pyramiding Sub1 and Qbph12 [J]. Field Crops Research, 2016, 188: 105—112 doi: 10.1016/j.fcr.2015.10.025
[9] 刘轩, 强巴央宗, 王强, 等. 藏猪繁殖性状多基因效应分析. 遗传, 2010, 32(5): 480—485 Liu X, Qiang B, Wang Q, et al. Effects of multi-genes for reproductive traits in Tibet pig [J]. Hereditas, 2010, 32(5): 480—485
[10] 陈克飞, 黄路生, 李宁, 等. 猪FSHβ及ESR合并基因型对猪产仔数性状的影响. 科学通报, 2000, 45(18): 1963—1966 doi: 10.3321/j.issn:0023-074X.2000.18.012 Chen K F, Huang L S, Li N, et al. Effects of combination genotype of FSHβ and ESR on litter size in pig [J]. Chinese Science Bulletin, 2000, 45(18): 1963—1966 doi: 10.3321/j.issn:0023-074X.2000.18.012
[11] 孙效文, 鲁翠云, 曹顶臣, 等. 镜鲤体重相关分子标记与优良子代的筛选和培育. 水产学报, 2009, 33(2): 177—181 Sun X W, Lu C Y, Cao D C, et al. Molecular markers associated with body weight of mirror carp and selection and raising of progenies [J]. Journal of Fisheries of China, 2009, 33(2): 177—181
[12] 李胜杰, 白俊杰, 赵荦, 等. 大口黑鲈EST-SNP标记开发及其与生长性状的相关性分析. 海洋渔业, 2018, 40(1): 38—46 doi: 10.3969/j.issn.1004-2490.2018.01.005 Li S J, Bai J J, Zhao L, et al. Development of EST-SNPs in largemouth bass (Micropterus salmoides) and analysis of their correlation with growth traits [J]. Marine Fishe-ries, 2018, 40(1): 38—46 doi: 10.3969/j.issn.1004-2490.2018.01.005
[13] Li S, Liu H, Bai J, et al. Transcriptome assembly and identification of genes and SNPs associated with growth traits in largemouth bass (Micropterus salmoides) [J]. Genetica, 2017, 145(2): 175—187 doi: 10.1007/s10709-017-9956-z
[14] 李胜杰, 姜鹏, 樊佳佳, 等. 大口黑鲈肌球蛋白重链基因SNPs的筛选及与生长性状的关联. 水产学报, 2018, 42(3): 305—313 Li S J, Jiang P, Fan J J, et al. SNPs detection of MYH gene and its association with growth traits in largemouth bass (Micropterus salmoides) [J]. Journal of Fisheries of China, 2018, 42(3): 305—313
[15] 李胜杰, 周春龙, 白俊杰, 等. 大口黑鲈组织蛋白酶B基因SNP筛选及其与生长性状关联分析. 淡水渔业, 2018, 48(2): 39—42 doi: 10.3969/j.issn.1000-6907.2018.02.006 Li S J, Zhou C L, Bai J J, et al. SNP detection in cathepsin B gene and analysis of its comelations with growth traits in largermouth bass (Micropterus salmoides) [J]. Freshwater Fisheries, 2018, 48(2): 39—42 doi: 10.3969/j.issn.1000-6907.2018.02.006
[16] 周春龙, 白俊杰, 李胜杰, 等. 大口黑鲈高密度脂蛋白结合蛋白基因(HBP)SNPs的筛选及与生长性状关联性分析. 农业生物技术学报, 2014, 22(2): 232—238 doi: 10.3969/j.issn.1674-7968.2014.02.013 Zhou C L, Bai J J, Li S J, et al. SNPs detection of high density lipoprotein binding protein gene (HBP) and its association with growth traits in largemouth bass (Micropterus salmoides) [J]. Journal of Agricultural Biotechnology, 2014, 22(2): 232—238 doi: 10.3969/j.issn.1674-7968.2014.02.013
[17] 杜芳芳, 白俊杰, 李胜杰, 等. 大口黑鲈POU1F1启动子区域SNPs对生长的影响. 水产学报, 2011, 35(6): 793—800 Du F F, Bai J J, Li S J, et al. Effects of SNPs in POU1F1 promoter on growth traits in largemouth bass (Micropte-rus salmoides) [J]. Journal of Fisheries of China, 2011, 35(6): 793—800
[18] 刘浩, 白俊杰, 李胜杰, 等. 大口黑鲈PACAP基因SNPs的筛选及其与生长性状的关联分析. 农业生物技术学报, 2016, 24(3): 390—396 Liu H, Bai J J, Li S J, et al. SNPs detection of PACAP gene and its association with growth traits in largemouth bass (Micropterus salmoides) [J]. Journal of Agricultural Biotechnology, 2016, 24(3): 390—396
[19] Li X H, Bai J J, Ye X, et al. Polymorphisms in the 5' flanking region of the insulin-like growth factor I gene are associated with growth traits in largemouth bass Micropterus salmoides [J]. Fisheries Science, 2009, 75(2): 351—358 doi: 10.1007/s12562-008-0051-3
[20] 刘浩, 白俊杰, 李胜杰, 等. 大口黑鲈ghrelin基因SNPs的筛选及与生长性状关联性分析. 水产学报, 2016, 40(4): 521—527 Liu H, Bai J J, Li S J, et al. SNPs detection of ghrelin gene and its association with growth traits in largemouth bass (Micropterus salmoides) [J]. Journal of Fisheries of China, 2016, 40(4): 521—527
[21] 李胜杰, 景燕娟, 白俊杰, 等. 大口黑鲈载脂蛋白基因序列单核苷酸多态性及与生长性状相关分析. 农业生物技术学报, 2018, 26(1): 132—139 Li S J, Jing Y J, Bai J J, et al. Single nucleotide polymorphism of apolipoprotein genes and analysis of its correlation with growth traits in Micropterus salmoides [J]. Journal of Agricultural Biotechnology, 2018, 26(1): 132—139
[22] 于凌云, 白俊杰, 樊佳佳, 等. 大口黑鲈肌肉生长抑制素基因单核苷酸多态性位点的筛选及其与生长性状关联性分析. 水产学报, 2010, 34(6): 665—671 Yu L Y, Bai J J, Fan J J, et al. SNPs detection in largemouth bass myostatin gene and its association with growth traits [J]. Journal of Fisheries of China, 2010, 34(6): 665—671
[23] Hu J, Cheng M, Gao G, et al. Pyramiding and evaluation of three dominant brown planthopper resistance genes in the elite indica rice 9311 and its hybrids [J]. Pest Mana-gement Science, 2013, 69(7): 802—808 doi: 10.1002/ps.2013.69.issue-7
[24] 李爱民, 马云, 杨东英, 等. 鲁西牛ANGPTL6基因的3个多态位点与其生长性状的关联性分析. 中国农业科学, 2012, 45(11): 2306—2314 doi: 10.3864/j.issn.0578-1752.2012.11.021 Li A M, Ma Y, Yang D Y, et al. Association analysis of three SNPs within ANGPTL6 gene with growth traits in luxi cattle [J]. Scientia Agricultura Sinica, 2012, 45(11): 2306—2314 doi: 10.3864/j.issn.0578-1752.2012.11.021
[25] 徐磊, 白俊杰, 李胜杰, 等. 生长相关优势基因型在大口黑鲈‘优鲈1号’选育世代中的聚合. 华南农业大学学报, 2014, 35(1): 7—11 doi: 10.7671/j.issn.1001-411X.2014.01.002 Xu L, Bai J J, Li S J, et al. Pyramiding of growth-related genotypes in generations of the largemouth bass, Micropterus salmoides, ‘Youlu No. 1’ [J]. Journal of South China Agricultural University, 2014, 35(1): 7—11 doi: 10.7671/j.issn.1001-411X.2014.01.002
[26] 宋易, 梁旭方, 田昌绪, 等. 生长相关分子标记在翘嘴鳜五代中的富集. 水生生物学报, 2016, 40(5): 951—957 doi: 10.7541/2016.123 Song Y, Liang X F, Tian C X, et al. Pyramiding of growth-related markers in five breeding generations of Siniperca chuatsi Basilewsky [J]. Acta Hydrobiologica Sinica, 2016, 40(5): 951—957 doi: 10.7541/2016.123
[27] 李红霞, 李建林, 唐永凯, 等. 建鲤ODC1基因型与增重的相关性分析. 水生生物学报, 2014, 38(3): 414—421 doi: 10.7541/2014.59 Li H X, Li J L, Tang Y K, et al. Correlation analysis between body weight gain and ODC1 genotypes in Cyprinus carpio var. Jian [J]. Acta Hydrobiologica Sinica, 2014, 38(3): 414—421 doi: 10.7541/2014.59
[28] 刘婵娟, 曾勇庆, 魏述东, 等. 8个猪种ESR和FSHβ基因合并基因型与繁殖性状关系的研究. 畜牧兽医学报, 2009, 40(3): 291—295 doi: 10.3321/j.issn:0366-6964.2009.03.002 Liu C J, Zeng Y Q, Wei S D, et al. Relationship between the combined genotypes of ESR and FSHβ genes and reproductive traits in eight pig breeds [J]. Acta Veterinaria et Zootechnica Sinica, 2009, 40(3): 291—295 doi: 10.3321/j.issn:0366-6964.2009.03.002
[29] Chen K, Li N, Huang L, et al. The combined genotypes effect of ESR and FSHβ genes on litter size traits in five different pig breeds [J]. Chinese Science Bulletin, 2001, 46(2): 140—143 doi: 10.1007/BF03187010
[30] 张成锋, 苏胜彦, 朱健, 等. 富集优势基因型的后备亲本筛选以及相关分子标记的遗传效应分析. 水生生物学报, 2017, 41(1): 79—85 doi: 10.7541/2017.10 Zhang C F, Su S Y, Zhu J, et al. Candidate parents selection containing multiple genotypes with higher perfor-mance and correlated molecular markers’ genetic effects analysis [J]. Acta Hydrobiologica Sinica, 2017, 41(1): 79—85 doi: 10.7541/2017.10
[31] 户国, 王守志, 张森, 等. ApoB与UCP基因间上位效应对鸡腹脂性状影响的遗传学分析. 遗传, 2010, 32(1): 59—66 doi: 10.3760/cma.j.issn.1673-4386.2010.01.014 Hu G, Wang S Z, Zhang S, et al. Genetic analysis of epistatic effects between ApoB and UCP on abdominal fat trait in chicken [J]. Hereditas, 2010, 32(1): 59—66 doi: 10.3760/cma.j.issn.1673-4386.2010.01.014
[32] 徐锐. 野生香菇数量性状与SSR分子标记的关联分析. 硕士学位论文. 武汉: 华中农业大学. 2013 Xu R. Association analysis of quantitative traits with SSR markers in strains of wild Lentinula edodes [D]. Wuhan: Huazhong Agricultural University. 2013
-
期刊类型引用(3)
1. 陶欣,邱丽华,张博,王鹏飞,闫路路,赵超,林云想,林锋. 花鲈igf3基因SNP位点的鉴定及其与生长性状的关联分析. 基因组学与应用生物学. 2024(01): 109-116 .  百度学术
百度学术
2. 孙雪,李胜杰,杜金星,姜鹏,周家辉,白俊杰. 草鱼生长相关优势基因型的聚合效果分析. 渔业科学进展. 2021(05): 40-46 .  百度学术
百度学术
3. 鲁翠云,匡友谊,郑先虎,孙志鹏,孙效文. 转化生长因子-β(TGF-β)基因家族在水产养殖中的潜在应用价值. 水产学杂志. 2020(06): 89-96 .  百度学术
百度学术
其他类型引用(3)
计量
- 文章访问数: 8028
- HTML全文浏览量: 6470
- PDF下载量: 68
- 被引次数: 6



 下载:
下载: