THE EFFECTIVE FECUNDITY IN MALE ILLEX ARGENTINUS IN SOUTHWEST ATLANTIC OCEAN
-
摘要: 对西南大西洋阿根廷滑柔鱼(Illex argentinus)雄性个体的有效繁殖力特性, 以及有效繁殖力与个体生长发育关系进行了研究。结果表明, 阿根廷滑柔鱼雄性个体的胴长、体重的生物学最小型分别为207.79 mm和162.55 g; 个体有效繁殖力为(374±280.33)条精荚, 胴长相对有效繁殖力为(179.18±117.66)条/mm; 精荚的平均长度为(21.57±4.17) mm, 是胴长的(10.22±1.82)%。随着性腺发育, 个体有效繁殖力和精荚长度均增长显著(P<0.05), 前者在功能性成熟期达到最大值, 为(811±181.34)条精荚; 后者在繁殖产卵期达到最大值, 为(23.89±3.87) mm。同时, 个体有效繁殖力和精荚长度均与胴长、体重呈显著的线性函数关系(P<0.05)。回归拟合数据集比较分析和多元线性回归分析显示, 个体有效繁殖力与胴长、体重之间的线性关系不存在显著性差异(P>0.05), 但是体重对个体有效繁殖力的影响更为显著(P<0.001); 精荚长度与胴长、体重之间的线性关系存在显著性差异(P<0.001), 并且胴长、体重两者对精荚长度具有一致的影响效应(P<0.001)。以上结果表明, 阿根廷滑柔鱼雄性个体随着性腺发育持续产生并存储精荚, 精荚长度也随之显著增加, 并且与个体大小密切相关。Abstract: Illex argentinus is one of the most important ommastrephid squids, due to its annual landing volume, and its key role as transient ‘biological pumps’ in southwest Atlantic ecosystem. In order to understand the fecundity characteristics of male ommastrephids, specimens of male I. argentinus, collected from December 2012 to March 2013, were used to analyze the fecundity and its relationship to reproductive development with biological statistics analysis. The results showed that the minimum biological size was 207.29 mm for mantle length (ML) and 162.55 g for body weight (BW). The effective fecundity (EF), defined as the sum of normal spermatophores in spermatophoric complex and spermatophoric sac, was in an average of (374±280.33) spermatophores. The mean value of relative effective fecundity by mantle length was (179.18±117.66) spermatophores per millimeter. The length of spermatophores (SL) varied from 6.34 to 33.14 mm, and its mean value was (21.57±4.17) mm, which was (10.22±1.82)% of mantle length. Both EF and SL significantly increased with the onset of sexual maturation (P<0.05). EF attained the maximum value at functionally maturity stage (Ⅵ), with a mean value of (811±181.34) spermatophores. SL increased up to the mating stage (Ⅶ), whereby it attained a mean value of (23.89±3.87) mm. Meanwhile, both EF and SL showed significantly linear relation with mantle length (EF=–581.92+4.56ML, R2=0.17, P<0.05;SL=5.77+0.075ML, R2=0.23, P<0.05) and body weight (EF=16.55+1.77BW, R2=0.37, P<0.05;SL=17.96+0.017BW, R2=0.17, P<0.05), indicating that individual with bigger size has larger EF and longer SL. Furthermore, the compare datasets of fitted model analysis revealed that there was no significant difference between the linear relationship of EF-ML and that of EF-BW (P>0.05). Based on multiple regression analysis, however, the influence on EF from body weight was more significant than that from mantle length (P<0.05). The compare datasets of fitted model analysis for SL showed that there was significant difference between the linear relationship of SL-ML and that of SL-BW (P<0.001), although the multiple regression analysis suggested a comparative influence on SL from both mantle length and body weight (P<0.001). These findings indicated that the EF of maleI. argentinus was a strategy of adaptability to its short lifespan by producing and accumulating spermatophores along with reproductive development and body growth, and the length of spermatophores will also increase with time.
-
个体繁殖力作为物种生存对策的重要数量遗传性状, 表征其繁殖后代和生存的能力, 是种群数量变动的重要影响因子[1]; 而繁殖力的变动及其调节规律是种群补充过程的最主要环节之一[2]。其中, 有效繁殖力(Effective fecundity, EF)是个体在某一段生活史时期或生命周期内可以成功排出并可完成授精的配子数量, 可以直接体现个体潜在繁殖力的有效部分[3, 4]。
阿根廷滑柔鱼(Illex argentinus)隶属于软体动物门, 头足纲, 枪形目, 柔鱼科, 滑柔鱼属, 广泛分布在22°—54°S的西南大西洋大陆架和大陆坡海域, 尤以35°—52°S海域资源最为丰富[5], 是世界上重要的经济头足类, 其渔获量占世界头足类总产量的10%以上[6], 也是我国远洋鱿钓渔业中的三大捕捞对象之一[7]。同时, 因生命周期短、生长速度快、资源生物量大等特点[5], 阿根廷滑柔鱼在西南大西洋生态系统中扮演着重要的“生物泵”角色, 是生态系统中主要的生物指标[8]。目前, 国内外研究表明, 阿根廷滑柔鱼索饵期间个体生长和性腺发育同步[9, 10], 雄性个体先于雌性个体性腺发育成熟[11], 功能性发育成熟时性腺指数达到最大值[12, 13], 雌性潜在繁殖力高达120万粒卵母细胞[14], 产卵期间歇性排卵[14, 15]等。然而, 这些研究集中于雌性个体, 对雄性个体的繁殖生物学鲜有报道, 尤其在雄性个体繁殖力特性研究方面较为缺乏。为此, 本研究以2012年12月至2013年3月渔汛期间采集的阿根廷滑柔鱼样本为对象, 进行雄性个体有效繁殖力特性及其与个体生长发育关系研究, 为科学合理地、可持续地开发利用该种群资源提供科学依据。
1. 材料与方法
1.1 样品来源
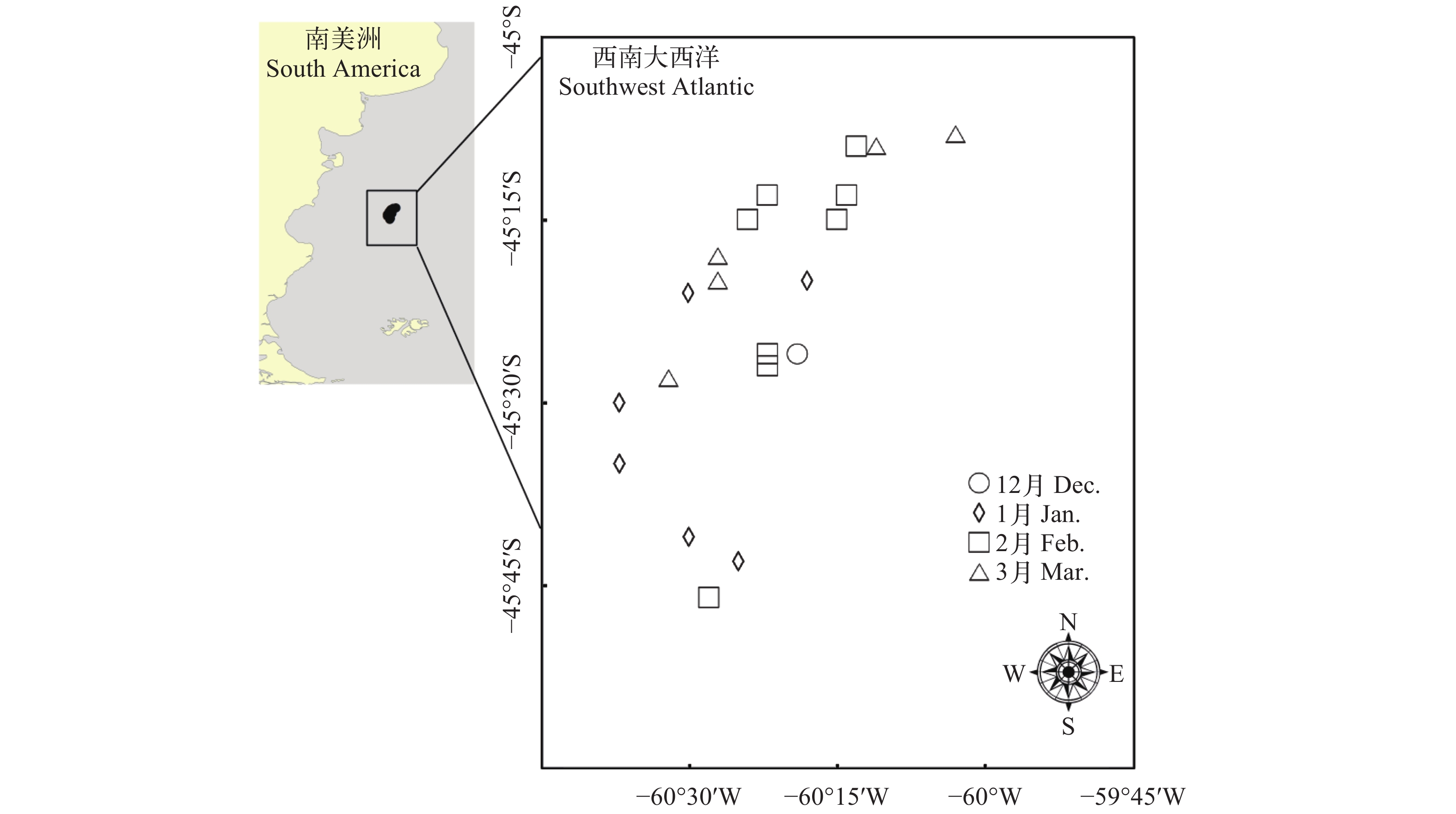
阿根廷滑柔鱼样本来自我国大洋性鱿钓渔船在西南大西洋阿根廷公海海域作业期间的渔获物, 作业方式为灯光诱捕法, 渔具为大洋性通用的垂钓式拟饵复钩型钓具; 采集时间为2012年12月下旬至2013年3月上旬, 采集海域为45°08′S—45°46′S、60°03′W—60°37′W (图 1)。根据大洋性鱿钓渔船作业渔场相对灵活的特点, 每周从钓捕的渔获物中随机采集样本1次, 每次平均随机采集30尾样本(不分雌雄)。期间, 进行了21次样本采集, 共采集样本732尾(不分雌雄)。采集样本经–20℃冷冻保藏运回实验室进行生物学等研究分析。
1.2 研究方法
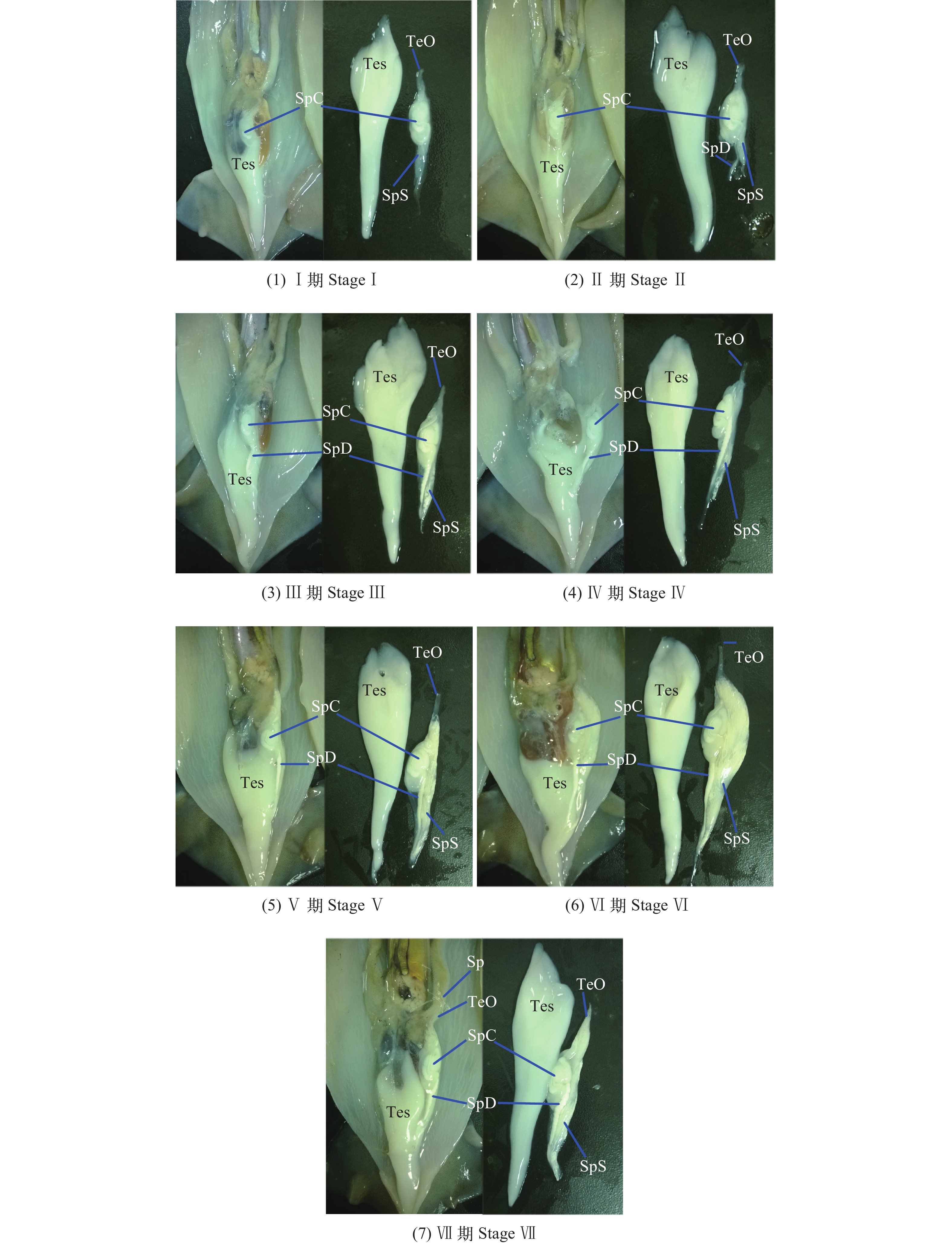
在实验室解冻后, 解剖分析判别样本雌雄性别, 测定分析了269尾雄性样本。测定的生物学数据, 包括胴长(ML)、体重(BW)、性腺成熟度等。胴长测定精确至1 mm, 体重测定精确至1 g。以Arkhipkin[16]和国际海洋考察理事会(International Council for the Exploration of the Sea, ICES)[17]等性腺成熟度划分标准为参考, 结合观察结果, 将阿根廷滑柔鱼雄性个体生殖系统发育程度划分为Ⅰ—Ⅷ个等级(图版Ⅰ)。其中, Ⅰ期未发育, 精巢小, 白色, 半透明, 肉眼不见输精管。Ⅱ期开始发育, 精巢变大变厚, 白色; 可见细小的白色输精管。Ⅲ期生理性发育, 精巢灰白色, 精荚复合体结构清晰, 输精管白色且迂回曲折, 精荚囊可见白色颗粒物和(或者)少量发育成熟的精荚; Ⅳ期生殖性成熟前期, 精巢完全发育成熟, 淡黄色; 输精管白色, 管径大; 端器延长, 凸出于内脏膜; 精荚囊可见成熟精荚, 精荚数量占其体积<20%。Ⅴ期生理性成熟后期, 精巢、输精管的形态如Ⅳ期, 精荚囊显著增大, 前、中、后3段区分明显, 精荚数量占其体积的20%—50%; Ⅵ期功能性成熟期, 精巢、输精管、精荚囊的形态如Ⅴ期, 精荚囊进一步增大, 50%—100%的体积充满精荚; 端器延长, 凸出于左鳃基部, 但未见有精荚。Ⅶ期繁殖期, 精巢和精荚复合体松软, 灰白色; 精荚囊前段、中段充满精荚, 后段精荚数量明显变少; 端器延长, 可见正在外排的精荚。Ⅷ期繁殖后期, 精巢萎缩, 精荚复合体松软, 精荚囊没有精荚或少量精荚。鉴别结果显示, 实验样本的性腺成熟度等级可鉴定为Ⅰ—Ⅶ期, Ⅷ期样本未发现。
![]() 图版Ⅰ 阿根廷滑柔鱼雄性个体的生殖系统发育图1—7分别示Ⅰ—Ⅶ性腺成熟度的生殖系统发育形态。其中,Sp表示精荚,SpC表示精荚复合体,SpD表示输精管,SpS表示精荚囊,TeO表示端器,Tes表示精巢图版Ⅰ. The development of reproductive system in male Illex argentinusAnatomical examination of 1—7 indicates the development of reproductive system in male Illex argentinus along with sexual maturation. Sp, spermatophore; SpC, spermatophoric complex; SpD, spermaduct; SpS, spermatophoric sac; TeO, terminal organ; Tes, testis
图版Ⅰ 阿根廷滑柔鱼雄性个体的生殖系统发育图1—7分别示Ⅰ—Ⅶ性腺成熟度的生殖系统发育形态。其中,Sp表示精荚,SpC表示精荚复合体,SpD表示输精管,SpS表示精荚囊,TeO表示端器,Tes表示精巢图版Ⅰ. The development of reproductive system in male Illex argentinusAnatomical examination of 1—7 indicates the development of reproductive system in male Illex argentinus along with sexual maturation. Sp, spermatophore; SpC, spermatophoric complex; SpD, spermaduct; SpS, spermatophoric sac; TeO, terminal organ; Tes, testis因为从性腺成熟度Ⅳ期开始精荚囊可见成熟的精荚, 因此随机选取Ⅳ期14尾、Ⅴ期13尾、Ⅵ期6尾和Ⅶ期13尾阿根廷滑柔鱼雄性个体, 摘取精荚复合体(含精荚腺和输精管)和精荚囊(含端器)保存于10%的福尔马林溶液中固定, 以进行有效繁殖力的估算。有效繁殖力(EF)估算为精荚复合体和精荚囊中所有精荚的数目之和, 胴长相对有效繁殖力(REF)为个体有效繁殖力与胴长的比值。估算后, 随机选取10条的精荚, 置于配有数码摄像仪的解剖镜(1×—4.5×)下摄取照片, 利用数码摄像仪相配套的Image-pro Plus 5.0软件测定精荚长度(Spermatophore length, SL), 精确到0.01 mm。
1.3 数据分析
基于测定的数据, 采用频率分布法计算阿根廷滑柔鱼雄性个体的胴长和体重组成。胴长组间距采用10 mm, 体重组间距采用20 g。计算平均胴长、平均体重及其方差; 以一组或多组合计比例高于80%为计算基准[18], 统计分析优势胴长组、优势体重组及其所占比例。根据不同性腺成熟度, 统计分析有效繁殖力、精荚长度随着性腺发育的异同性。
(1)利用幂函数, 求取阿根廷滑柔鱼雄性个体胴长与体重之间的关系:
$B \! W = {\rm{a}}M{L^{\rm{b}}}$
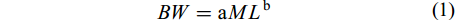
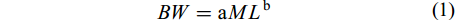
(1) 式中, BW为体重(g); ML为胴长(mm): a、b为(1)的估算参数。
(2)利用Logistic曲线, 以10 mm和20 g为间距, 拟合回归求取阿根廷滑柔鱼雄性个体的胴长和体重生物学最小型:
${P_i} = \frac{1}{{1 + {e^{ - \left( {{\rm{c}} + {\rm{d}}{l_i}} \right)}}}}$
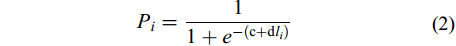
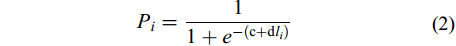
(2) ${P_i} = \frac{1}{{1 + {e^{ - \left( {{\rm{e}} + {\rm{f}}{w_i}} \right)}}}}$
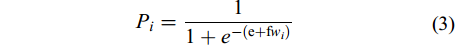
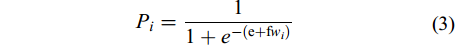
(3) 式中: Pi为成熟个体占组内样本的百分比; li和wi分别为各胴长组(mm)和体重组(g); c、d和e、f分别为(2)和(3)的估算参数; 胴长生物学最小型ML50%= –c/d, 体重生物学最小型TW50%= –e/f。
(3)利用线性函数, 拟合回归阿根廷滑柔鱼雄性有效繁殖力、精荚长度与胴长、体重的关系。同时, 利用多元线性回归分析建立有效繁殖力、精荚长度与胴长、体重的全回归方程关系, 求取标准化回归系数, 分析胴长、体重对有效繁殖力和精荚长度的影响显著性。
数据处理采用统计学软件Origin 2015和SPSS 20.0。单因素方差分析(one-way ANOVA)检验个体有效繁殖力、精荚长度随性腺发育的差异性, 卡方(χ2)检验分析个体胴长相对有效繁殖力、胴长相对精荚长度随性腺发育的差异性; 若存在差异性, 则采用Tukey HSD检验(Tukey’s honest significant post-hoc test)分析差异性存在的成熟度等级; 回归拟合数据集比较(Compare datasets of fitted models)检验分析有效繁殖力、精荚长度两者分别与胴长、体重线性拟合回归关系的差异性[19]。同时, 采用多元线性回归分析(Multiple regression analysis)分别建立个体有效繁殖力、精荚长度两者与胴长和体重的全回归方程关系, 建立标准化回归方程及其标准化回归系数, 分析胴长和体重对个体有效繁殖力、精荚长度的影响效应的差异性。统计学显著性水平为P<0.05; 实验相关数据以平均值±标准差(SD)表示。
2. 结果
2.1 雄性个体组成
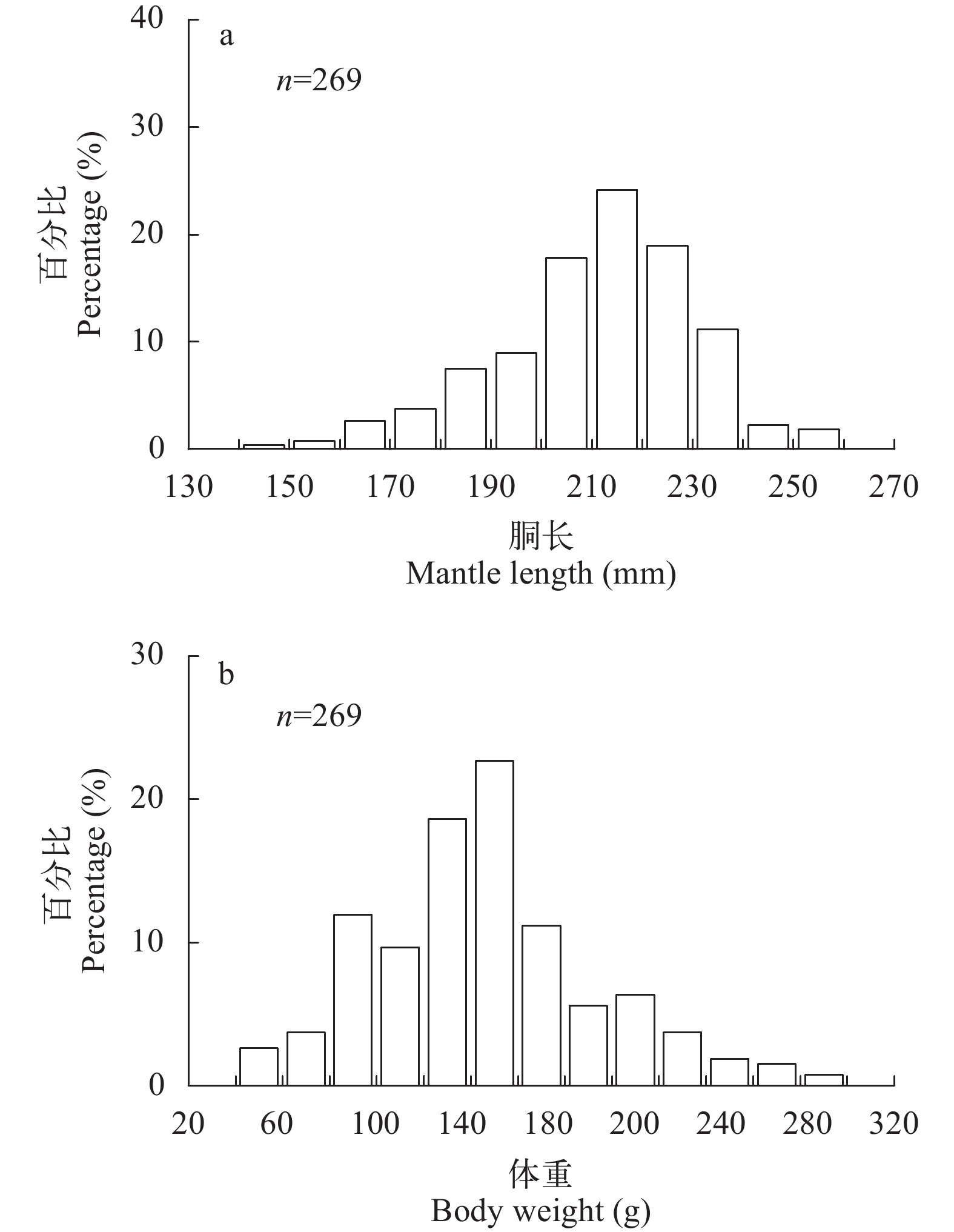
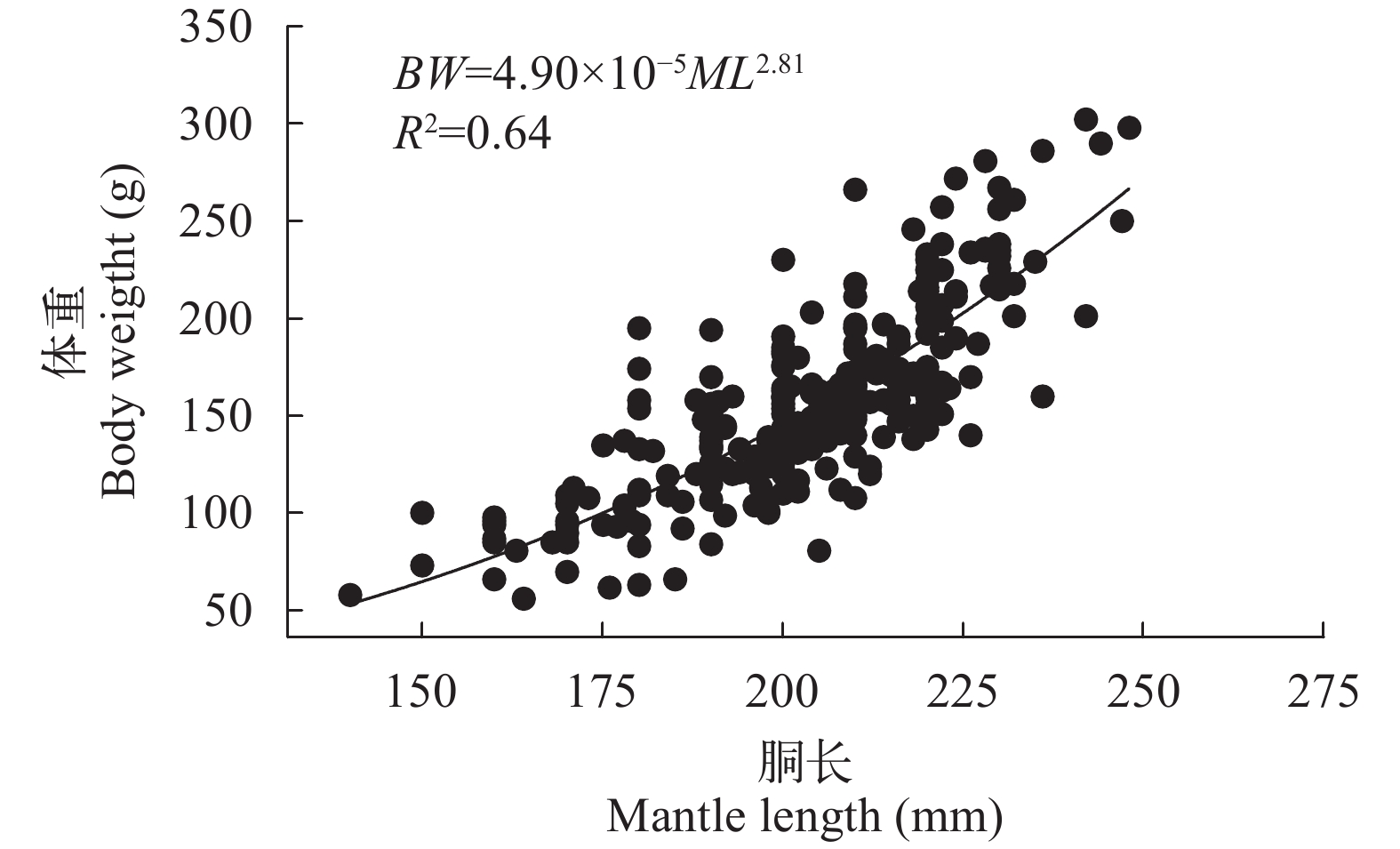
统计分析显示, 阿根廷滑柔鱼雄性个体的胴长范围为140—248 mm, 平均胴长为(203.46±18.90) mm, 优势胴长为170—230 mm, 约占总体的88.15%(图 2a); 体重范围为56—302 g, 平均值为(155.86±47.25) g, 优势体重范围为80—240 g, 约占总体的92.19% (图 2b)。体重与胴长的幂函数关系式为BW=4.90×10–5·ML2.81(n=269, R2=0.64, P<0.01) (图 3)。
2.2 生物学最小型
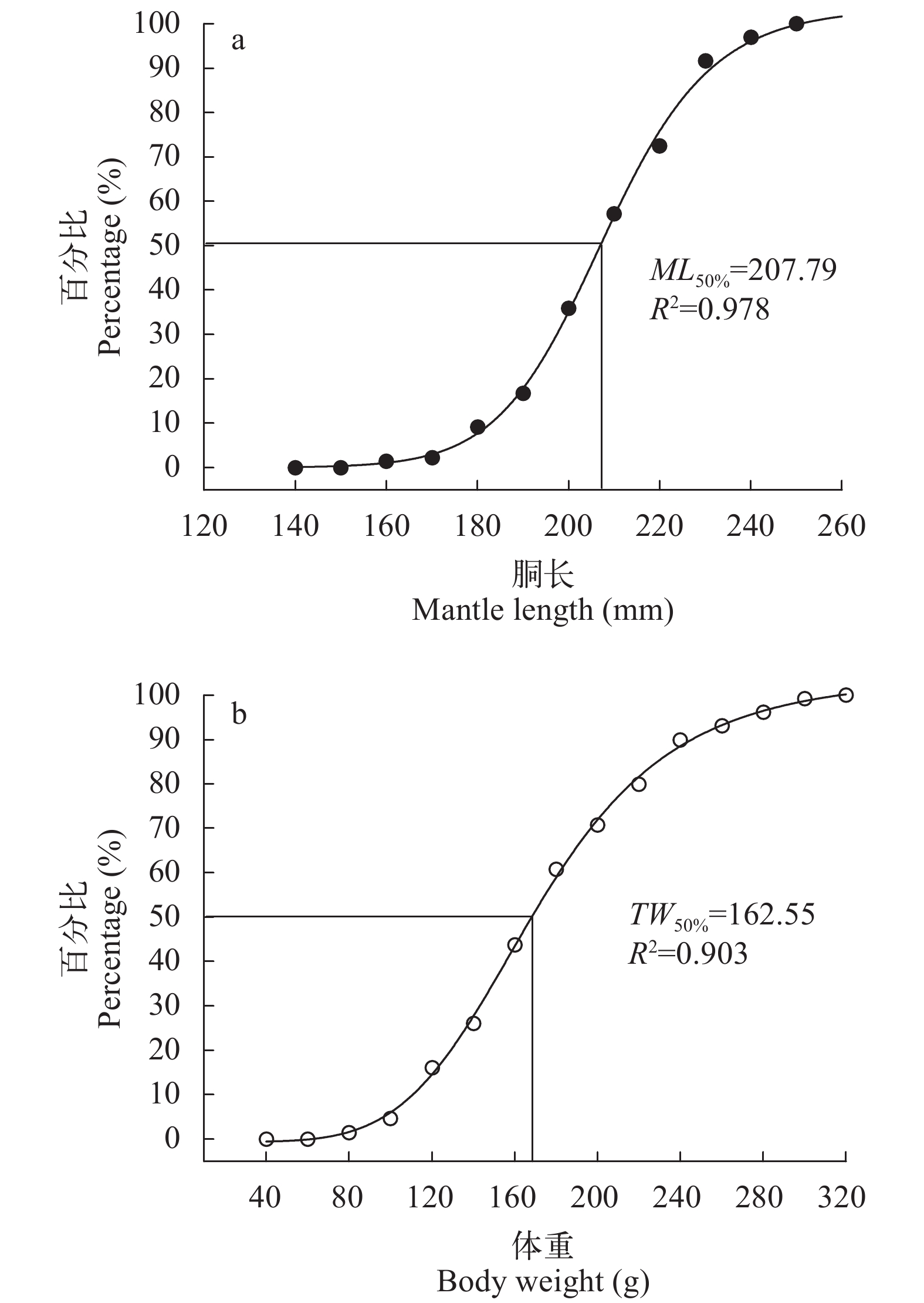
在实验样本中, 阿根廷滑柔鱼雄性个体性腺发育成熟的最小胴长为160 mm, 最小体重为56 g; 胴长大于236 mm、体重大于286 g的个体均性腺发育成熟。Logistic曲线拟合结果显示, 雄性个体的胴体生物学最小型ML50%为207.79 mm (R2=0.978), 体重生物学最小型TW50%为162.55 g (R2=0.903) (图 4)。
2.3 个体有效繁殖力
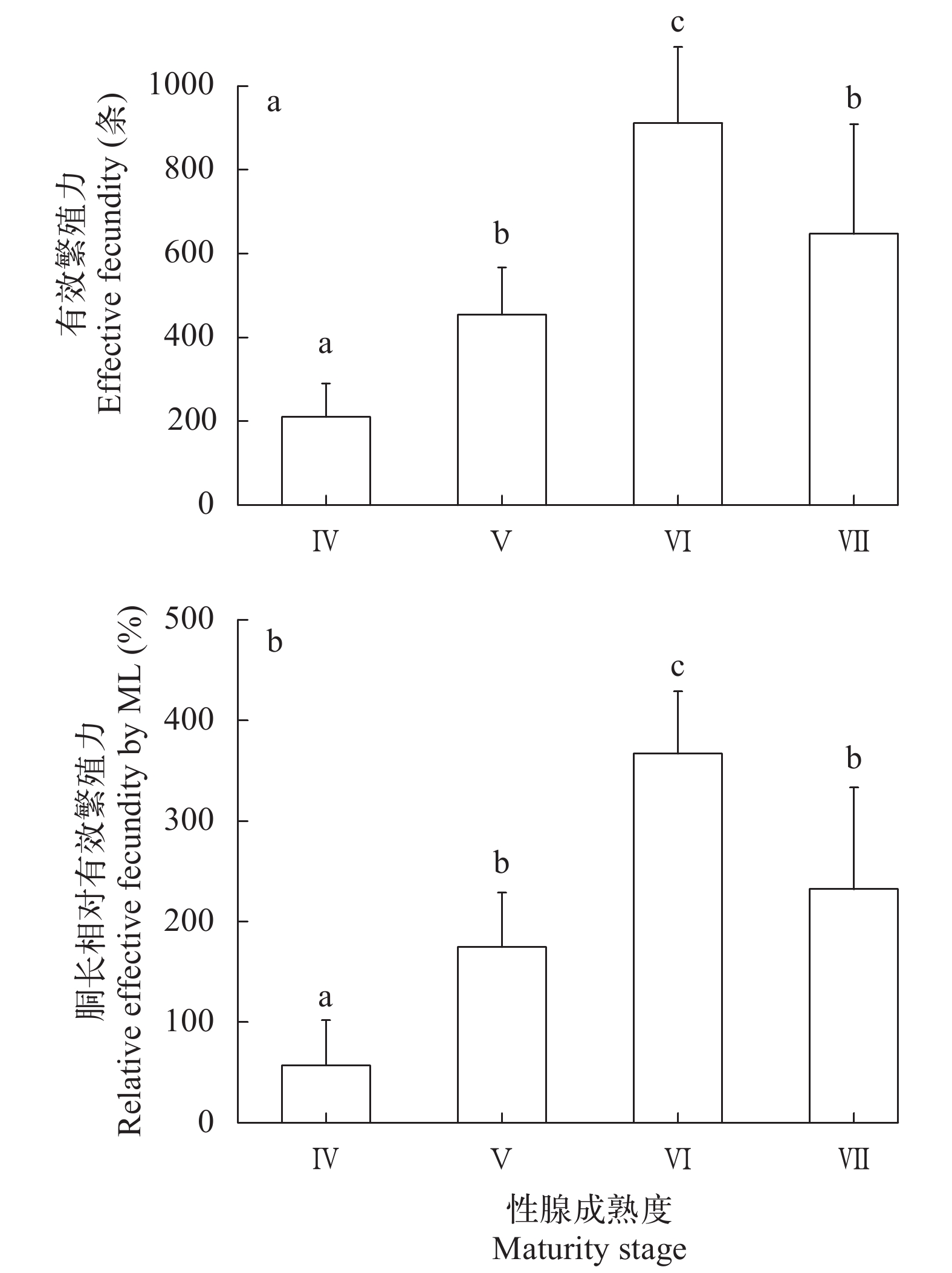
分析显示, 阿根廷滑柔鱼雄性个体有效繁殖力为11—1049条精荚, 平均有效繁殖力为(374±280.33)条精荚; 胴长相对有效繁殖力为(179.18±117.66)条/mm。随着性腺发育, 雄性个体的有效繁殖力显著增加(ANOVA: F=30.39, P<0.001), 并且在Ⅵ期时达到最大值(图 5a); 同时, 不同性腺成熟, 个体的胴长相对有效繁殖力差异性显著(χ2=1069.58, P<0.001)(图 5b)。其中, 性腺成熟度Ⅳ时, 有效繁殖力为11—216条精荚, 平均有效繁殖力为(110±79.69)条精荚, 平均胴长相对有效繁殖力为(57.08±44.71)条/mm; Ⅴ期时, 有效繁殖力为199—583条精荚, 平均有效繁殖力为(354±112.03)条精荚, 平均胴长相对有效繁殖力为(174.59±53.84)条/mm; Ⅵ时, 有效繁殖力为624—1049条精荚, 平均有效繁殖力为(811±181.34)条精荚, 平均胴长相对有效繁殖力为(366.90±61.67)条/mm; Ⅶ时, 有效繁殖力为241—991条精荚, 平均有效繁殖力为(547±261.23)条精荚, 平均胴长相对有效繁殖力为(232.18±101.06)条/mm。
![]() 图 5 阿根廷滑柔鱼雄性有效繁殖力和胴长相对有效繁殖力分布各组平均值上标示的不同字母表示Tukey HSD检验差异显著(P<0.05); 下同Figure 5. The distribution of effective fecundity and relative effective fecundity by mantle length with sexual maturationin male Illex argentinusMean values with different subscripts are significantly different (P<0.05) as determined using Tukey HSD test; the same applies below
图 5 阿根廷滑柔鱼雄性有效繁殖力和胴长相对有效繁殖力分布各组平均值上标示的不同字母表示Tukey HSD检验差异显著(P<0.05); 下同Figure 5. The distribution of effective fecundity and relative effective fecundity by mantle length with sexual maturationin male Illex argentinusMean values with different subscripts are significantly different (P<0.05) as determined using Tukey HSD test; the same applies below2.4 个体有效繁殖力与胴长、体重关系
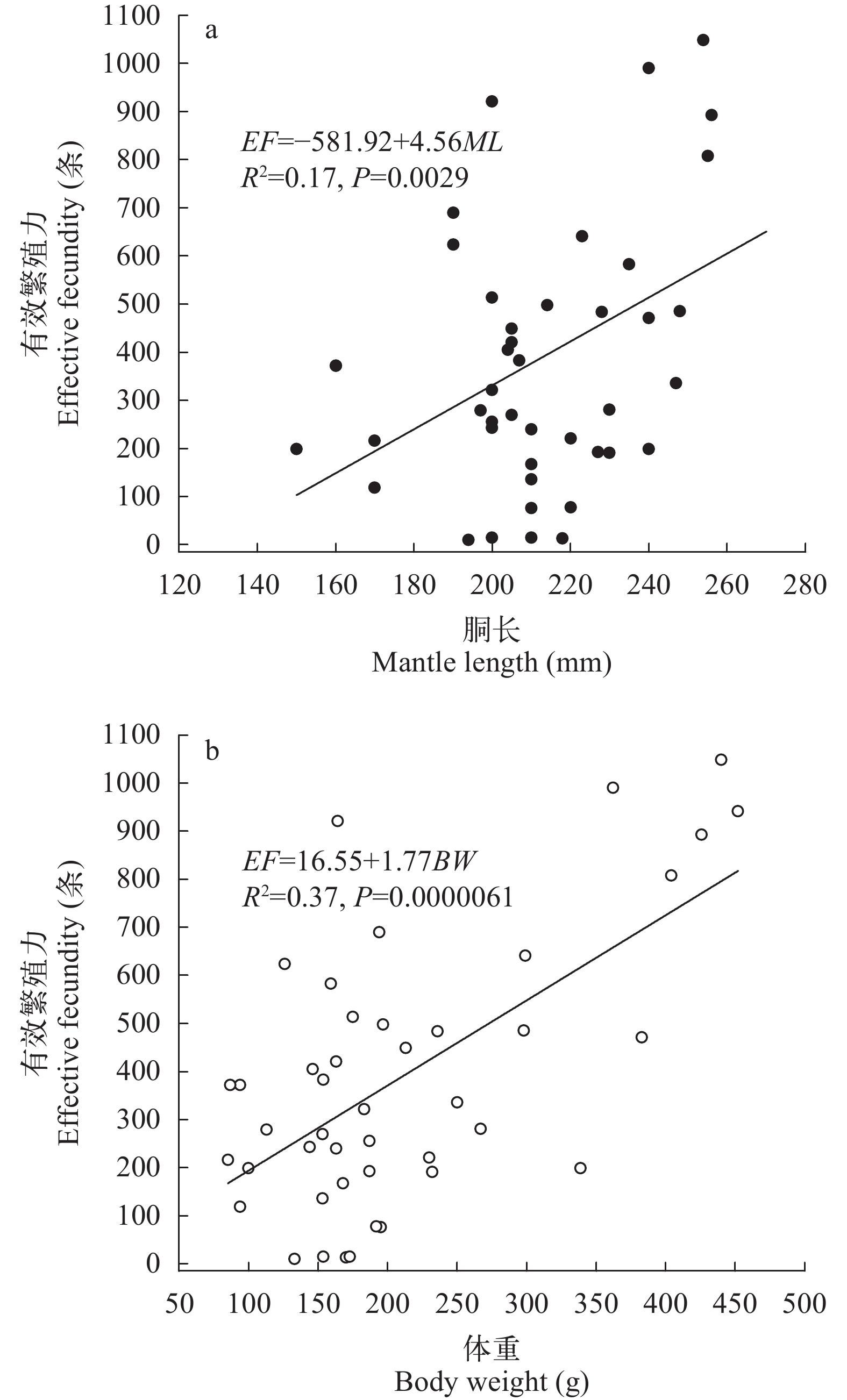
随着个体生长, 阿根廷滑柔鱼雄性有效繁殖力呈显著的正相关关系(图 6)。其中, 回归分析显示, 雄性有效繁殖力与胴长呈显著的线性关系(F=9.98, P<0.05), 回归方程式为EF=–581.92+4.56ML (R2=0.17); 雄性有效繁殖力与体重的线性回归关系式为EF=16.55+1.77BW (R2=0.37; F=26.73, P<0.001)。
回归拟合数据集的比较分析显示, 阿根廷滑柔鱼雄性个体的有效繁殖力与胴长、体重之间的线性关系不存在显著性差异(F=1.98, P>0.05)。但是, 多元回归分析显示雄性有效繁殖力与胴长和体重的全回归方程为EF=733.644–4.41ML+2.82BW (R2=0.43, F=15.64, P<0.001), 胴长、体重的标准化回归系数分别为–0.42 (P>0.05)和0.99 (P<0.001), 表明个体有效繁殖力与体重的相关性更为显著。
2.5 个体精荚长度
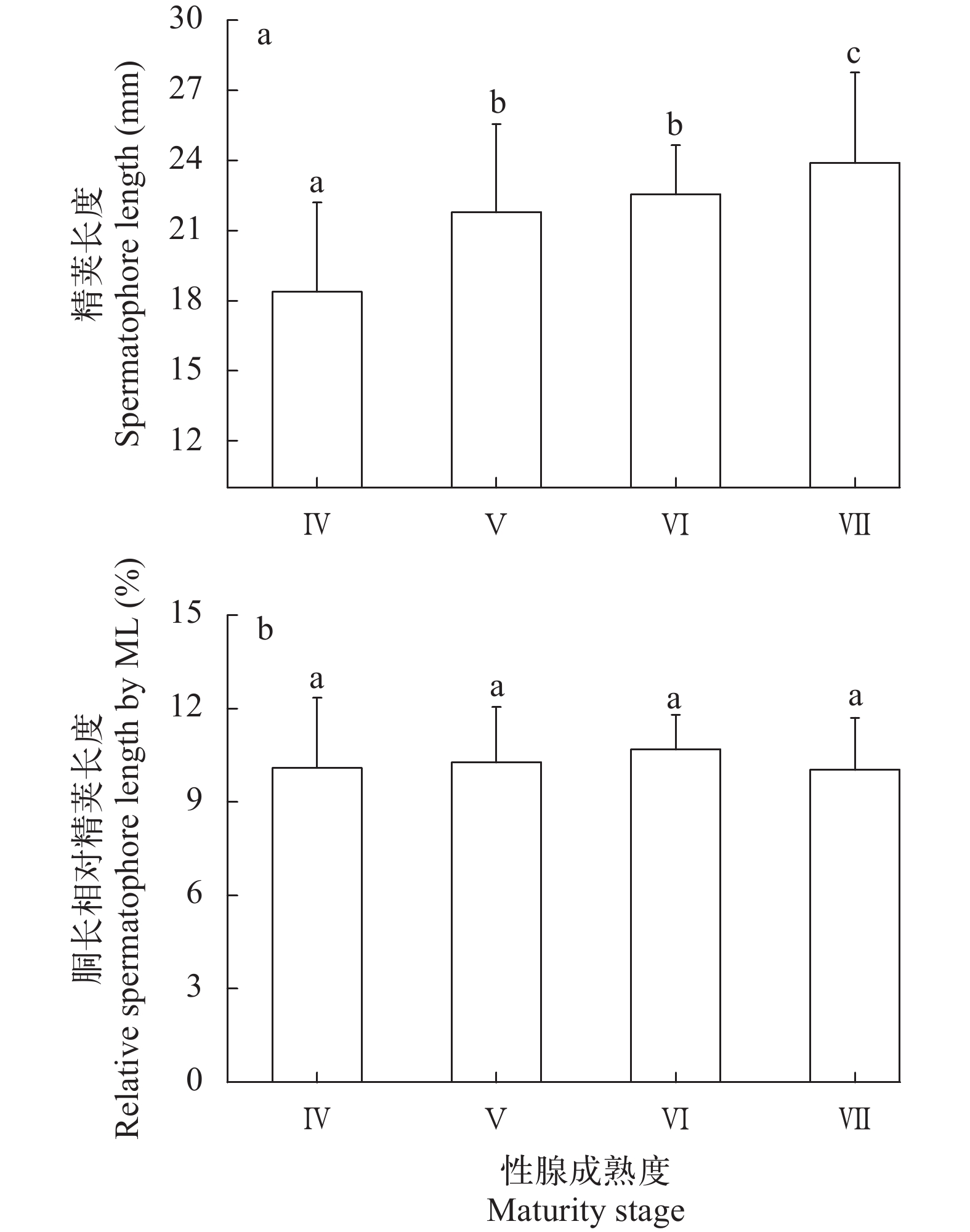
分析显示, 雄性个体的精荚长度为6.34—33.14 mm, 平均长度为(21.57±4.17) mm, 胴长相对平均长度为(10.22±1.82)%。随着性腺发育, 个体的精荚长度增长显著(ANOVA: F=48.04, P<0.001); 在不同性腺成熟度之间, 精荚的胴长相对长度的差异性不显著(χ2=1.97, P=0.12)(图 7)。其中, Ⅳ期时精荚长度为6.34—26.92 mm, 平均长度为(18.39±3.81) mm, 胴长相对平均长度为(10.10±2.23)%; Ⅴ期时精荚长度为9.36—31.76 mm, 平均长度为(21.79±3.77) mm, 胴长相对平均长度为(10.27±1.76)%; Ⅵ期时精荚长度为16.97—32.35 mm, 平均长度为(22.55±2.01) mm, 胴长相对平均长度为(10.68±1.11)%; Ⅶ期时精荚长度为17.20—33.14 mm, 平均长度为(23.89±3.87) mm, 胴长相对平均长度为(10.03±1.67)%。
2.6 个体精荚长度与胴长、体重的关系
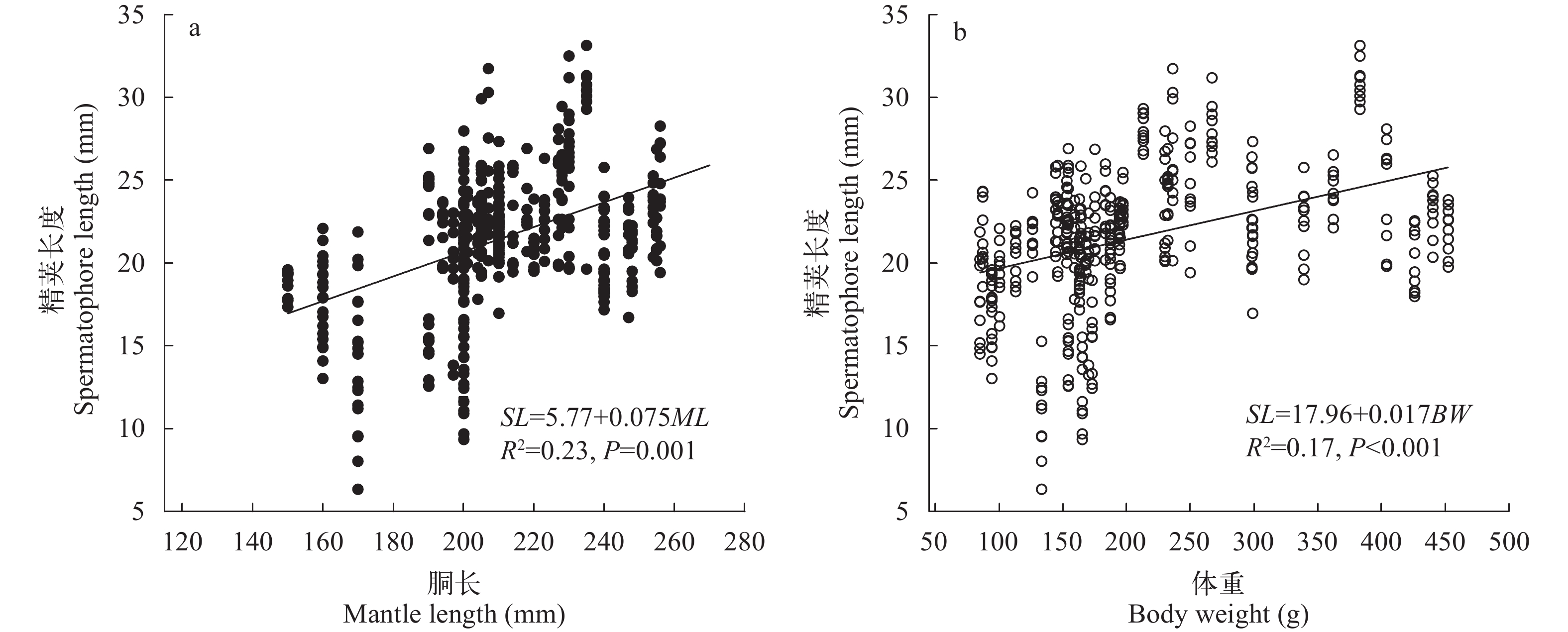
线性回归分析显示, 阿根廷滑柔鱼雄性的精荚长度与胴长和体重均呈显著的正相关关系(图 8), 回归函数式分别为: SL=5.77+0.075ML (R2=0.23, F=128.36, P<0.001)和SL=17.96+0.017BW (R2=0.17, F=86.17, P<0.001)。回归拟合数据集的比较分析显示, 阿根廷滑柔鱼雄性个体的精荚长度与胴长、体重之间的线性关系存在显著性差异(F=33.92, P<0.001)。同时, 精荚长度与胴长、体重的全回归方程为SL=7.63+0.057ML+0.009BW (R2=0.25, F=76.04, P<0.001), 胴长、体重的标准化回归系数分别为0.36 (P<0.001)和0.21 (P<0.001), 表明胴长、体重对精荚长度具有一致的影响关系。
3. 讨论
3.1 个体生物学组成
依据成熟个体大小、产卵季节及其产卵海域分布等, 阿根廷滑柔鱼可以划分为南巴塔哥尼种群(SPS)、布宜诺斯艾利斯—巴塔哥尼种群(BNS)、夏季产卵群(SSS)和春季产卵群(SpSS)等多个群体[5, 20]。其中, SPS种群和BNS种群的成熟个体较大, 平均胴长265 mm左右, 分别在秋季和冬季产卵; SpSS种群在春季产卵时间, 成熟产卵个体较大, 一般为230—350 mm; 而SSS种群的成熟产卵个体最小, 一般在140—250 mm, 在夏季产卵。在本研究中, 阿根廷滑柔鱼个体最大胴长为248 mm, 胴长236 mm、体重286 g以上的全部个体性腺发育成熟; 并且胴长生物学最小型ML50%为207 mm, 体重生物学最小型BW50%为162 g; 胴长和体重的频率分布均表现为一个峰值区间分布。因此, 结合本次样本采集时间为12月至翌年3月份, 可以初步推断本次采集的阿根廷滑柔鱼样本来自于SSS种群。
体重和胴长的幂函数回归分析显示, 本研究阿根廷滑柔鱼雄性个体样本的幂函数参数a值为4.90×10–5, 大于2007—2011年度相同月份采集雄性个体的幂函数参数a值, 这些年份的a值均为10–6[18, 21]。鱼类体重-胴长幂函数回归的a值一般表征个体的营养体征, 与环境因子中的饵料生物丰度密切相关[2]。据此, 可认为本研究样本的渔获年度其海洋环境较往年适宜, 有利于阿根廷滑柔鱼个体的生长发育。同时, 2013年阿根廷滑柔鱼的渔获量为52.54×107 kg, 高于过去十年的平均产量水平44.64×107 kg [22], 也说明该年份的海洋环境比较适宜这些群体的生长。此外, 阿根廷滑柔鱼雄性个体体重-胴长幂函数关系的b值为2.81, 小于往年相同月份采集的雄性个体体重-胴长幂函数关系的b值, 这些年份的b值均在3.0以上[18, 21]。这可能与研究种群的来源密切相关, 因为种群间的生长发育差异性往往导致体重-胴长幂函数关系b值的差异性, 并可作为表征鱼类个体的生长率及其身体形态发育等差异性的指标之一[23]。本研究的阿根廷滑柔鱼种群推断为来源于SSS种群, 而往年的研究种群则为SPS种群或SPS、SSS混合种群[18, 21]。SPS种群个体较大、并且具有更快的生长速率[5]。
3.2 有效繁殖力特性
鱼类繁殖力是渔业资源生物学的重要研究内容, 反映了种群数量变动及其资源量补充过程[1, 2], 而有效繁殖力则可以更直接地表征个体潜在繁殖力的有效部分[3, 4]。一般地, 现生头足类雄性个体具有精荚腺(Spermatophoric gland)和精荚囊(Spermatophoric sac)结构, 在繁殖交配前持续产生并积累精荚[24, 25]。本研究显示, 性腺发育成熟后, 阿根廷滑柔鱼雄性个体的有效繁殖力增加显著(P<0.05), 并且在繁殖交配(Ⅶ期)前达到最大值, 与Arkhipkin等[11]的研究结果一致。Arkhipkin等[11]曾报道阿根廷滑柔鱼雄性成熟个体平均每天可以产生精荚10—20条并持续储存在精荚囊中, 至繁殖交配前精荚囊储存的精荚可达1400条。
同时, 类似于雌性个体繁殖力[26], 头足类雄性个体的有效繁殖力往往与个体大小呈一定的正相关关系, 如虎斑乌贼(Sepia pharaonis)[27]、多氏乌贼(Sepia dollfusi)[27]、狼乌贼(Lycoteuthis lorigera)[28]、科氏滑柔鱼(Illex coindetii)[29]和菱鳍乌贼(Thysanoteuthis rhombus)[30]等。本研究结果显示, 阿根廷滑柔鱼雄性个体的有效繁殖力随着个体生长增加显著(P<0.05)。雄性成熟个体胴长<18 cm时, 其有效繁殖力为200—600条精荚, 在25—31 cm时为1400—1600条精荚[31]。本研究的雄性个体最大有效繁殖力介于这两者之间, 这应该是本研究样本的成熟个体大小介于16—25 cm的原因。此外, 本研究的雄性个体有效繁殖力与体重的相关性更为显著(多元线性回归的标准化系数为0.99), 这可能与较大重量的个体具有较高的体征指标以供给性腺更多的生殖能量密切相关[32, 33], 从而产生更多的精荚。
此外, 与其他头足类相比较, 阿根廷滑柔鱼雄性个体具有较高的最大有效繁殖力, 并且类似于同科属的科氏滑柔鱼[29], 后者的最大有效繁殖力为1555条精荚。其他的如章鱼类最大有效繁殖力为172条精荚[34], 乌贼类的最大有效繁殖力为530条精荚[27], 枪乌贼类的则在200条精荚以内[30, 35, 36]。这是不同种类之间的繁殖生态策略差异性所致。因为章鱼类、乌贼类和枪乌贼类多为营底栖生活, 栖息水域环境相对稳定, 并且雌性个体具有纳精囊或具有存储功能的周口膜储存精荚, 繁殖策略倾向于K策略[26]; 而柔鱼类多为大洋性种类(除了短柔鱼(Todaropsis eblanae)外), 营浮游生活, 精荚多为植入雌性体表或鳃基部, 繁殖策略倾向于r策略[37]。
3.3 有效繁殖力的精荚长度
类似于其他软体动物, 头足类产生数以百万计的精子存储于精荚内[38], 精荚长度大小可以表征个体繁殖对策的遗传性状[1]。一般地, 头足类的精荚长度决定于精荚包装器官—精荚腺的大小, 而精荚腺大小则与个体大小密切相关[35]。本研究结果显示, 阿根廷滑柔鱼雄性个体的精荚长度具有性腺成熟度差异性, 随着性腺发育精荚长度增长显著(P<0.001), 并在繁殖交配(Ⅶ期)前达到最大值, 最大精荚长度为33.14 mm, 略低于Nigmatullin等的36.00 mm[39]。不同成熟度间, 精荚的胴长相对长度不存在显著性差异(P=0.12), 平均为胴长的10.22%, 也略小于Nigmatullin等的11.50%[39]。这应该是本研究的阿根廷滑柔鱼雄性个体小于Nigmatullin等[39]所研究的雄性个体大小所致, 因为较大的个体具有较大的精荚腺以产生较长的精荚[35]。
同时, 阿根廷滑柔鱼雄性个体的精荚长度与胴长、体重均呈显著的线性函数关系, 进一步表明该柔鱼的精荚长度与个体大小密切相关。类似的研究结果在大西洋耳乌贼(Sepiola atlantica)[40]、真枪乌贼(Loligo vulgaris)[41]、福氏枪乌贼(Loligo forbesi)[41]、科氏滑柔鱼[29]、强壮桑椹乌贼(Onykia ingens)[35]等种类中也曾被报道, 这与头足类的精荚产生及其存储的策略选择密切相关。一般地, 头足类生命周期短、性腺成熟至繁殖死亡的时间仅占整个生命周期的1/3时间不到[42]。因此, 头足类自性腺生理性成熟时便开始产生精荚并存储于精荚囊中, 与此同时个体继续生长发育直至性腺功能性成熟期[9—11], 有些种类甚至在繁殖产卵期间继续摄食和生长[35], 随之精荚腺也继续生长并产生更长的精荚[35]。在此时期, 精荚囊则持续存储精荚; 在繁殖期间通过茎化腕输送至雌性纳精囊中, 或植入雌性个体的体表和胴体腔内[39]。因此, 精荚的产生及其长度随着个体生长而变化, 在繁殖交配时产生的精荚长度最大[35, 39]。此外, 栖息环境的优劣也是影响头足类雄性个体精荚长度变化的原因之一[43]。一般地, 良好的环境可带来丰富的饵料生物, 为繁殖群体提供可观的营养物质以供给配子发生; 而环境恶劣时则产生数量多但较短的精荚, 以提高潜在的繁殖机会[35, 43]。
综上所述, 阿根廷滑柔鱼雄性个体的有效繁殖力及其精荚长度与个体的生长发育密切相关。随着性腺生长发育(Ⅳ—Ⅵ期), 两者均显著增加, 前者在功能性成熟期(Ⅵ期)时达到最大值, 并且不同性腺成熟度之间的胴长相对有效繁殖力差异性显著; 后者在繁殖交配期(Ⅶ期)达到最大值, 然而不同成熟度之间精荚的胴长相对长度差异性不显著。同时, 个体有效繁殖力和精荚长度均与胴长、体重呈显著的线性函数关系, 表明个体越大其有效繁殖力越高、精荚长度也越长。回归拟合数据集比较分析和多元线性回归分析进一步显示, 体重对有效繁殖力的影响尤为显著, 而胴长和体重对精荚长度具有一致的影响效应, 表明雄性个体的体征指标越高供给配子发生的生殖投入越大。这可能是短生命周期头足类的共同特性, 是雄性个体自生理性发育开始后便持续产生并积累精荚的选择适应性策略, 以提高潜在的繁殖机会[35, 43]。
此外, 阿根廷滑柔鱼是我国远洋鱿钓渔业中的三大捕捞对象之一[7], 既有研究已经表明该种类因其生命周期短、生命速度快等特点, 其资源生物量取决于补充群体大小[5]。而有效繁殖力直接体现生物个体潜在繁殖力的有效部分[3, 4], 决定着补充群体的数量、质量以及多样性水平的高低, 是群体大小的关键因素[44, 45]。在渔业种群变动及渔业管理上, 繁殖力研究已经成为渔业种群资源评估的基础[46]。因此, 本研究结果也将为今后以繁殖力研究为基础开展资源评估与管理工作提供基础, 为科学合理地、可持续地开发利用该资源提供科学支撑。
-
图版Ⅰ 阿根廷滑柔鱼雄性个体的生殖系统发育
图1—7分别示Ⅰ—Ⅶ性腺成熟度的生殖系统发育形态。其中,Sp表示精荚,SpC表示精荚复合体,SpD表示输精管,SpS表示精荚囊,TeO表示端器,Tes表示精巢
图版Ⅰ. The development of reproductive system in male Illex argentinus
Anatomical examination of 1—7 indicates the development of reproductive system in male Illex argentinus along with sexual maturation. Sp, spermatophore; SpC, spermatophoric complex; SpD, spermaduct; SpS, spermatophoric sac; TeO, terminal organ; Tes, testis
图 5 阿根廷滑柔鱼雄性有效繁殖力和胴长相对有效繁殖力分布
各组平均值上标示的不同字母表示Tukey HSD检验差异显著(P<0.05); 下同
Figure 5. The distribution of effective fecundity and relative effective fecundity by mantle length with sexual maturationin male Illex argentinus
Mean values with different subscripts are significantly different (P<0.05) as determined using Tukey HSD test; the same applies below
-
[1] Hunter J, Macewicz B, Chyan-Huei L N, et al. Fecundity, spawning, and maturity of female Dover sole Microstomus pacificus, with an evaluation of assumptions and precision [J]. Fishery Bulletin, 1992, 90(1): 101—128
[2] 苏锦祥. 鱼类学与海水鱼类养殖(第二版). 北京: 中国农业出版社. 2000, 507 Su J X. Ichthyology and Marine Fishes Aquaculture (2nd edition) [M]. Beijing: China Agriculture Press. 2000, 507
苏锦祥. 鱼类学与海水鱼类养殖(第二版). 北京: 中国农业出版社. 2000, 507[3] Christiansen F B, Fenchel T M. Evolution of marine invertebrate reproductive patterns [J]. Theoretical Population Biology, 1979, 16(3): 267—282
[4] Boletzky S V. Fecundity variation in relation to intermittent or chronic spawning in the cuttlefish, Sepia officinalis L. (Mollusca: Cephalopoda) [J]. Bulletin of Marine Science, 1987, 40(2): 382—387
[5] Rodhouse P G K, Arkhipkin A I, Laptikhovsky V, et al. Illex argentinus, Argentine shortfin squid, in Advances in Squid Biology, Ecology and Fisheries. Part II - Oegopsid squids, R. Rosa, G. Pierce, and R. O’Dor, Editors. Nova Science Publishers: New York. 2013, 109—148
[6] FAO. Review of the State of World Marine Fishery Resources [M]. Rome: Food and Agriculture Organization of the United Nations. 2011, 63—105
[7] 陈新军, 陆化杰, 刘必林, 等. 大洋性柔鱼类资源开发现状及可持续利用的科学问题. 上海海洋大学学报, 2012, 21(5): 831—840 Chen X J, Lu H J, Liu B L, et al. Current exploitation and some scientific issues in the sustainable utilization of Ommastrephidae [J]. Journal of Shanghai Ocean University, 2012, 21(5): 831—840
陈新军, 陆化杰, 刘必林, 等. 大洋性柔鱼类资源开发现状及可持续利用的科学问题. 上海海洋大学学报, 2012, 21(5): 831—840[8] Arkhipkin A I. Squid as nutrient vectors linking Southwest Atlantic marine ecosystems [J]. Deep-Sea Research Part II: Topical Studies in Oceanography, 2013, 95(6): 7—20
[9] Rodhouse P G, Hatfield E M C. Production of soma and gonad in maturing male Illex argentinus (Mollusca: Cephalopoda) [J]. Journal of the Marine Biological Association of the United Kingdom, 1992, 72(2): 293—300
[10] Hatfield E, Rodhouse P, Barber D. Production of soma and gonad in maturing female Illex argentinus (Mollusca: Cephalopoda) [J]. Journal of the Marine Biological Association of the United Kingdom, 1992, 72(2): 281—291
[11] Arkhipkin A, Laptikhovsky V. Seasonal and interannual variability in growth and maturation of winter-spawning Illex argentinus (Cephalopoda: Ommastrephidae) in the Southwest Atlantic[J]. Aquatic Living Resources, 1994, 7(4): 221—232
[12] Santos R A, Haimovici M. Reproductive biology of the winter-spring spawners of Illex argentinus (Cephalopoda: Ommastrephidae) off Southern Brazil [J]. Scientia Marina, 1997, 61(1): 53—64
[13] 林东明, 陈新军, 方舟. 西南大西洋阿根廷滑柔鱼夏季产卵种群繁殖生物学的初步研究. 水产学报, 2014, 38(6): 843—852 Lin D M, Chen X J, Fang Z. Preliminary study on reproductive biology of summer spawning stock of Illex argentinus in the southwestern Atlantic Ocean [J]. Journal of Fisheries of China, 2014, 38(6): 843—852
林东明, 陈新军, 方舟. 西南大西洋阿根廷滑柔鱼夏季产卵种群繁殖生物学的初步研究. 水产学报, 2014, 38(6): 843—852[14] Laptikhovsky V V, Nigmatullin C M. Egg size, fecundity, and spawning in females of the genus Illex (Cephalopoda: Ommastrephidae) [J]. ICES Journal of Marine Science: Journal du Conseil, 1993, 50(4): 393—403
[15] Lin D M, Chen X J, Chen Y, et al. Ovarian development in Argentinean shortfin squid Illex argentinus: group-synchrony for corroboration of intermittent spawning strategy [J]. Hydrobiologia, 2017, 795(1): 327—339
[16] Arkhipkin A. Reproductive system structure, development and function in cephalopods with a new general scale for maturity stages [J]. Journal of Northwest Atlantic Fishery Science, 1992, 12: 63—74.
[17] ICES. Report of the Workshop on Sexual Maturity Staging of Cephalopods, 8—11 November 2010, Livorno, Italy. ICES CM 2010/ACOM:49. 2010, 97
[18] 方舟, 陆化杰, 陈新军, 等. 西南大西洋阿根廷滑柔鱼生物学年间比较. 生态学报, 2012, 32(2): 371—379 Fang Z, Lu H J, Chen X J, et al. Annual variability in biological characteristics of Illex argentinus in the southwest Atlantic Ocean [J]. Acta Ecologica Sinica, 2012, 32(2): 371—379
方舟, 陆化杰, 陈新军, 等. 西南大西洋阿根廷滑柔鱼生物学年间比较. 生态学报, 2012, 32(2): 371—379[19] Zar J H. Biostatistical Analysis, fourth Edition [M]. New Jersey: Prentice Hall. 1999, 960
[20] Jereb P, Roper C F E. Cephalopods of the World. An Annotated and Illustrated Catalogue of Cephalopod Species Known to Date. Volume 2. Myopsid and Oegopsid Squids [M]. Rome: FAO. 2010, 269—347
[21] 刘岩, 张秀梅, 周游, 等. 2011年西南大西洋拖网渔获物阿根廷滑柔鱼生物学分析. 南方水产科学, 2011, 8(3): 39—47 Liu Y, Zhang X, Zhou Y, et al. An analysis of biological characteristics of Argentine shortfin squid Illex argentinus collected by trawl in southwest Atlantic in 2011 [J]. South China Fisheries Science, 2012, 8(3): 39—47
刘岩, 张秀梅, 周游, 等. 2011年西南大西洋拖网渔获物阿根廷滑柔鱼生物学分析. 南方水产科学, 2011, 8(3): 39—47[22] FAO. The State of World Fisheries and Aquaculture 2016. Contributing to Food Security and Nutrition for All [M]. Rome: FAO. 2016, 200
[23] Froese R. Cube law, condition factor and weight–length relationships: history, meta-analysis and recommendations [J]. Journal of Applied Ichthyology, 2006, 22(4): 241—253
[24] Jereb P, Roper C. Cephalopods of the World, an Annotated and Illustrated Catalogue of Cephalopod Species Known to Date. Volume 1. Chambered Nautiluses and Sepioids (Nautilidae, Sepiidae, Sepiolidae, Sepiadariidae, Idiosepiidae and Spirulidae) [M]. Rome: FAO. 2005, 269
[25] 林东明, 陈新军. 头足类生殖系统组织结构研究进展.上海海洋大学学报, 2013, 22(3): 410—418 Lin D M, Chen X J. Research progress on histological structure of reproductive system in cephalopod [J]. Journal of Shanghai Ocean University, 2013, 22(3): 410—418
林东明, 陈新军. 头足类生殖系统组织结构研究进展.上海海洋大学学报, 2013, 22(3): 410—418[26] Boyle P, Rodhouse P. Cephalopods: Ecology and Fisheries [M]. Oxford, UK: Wiley-Blackwell. 2005, 464
[27] Gabr H R, Hanlon R T, Hanafy M H, et al. Maturation, fecundity and seasonality of reproduction of two commercially valuable cuttlefish, Sepia pharaonis and S. dollfusi, in the Suez Canal [J]. Fisheries Research, 1998, 36(2–3): 99—115
[28] Hoving H J T, Laptikhovsky V V, Lipinski M R, et al. Fecundity, oogenesis, and ovulation pattern of southern African Lycoteuthis lorigera (Steenstrup, 1875) [J]. Hydrobiologia, 2014, 725(1): 23—32
[29] Gonzalez A F, Guerra A. Reproductive biology of the short-finned squid Illex coindetii (Cephalopoda: Ommastrephidae) of the Northeastern Atlantic [J]. Sarsia, 1996, 81(2): 107—118
[30] Nigmatullin C M, Arkhipkin A,Sabirov R. Age, growth and reproductive biology of diamond-shaped squid Thysanoteuthis rhombus (Oegopsida: Thysanoteuthidae) [J]. Marine Ecology Progress Series, 1995, 43(5): 73—87
[31] Laptikhovsky V, Nigmatullin C M. Caracteristicas reproductivas de machos y hembras del calamar (Illex argentinus) [J]. Frente Marítimo, 1992, 12(A): 23—37
[32] Lin D M, Chen X J, Wei Y R, et al. The energy accumulation of somatic tissue and reproductive organs in post-recruit female Illex argentinus and the relationship with sea surface oceanography [J]. Fisheries Research, 2017, 185: 102—114
[33] 林东明, 陈新军, 魏嫣然, 等. 阿根廷滑柔鱼雌性个体肌肉和性腺组织能量积累及其生殖投入.水产学报, 2017, 41(1): 70—80 Lin D M, Chen X J, Wei Y R, et al. Energy accumulation of both somatic and reproductive tissues and its allocation to reproduction in Argentinean short-fin squid (Illex argentinus) [J]. Journal of Fisheries of China, 2017, 41(1): 70—80
林东明, 陈新军, 魏嫣然, 等. 阿根廷滑柔鱼雌性个体肌肉和性腺组织能量积累及其生殖投入.水产学报, 2017, 41(1): 70—80[34] Villanueva R. Continuous spawning in the cirrate octopods Opisthoteuthis agassizii and O. vossi: features of sexual maturation defining a reproductive strategy in cephalopods [J]. Marine Biology, 1992, 114(2): 265—275
[35] Hoving H J T, Arkhipkin A I, Laptikhovsky V V, et al. Mating tactics in the sub-Antarctic deep-sea squid Onykia ingens (Cephalopoda: Onychoteuthidae) [J]. Polar Biology, 2016, 39(7): 1319—1328
[36] Hastie L C, Joy J B, Pierce G J, et al. Reproductive biology of Todaropsis eblanae (Cephalopoda: Ommastrephidae) in Scottish waters [J]. Journal of the Marine Biological Association of the United Kingdom, 1994, 74(2): 367—382
[37] Nigmatullin C M, Laptikhovsky V. Reproductive strategies in the squids of the family Ommastrephidae (preliminary report) [J]. Ruthenica, 1994, 4(1): 79—82
[38] Mann T. Spermatophores: Development, Structure, Biochemical Attributes and Role in the Transfer of Spermatozoa [M]. Berlin: Springer Berlin Heidelberg, 1984, 215
[39] Nigmatullin C M, Sabirov R M, Zalygalin V P. Ontogenetic aspects of morphology, size, structure and production of spermatophores in ommastrephid squids: an overview [J]. Berliner Paläobiol. 2003, 3: 225—240
[40] Rodrigues M, Guerra Á,Troncoso J S. Reproduction of the Atlantic bobtail squid Sepiola atlantica (Cephalopoda: Sepiolidae) in northwest Spain [J]. Invertebrate Biology, 2012, 131(1): 30—39
[41] Rocha F, Guerra A. Signs of an extended and intermittent terminal spawning in the squids Loligo vulgaris Lamarck and Loligo forbesi Steenstrup (Cephalopoda: Loliginidae) [J]. Journal of Experimental Marine Biology and Ecology, 1996, 207(1–2): 177—189
[42] Schwarz R, Perez J A A. Age structure and life cycles of the Argentine shortfin squid Illex argentinus (Cephalopoda: Ommastrephidae) in southern Brazil [J]. Journal of the Marine Biological Association of the United Kingdom, 2013, 93(2): 557—565
[43] Laptikhovsky V, Salman A, Önsoy B, et al. Reproduction in rare bathyal octopods Pteroctopus tetracirrhus and Scaeurgus unicirrhus (Cephalopoda: Octopoda) in the east Mediterranean as an apparent response to extremely oligotrophic deep seas [J]. Deep-Sea Research Part I: Oceanographic Research Papers, 2014, 92(1): 85—92
[44] dos Santos Schmidt T C, Slotte A, Kennedy J, et al. Oogenesis and reproductive investment of Atlantic herring are functions of not only present but long-ago environmental influences as well [J]. Proceedings of the National Academy of Sciences, 2017, 114(10): 2634—2639
[45] Lowerre-Barbieri S, DeCelles G, Pepin P, et al. Reproductive resilience: a paradigm shift in understanding spawner-recruit systems in exploited marine fish [J]. Fish and Fisheries, 2017, 18(2): 285—312
[46] Marshall C T, Yaragina N A, Lambert Y, et al. Total lipid energy as a proxy for total egg production by fish stocks [J]. Nature, 1999, 402(6759): 288—290
-
期刊类型引用(11)
1. 吴海珠,陈昭凯,林东明. 海域环境对阿根廷滑柔鱼雌性个体繁殖力特性的影响. 南方水产科学. 2024(01): 130-140 .  百度学术
百度学术
2. 李晓燕,林东明. 阿根廷滑柔鱼肌肉组织的能量密度及能量积累. 上海海洋大学学报. 2024(02): 452-463 .  百度学术
百度学术
3. 王孟佳,徐开达,胡桂森,朱凯. 养殖曼氏无针乌贼雄性个体繁殖特性的研究. 浙江海洋大学学报(自然科学版). 2024(01): 33-40 .  百度学术
百度学术
4. 刘伟,冯艺璇,宋维,林东明. 阿根廷滑柔鱼雄性成熟个体的体征和生殖投入. 渔业科学进展. 2023(05): 11-20 .  百度学术
百度学术
5. 刘连为,隋宥珍,徐开达,徐晓萱,刘姝含,谢慕原,徐汉祥,周永东. 舟山沿岸水域曼氏无针乌贼个体繁殖力特性. 大连海洋大学学报. 2022(03): 457-463 .  百度学术
百度学术
6. 林东明,宣思鹏,陈新军. 头足类鞘亚纲繁殖力研究进展. 海洋渔业. 2021(01): 112-128 .  百度学术
百度学术
7. 臧娜,连晋欣,陈新军,林东明. 阿根廷滑柔鱼年间生长及体征变化. 水生生物学报. 2021(04): 906-916 .  本站查看
本站查看
8. 臧娜,陈新军,林东明. 阿根廷滑柔鱼生长发育和生殖投入的研究现状与展望. 海洋渔业. 2021(05): 626-640 .  百度学术
百度学术
9. 王继隆,刘伟,王维坤,李培伦,杨文波. 绥芬河大麻哈鱼个体生物学研究. 水生生物学报. 2020(01): 162-169 .  本站查看
本站查看
10. 董恩和,黄宝善,石胜旗,黄洪亮,陈新军. 新时代背景下我国远洋鱿钓渔业可持续发展的有关建议. 水产科技情报. 2020(05): 261-265 .  百度学术
百度学术
11. 朱凯,张立川,陈新军,陆化杰,林东明,姚吉祥,马有成. 基于精荚数量对鸢乌贼中型群雄性个体有效繁殖力的研究. 动物学杂志. 2019(04): 517-528 .  百度学术
百度学术
其他类型引用(4)



 下载:
下载: