GROWTH ANALYSIS OF ALL-FEMALE LARGE YELLOW CROAKER IN SINGLE-SEX AQUACULTURE AND THE EFFECTS OF CONTINUOUS COOLING ON ITS TISSUE STRUCTURE, IMMUNE RESPONSES, AND INTESTINAL MICROBIOTA
-
摘要:
为探索全雌养殖大黄鱼(Larimichthys crocea)的生长性能及其对连续降温胁迫的响应, 研究以正常繁殖的后代作为对照组[雌鱼体重: (14.01±2.52) g; 雄鱼体重: (13.87±3.17) g], 以全雌大黄鱼作为全雌养殖实验组[体重: (14.09±2.72) g], 养殖周期120d, 比较对照组雌鱼(CF)、对照组雄鱼(CM)和全雌养殖大黄鱼(AF)的生长性能并分析连续降温胁迫对其鳃和肠道的组织结构、免疫反应及肠道菌群的影响。结果显示, 在30d和60d时, AF的体重与CF和CM相比均无显著差异; 而在120d时, AF的末体重和增重率均显著高于CM, 而与CF无显著差异。进一步的连续降温胁迫实验结果显示, 随着温度的连续降低, CF、CM和AF的鳃细胞均出现空泡化、鳃丝严重变形; 肠细胞融合、杯状细胞肿胀、黏膜细胞坏死和脱落; AF鳃和肠道组织中超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GSH-Px)的活性及丙二醛(MDA)含量与CF和CM变化趋势相同, 均呈现先显著升高后显著降低的趋势; 在6℃时, AF鳃组织中SOD和CAT活性均显著低于CF和CM; AF肠道中CAT、GSH-Px活性及MDA含量也均显著低于CF和CM; 免疫相关基因分析表明, 在6℃时, AF鳃和肠道中IL-6基因的表达量均显著低于CF和CM; 肠道菌群分析表明, 低温胁迫显著影响CF和AF肠道菌群中优势门和优势属的相对丰度, 而对CM无显著影响; 低温胁迫显著影响CF、CM和AF肠道菌群网络结构组成。综上, 全雌养殖大黄鱼具有较快的生长速度; 低温胁迫可导致CF、CM和AF的鳃和肠道组织均出现损伤、氧化应激、炎症反应及显著影响肠道菌群网络结构。研究为大黄鱼全雌养殖模式的进一步研究提供参考依据。
Abstract:This study investigated the growth performance of monosex-cultured all-female large yellow croaker (Larimichthys crocea) and their response to continuous cooling stress. The experimental group consisted of all-female fish (body weight: 14.09±2.72 g), while the control group included naturally reproduced offspring, comprising females (14.01±2.52 g) and males (13.87±3.17 g). Over a period of 120 days, growth performance was compared across groups, and the effects of cooling stress on tissue structure, immune responses, and intestinal microbiota were analyzed. At days 30 and 60, no significant differences in body weight were observed among groups. By day 120, the all-female group exhibited significantly higher body weight and weight gain rate than those of control group males, with no differences compared to the females. Under continuous cooling stress, all groups exhibited vacuolation in gill cells, severe gill filament deformation, intestinal cell fusion, goblet cell swelling, mucosal necrosis, and shedding. Enzyme activities (SOD, CAT, GSH-Px) and MDA content initially increased significantly, followed by a significant decrease. At 6°C, SOD and CAT activities in the gills of the all-female group were significantly lower than those of the control group. Similarly, in the intestine, CAT and GSH-Px activities, along with MDA content, were lower in the all-female group. IL-6 gene expression in the all-female group was also significantly lower than that in the control group. Intestinal microbiota analysis showed that low-temperature stress altered the relative abundance of dominant phyla and genera in the all-female group and control group females, with no significant effect on males. Microbiota network structure changes were observed across all groups. In conclusion, monosex all-female large yellow croaker maintained rapid growth under the monosex farming model. However, low-temperature stress induced tissue damage, oxidative stress, inflammatory responses, and microbiota network alterations in all groups. This study serves as a valuable reference for advancing monosex farming research for large yellow croaker.
-
大黄鱼(Larimichthys crocea)是我国最重要的海水养殖鱼类之一, 其养殖区域遍布我国东南沿海[1], 据《中国渔业统计年鉴》统计, 2023年我国养殖大黄鱼产量已达28.1万吨。大黄鱼雌雄具有明显的生长二态性, 即在相同的生长条件下, 雌鱼生长速度更快[2]。在鱼类中, 性别生长二态性已有相关报道, 如尼罗罗非鱼(Oreochromis niloticus)[3]、金钱鱼(Scatophagus argus)[4]、半滑舌鳎(Cynoglossus semilaevis)[5]、孔雀鱼(Poecilia reticulata)[6]、黄颡鱼(Tachysurus fulvidraco)[7]、牙鲆(Paralichthys olivaceus)[8]等。为了提高鱼类养殖的经济价值, 众多学者开展了鱼类的单性苗种的养殖模式研究。例如, Githukia等[9]报道尼罗罗非鱼单性养殖具有更好的生长性能; Kunda等[3]进一步评估了不同养殖密度条件下单性尼罗罗非鱼的生产性能; Lavrutich等[10]研究表明大西洋鲑(Salmo salar)单性养殖模式下其生长更快、死亡率更低。我们前期利用激素处理结合分子辅助育种技术获得全雌大黄鱼, 并实现了全雌鱼的大规模繁育[2], 但是对于全雌养殖大黄鱼的生长等情况还了解甚少。
鱼类作为变温动物, 极易受到环境温度的影响[11], 具体表现为器官组织损伤、多器官功能障碍、免疫和代谢抑制等[12]。大黄鱼具有较强的温度敏感性, 对低温尤为敏感, 当养殖水温低于10℃时, 其活动量和摄食量开始下降[13]; 当水温低于7℃时, 大黄鱼开始出现大量死亡[14]。目前, 关于大黄鱼低温应激已有相关研究, 如Suo等[15]利用全基因组关联分析探索了低温胁迫下大黄鱼鳃中相关基因的差异表达; Lv等[16]研究表明在实验室条件下, 低温胁迫后大黄鱼肝脏中抗氧化酶活性显著增加, 而肠道菌群组成没有明显变化; Cen等[1]研究表明网箱养殖大黄鱼越冬前后其肠道结构和免疫相关基因表达及肠道菌群组成均出现显著的性别差异。虽然, 上述研究分析了低温胁迫对大黄鱼的生长、摄食和生理生化指标的影响, 但对于全雌养殖大黄鱼低温胁迫后的相关生理响应变化尚未涉及。
本实验以全雌大黄鱼为单性养殖研究对象, 探究其单性养殖模式下的生长性能及低温胁迫下鳃和肠道组织结构、氧化应激指标、相关免疫基因及肠道菌群响应变化; 研究结果以期为大黄鱼单性养殖模式的构建提供科学依据。
1. 材料与方法
1.1 实验鱼
实验所用的对照组大黄鱼和全雌大黄鱼均由浙江省舟山市水产研究所自主繁育获得; 养殖实验在浙江省舟山市水产研究所朱家尖基地开展; 对照组为正常繁殖的后代; 全雌大黄鱼培育方法: 首先利用紫外灭活大黄鱼精子中的遗传物质, 然后再与大黄鱼卵子进行受精, 接着利用冷休克的方法进行染色体加倍, 诱导其雌核发育; 利用来曲唑对雌核发育大黄鱼进行性逆转诱导, 培育伪雄鱼; 利用伪雄鱼与正常大黄鱼雌鱼进行交配, 培育出全雌大黄鱼。对照组大黄鱼和全雌大黄鱼均为同批次繁育获得。
1.2 实验设计和样品采集
从养殖池中(4 m ×5 m ×1.2 m)挑选健康、规格相近的对照组大黄鱼和全雌大黄鱼各1500尾, 对照组雌鱼(CF)和对照组雄鱼(CM)初始体重和体长分别为(14.01±2.52) g和(9.13±0.78) cm、(13.87±3.17) g和(9.22±0.64) cm; 实验组全雌鱼(AF)的初始体重和体长分别为(14.09±2.72) g和(9.66±0.68) cm; 对照组经性腺组织切片鉴定性别。对照组和实验组各设3个平行, 每桶500尾(1吨桶: 圆桶形, 直径1.2 m, 高度0.9 m), 连续充气, 流水养殖, 每天早上9点和下午3点投喂饲料, 每天投喂前吸出残饵粪便, 并且换水50%。饲料成分由粗蛋白质(≥40.0%)、粗脂肪(≥6.0%)、粗纤维(≤4.0%)、粗灰分(≤16.0%)、总磷(≥1.2%)、水分(≤12.0%)和赖氨酸(≥2.1%)等组成。养殖时间从2023年7月25日至2023年11月22日, 共计120d, 养殖期间, 分别于第30、第60和第120天时从每个平行各取50尾鱼进行生长测定; 在第30和第60天时, 通过性腺组织切片鉴定对照组大黄鱼的性别; 在第120天时, 通过解剖观察来确定对照组大黄鱼的性别。为保持实验过程中每桶鱼的数量一致, 对照组和全雌养殖大黄鱼组在各取样时间点均随机取样50尾鱼。生长指标包括体重(g)、体长(cm)、增重率(%)、特定生长率(%/d)、肥满度(g/cm3)和饲料系数, 计算公式:
增重率(%)=(末体重–初体重)/初体重×100
特定生长率(%/d)=(ln末体重–ln初体重)/养殖时间
肥满度(g/cm3)=体重/体长3
饲料系数=摄食饲料总重/(末体重−初体重)
在养殖结束后, 随后随机挑选健康、规格相近的对照组大黄鱼和全雌大黄鱼各240尾[CF体重(67.04±4.31) g; CM体重(66.03±4.15) g; AF体重(69.67±3.36) g], 放置于6个1吨桶内(圆桶形, 直径1.2 m, 高度0.9 m), 每桶80尾, 进行连续降温胁迫实验。实验开始前, 水温为13.6℃, 大黄鱼在12℃时依然可以正常摄食和游动[16], 因此, 连续降温实验起始温度设置为12℃。实验温度从12℃急性降温(2℃/h)至6℃, 然后再恢复至12℃, 分别在12、10、8、6℃和恢复后的12℃维持2h后, 采集鳃和肠道样品进行组织结构、抗氧化酶活性、相关免疫基因表达及肠道菌群分析。
鳃和肠道样品采集: 采用MS-222快速麻醉鱼体后用无菌剪刀解剖, 采集鳃和肠道样品, 其中部分鳃和肠道样品用Bouin’s固定液固定, 用于组织结构观察; 部分鳃和肠道样品置于RNA保护液中, 用于相关免疫基因表达分析; 部分鳃和肠道样品保存至-80℃冰箱, 用于非特异性免疫酶活性测定; 在12℃和6℃时, 采集中肠内容物: 首先用75%酒精消毒鱼体表面, 然后用无菌剪刀解剖鱼体, 随后将中肠转移至无菌培养皿中, 接着用无菌剪刀解剖, 用无菌生理盐水冲洗中肠, 将全部内容物收集于2 mL无菌管中; 每个实验桶中的3尾鱼的中肠肠道内容物进行混合后作为1个样品; 样品先于液氮中冷冻, 然后保存于-80℃冰箱, 用于肠道菌群分析。
1.3 鳃和肠道的组织学观察
鳃和肠道组织样品于Bouin’s固定液中固定24h后, 转移到70%乙醇中, 经脱水、包埋后切片, 切片厚度为5 μm, 然后经苏木精-伊红(HE)染色和中性树胶封片后对鳃和肠道组织学切片进行拍照观察。
1.4 抗氧化酶活指标分析
超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GSH-Px)活性和丙二醛(MDA)含量的测定均使用南京建成生物工程研究所的试剂盒, 测定具体操作步骤参照说明书。测定时, 分别取鳃和肠道组织约0.1 g, 按质量体积比1﹕9加入预冷的生理盐水, 在冰上充分匀浆, 然后4℃ 2500 r/min离心15min, 取上清液用于酶活性检测。利用酶标仪(伯腾, 美国)测定其吸光值, 根据标准曲线计算每个样品的SOD、CAT、GSH-Px活性和MDA含量, 每个样品重复测定3次。
1.5 总RNA提取和荧光定量PCR实验
采用总RNA提取试剂盒(索莱宝, 北京)提取鳃和肠道组织总RNA样品, 并检测总RNA纯度和质量。然后用PrimescriptTM RT试剂盒(宝生物, 日本)将提取的总RNA反转录成cDNA。测定鳃组织和肠道组织中IL-6、TNF-α、HSP70和HSP90基因的表达, 使用的引物序列见表 1。荧光定量PCR反应体系为20 μL: 2×ChamQ Universal SYBR qPCR Master Mix 10 μL, 上下游引物各0.4 μL, Template cDNA 2 μL, ddH2O 7.2 μL; 扩增程序为: 95℃预变性30s, 95℃变性10s, 60℃退火30s, 共40个循环, 熔解曲线95℃ 15s, 60℃退火60s, 95℃ 15s, 基因相对表达量采用2–∆∆Ct方法进行计算。
表 1 荧光定量引物Table 1. RT-qPCR primers引物
Primer引物序列
Primer sequence (5′—3′)来源
SourceIL-6-F TGAAGGCTCCGACGAAATG Cen et al.[1] IL-6-R GTCCAGTAGGCTAAACTGCTATC Cen et al.[1] TNF-α-F CGTCGTTCAGAGTCTCCTGC Tan et al.[17] TNF-α-R TGTACCACCCGTGTCCCACT Tan et al.[17] HSP70-F CGCAGTCATCACAGTTCCG Lv et al.[16] HSP70-R TGCCGTCTTCAATGGTCAG Lv et al.[16] HSP90-F CCGCTACGAAAGCCTGACTGA Lv et al.[16] HSP90-R ACGACCACCTTCTCGGCAAC Lv et al.[16] β-actin-F GACCTGACAGACTACCTCATG Tan et al.[17] β-actin-R AGTTGAAGGTGGTCTCGTGGA Tan et al.[17] 1.6 肠道菌群16S rRNA高通量测序
肠道内容物样品用干冰保存送至上海美吉生物医药科技有限公司进行16S rRNA高通量测序。基于Illumina平台, 利用Barcode特异引物343F (5′-TACGGRAGGCAGCAG-3′)和798R (5′-AGGGTATCTAATCCT-3′)扩增16S rRNA基因的V3—V4区。
首先对原始Reads序列进行质控和过滤, 然后利用DADA2软件进行序列降噪处理以获得有效序列; 基于Silva (v. 138)数据库, 利用q2-feature-classifier软件进行序列比对和注释, 获得ASV (Amplicon Sequence Variant)代表序列和丰度信息。利用QIIME2软件进行PCoA (principal co-ordinates analysis)分析、Alpha多样性分析和Beta多样性分析; 利用R软件, 基于vegan包进行多元方差分析(Permutational Multivariate Analysis of Variance, PERMANOVA)和相似性分析(Analysis of Similarity, ANOSIM)。利用随机矩阵理论构建肠道菌群网络, 基于fast greedy modularity optimization方法进行网络模块化分析; 利用Cytoscape (v. 3.10.2)软件对肠道菌群网络进行可视化分析。
1.7 数据分析
所得数据均以平均值±标准误表示; 利用SPSS 23软件对生长指标、抗氧化酶活性和相关免疫基因表达数据进行单因素方差分析(One-way ANOVA)和Duncan’s多重比较分析。肠道菌群数据采用Kruskal Wallis检验进行比较分析。P<0.05表示差异显著。
2. 结果
2.1 全雌养殖大黄鱼生长指标比较分析
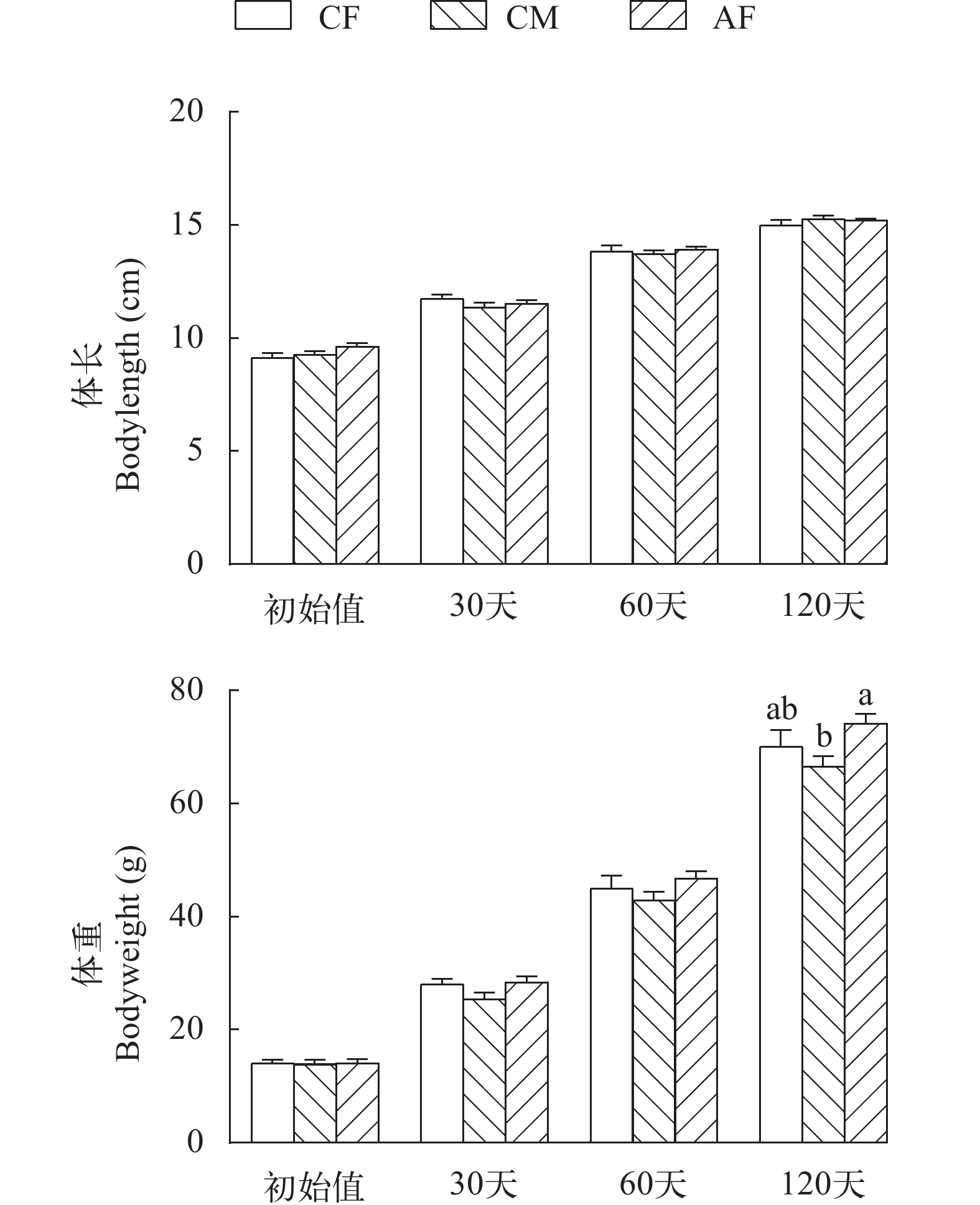
实验鱼养殖120d后, 对照组大黄鱼和全雌大黄鱼的成活率均在95%以上。由图 1可知, 在各取样时间点AF的体长与CF和CM相比没有显著差异(P>0.05); 在30d和60d时, CF、CM和AF之间体重均无显著差异(P>0.05), 而在120d时, AF的体重显著高于CM (P<0.05), 而与CF无显著差异(P>0.05); CF与CM的体重无显著差异(P>0.05)。由表 2可知, AF的末体重和增重率均显著高于CM (P<0.05), 而与CF无显著差异(P>0.05); CF与CM的末体重和增重率均无显著差异(P>0.05); CF和AF的肥满度均显著高于CM (P<0.05); 全雌养殖大黄鱼的饲料系数显著低于对照组大黄鱼(P<0.05)。
表 2 对照组和全雌养殖大黄鱼的生长指标Table 2. The growth indexes of control group and all-female culture of L. crocea组别
Group初体重
Initial body
Weight (g)末体重
Final body
Weight (g)增重率
Weight gain
rate (%)特定生长率
Specific growth
rate (%/d)肥满度
Condition factor
(g/cm3)饲料系数
Feed conversion
ratioCF 14.01±2.52 70.04±11.37ab 401.45±24.83ab 1.34±0.04 2.09±0.28a 1.47±0.14a CM 13.87±3.17 66.56±7.00b 390.45±49.50b 1.32±0.09 1.88±0.17b AF 14.09±2.72 74.16±6.39a 438.04±66.52a 1.40±0.23 2.11±0.17a 1.35±0.26b 注: 同列不同小写字母表示差异显著(P<0.05)Note: Different lowercase letters in the same column indicate significant differences (P<0.05) 2.2 连续降温对大黄鱼鳃和肠道组织学结构的影响
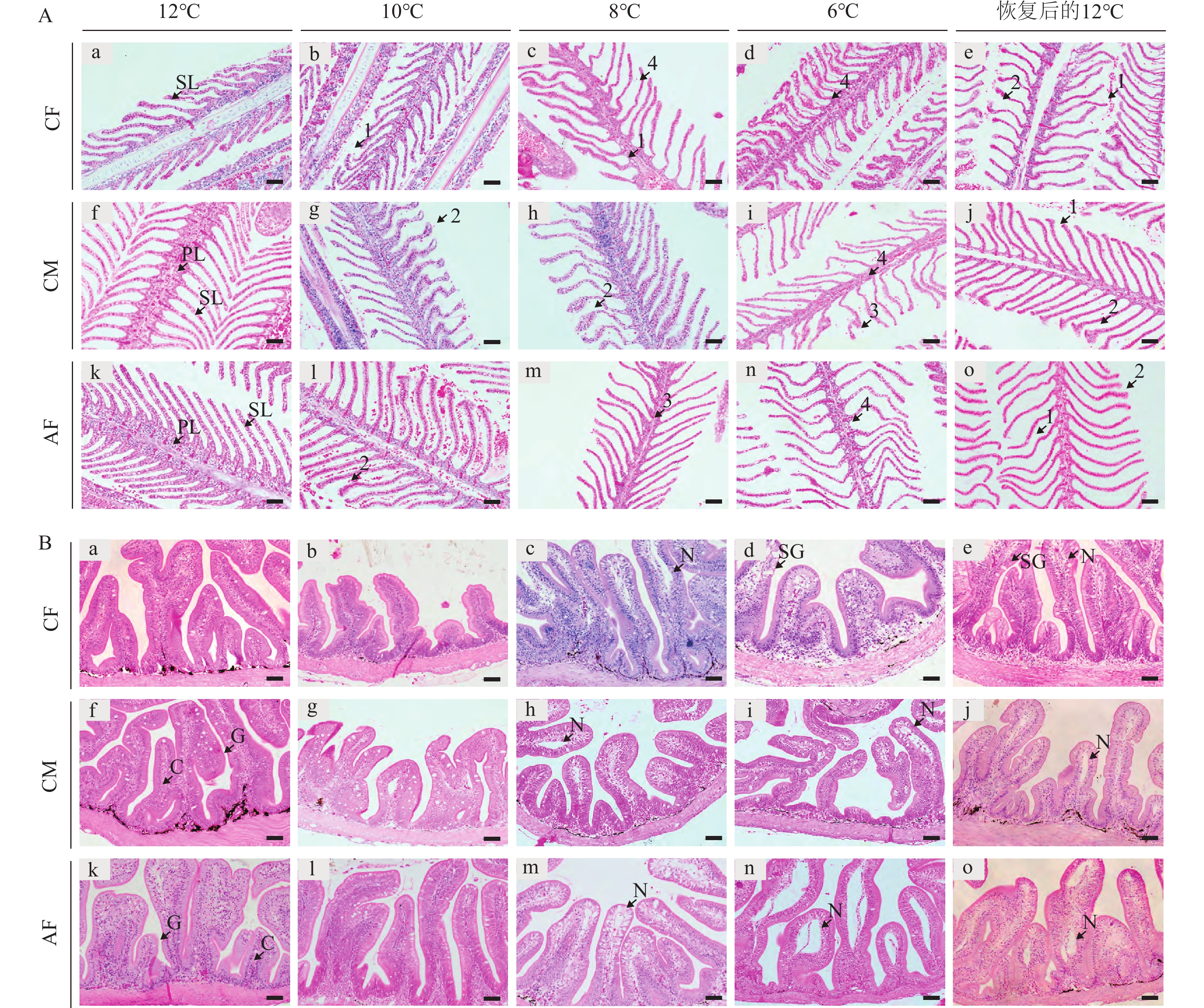
连续降温对CF、CM和AF的鳃和肠道组织的影响如图 2所示。在12℃时, CF、CM和AF的鳃丝均未见病变现象, 细胞核清晰可见, 排布均匀, 泌氯细胞和上皮细胞排列致密有序, 鳃丝结构完整, 两侧鳃小片排列整齐规律; 在10℃和8℃时, CF、CM和AF的鳃丝部分上皮细胞均出现水肿和末端轻微弯曲, 鳃丝细胞出现空泡化; 在6℃时, CF、CM和AF的鳃细胞空泡化严重, 鳃丝严重变形(图 2A)。
![]() 图 2 低温胁迫对大黄鱼鳃(A)和肠道(B)组织显微结构的影响(×200, 比例尺=50 μm)SL. 鳃小片; PL. 鳃丝; 1. 鳃小片末端弯曲; 2. 上皮细胞水肿; 3. 细胞空泡化。C. 柱状细胞; G. 杯状细胞; SG. 杯状细胞肿胀; N. 黏膜层坏死Figure 2. Effects of low temperature stress on the gill (A) and intestine (B) structure in L. crocea (×200, scale bar=50 μm)SL. Secondary lamella; PL. Primary lamellae; 1. Curved tips and hyperemia at ending; 2. Epithelial oedema; 3. Cellular vacuolation; C. Columnar cell; G. Goblet cell; SG. Swelling of goblet cell; N. Necrosis in the mucosal layer
图 2 低温胁迫对大黄鱼鳃(A)和肠道(B)组织显微结构的影响(×200, 比例尺=50 μm)SL. 鳃小片; PL. 鳃丝; 1. 鳃小片末端弯曲; 2. 上皮细胞水肿; 3. 细胞空泡化。C. 柱状细胞; G. 杯状细胞; SG. 杯状细胞肿胀; N. 黏膜层坏死Figure 2. Effects of low temperature stress on the gill (A) and intestine (B) structure in L. crocea (×200, scale bar=50 μm)SL. Secondary lamella; PL. Primary lamellae; 1. Curved tips and hyperemia at ending; 2. Epithelial oedema; 3. Cellular vacuolation; C. Columnar cell; G. Goblet cell; SG. Swelling of goblet cell; N. Necrosis in the mucosal layer在12℃和10℃时, CF、CM和AF肠道组织结构完整清晰, 上皮细胞排列有序, 没有明显的病变现象; 而在8℃和6℃时, CF、CM和AF均出现肠细胞融合、杯状细胞肿胀、黏膜细胞坏死和脱落现象(图 2B)。
2.3 连续降温对大黄鱼鳃和肠道抗氧化酶活性的影响
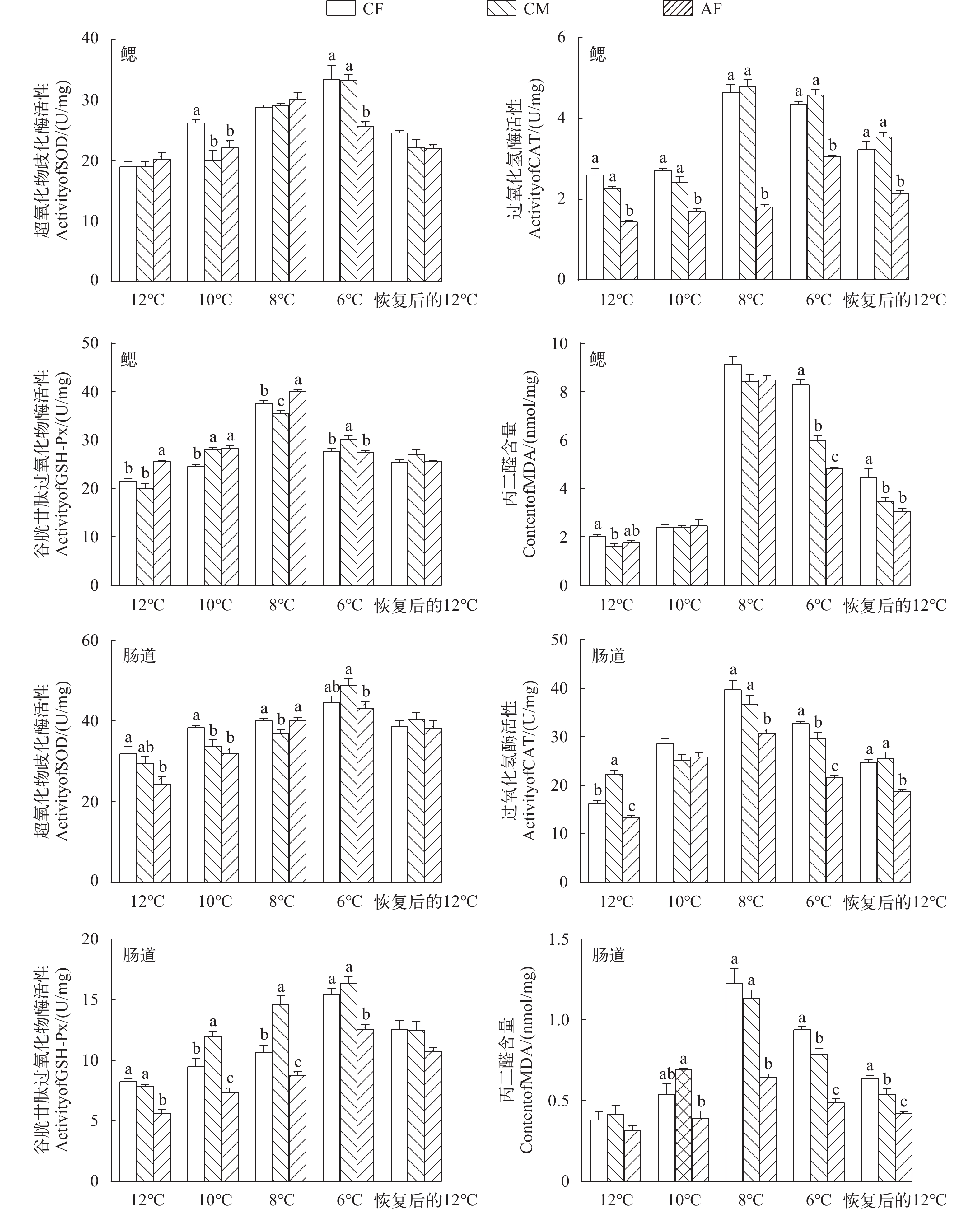
连续降温对CF、CM和AF的鳃和肠道组织的抗氧化酶活性的影响如图 3所示。连续降温期间, CF、CM和AF的鳃中SOD、CAT、GSH-Px活性和MDA含量均呈现先显著升高后显著降低的趋势; 在6℃时, AF鳃中SOD活性显著低于CF和CM (P<0.05)。AF鳃中CAT活性在12℃、10℃、8℃、6℃和恢复后的12℃时均显著低于CF和CM (P<0.05), CF和CM间差异不显著(P>0.05)。AF鳃中GSH-Px活性在12℃和8℃时均显著高于CF和CM (P<0.05)。CF鳃中MDA含量在6℃和恢复后的12℃时均显著高于CM和AF (P<0.05); 而在10℃和8℃时, CF、CM和AF间差异不显著(P>0.05)。
![]() 图 3 低温胁迫对大黄鱼鳃和肠道组织超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶活性及丙二醛含量的影响图上不同小写字母表示相同温度下不同组间差异显著(P<0.05); 下同Figure 3. Effects of low temperature stress on the activities of SOD, CAT, GSH-Px, and MDA content in gill and intestine of L. croceaDifferent lowercase letters on the graph indicate significant differences in groups at the same temperature (P<0.05); The same applies below
图 3 低温胁迫对大黄鱼鳃和肠道组织超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶活性及丙二醛含量的影响图上不同小写字母表示相同温度下不同组间差异显著(P<0.05); 下同Figure 3. Effects of low temperature stress on the activities of SOD, CAT, GSH-Px, and MDA content in gill and intestine of L. croceaDifferent lowercase letters on the graph indicate significant differences in groups at the same temperature (P<0.05); The same applies below连续降温期间, CF、CM和AF的肠道中SOD、CAT、GSH-Px活性和MDA含量均呈现先显著升高后显著降低的趋势(P<0.05)。CF肠道中SOD活性在12℃和10℃时均显著高于AF (P<0.05)。AF肠道中CAT活性在12℃、8℃、6℃和恢复后的12℃时均显著低于CF和CM (P<0.05)。AF肠道中GSH-Px活性在12℃、10℃、8℃和6℃时均显著低于CF与CM (P<0.05)。AF肠道中MDA含量在8℃、6℃和恢复后的12℃时均显著低于CF与CM (P<0.05)。
2.4 连续降温对大黄鱼鳃和肠道相关免疫基因表达的影响
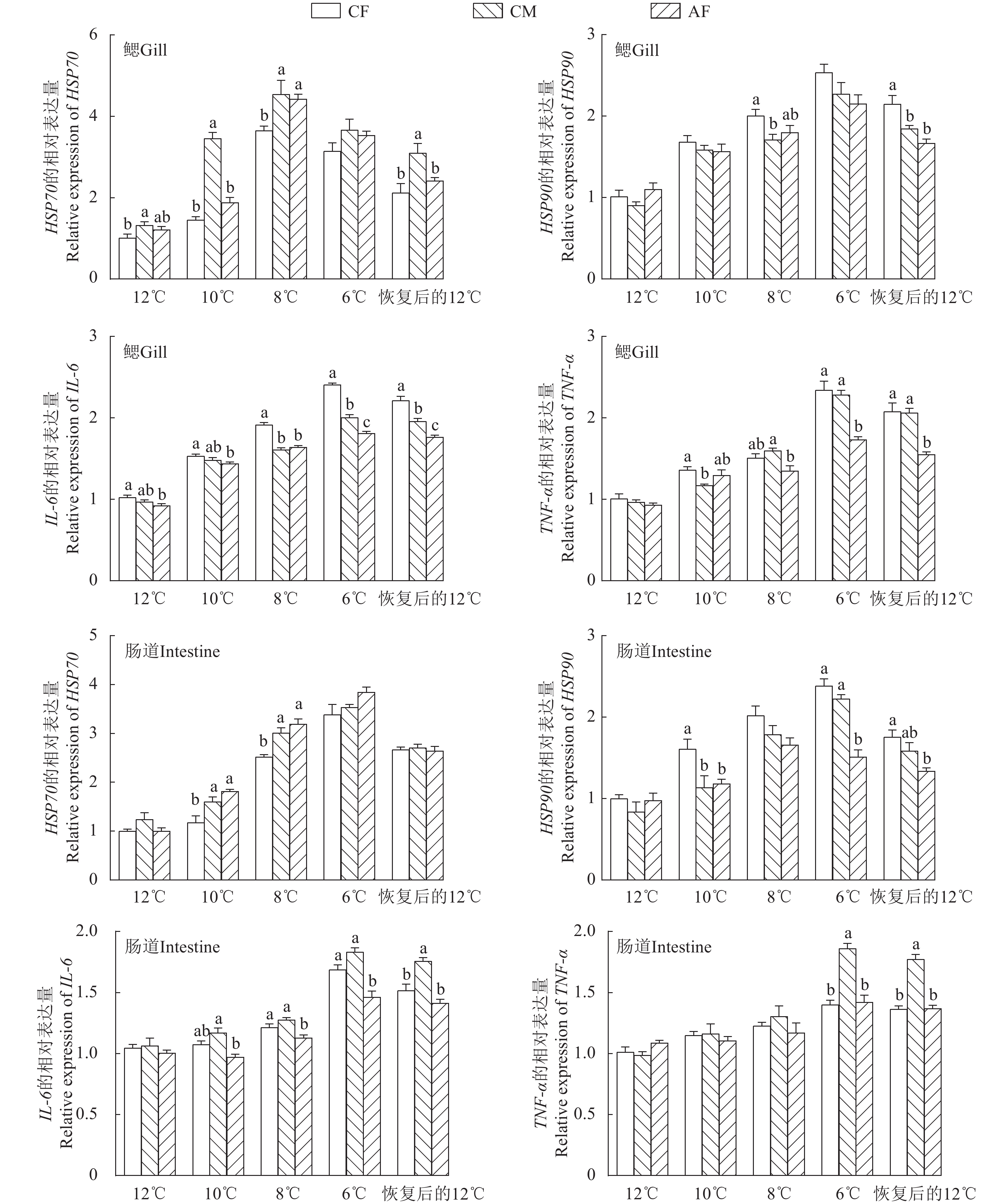
连续降温对CF、CM和AF的鳃和肠道中HSP70和HSP90基因表达量的影响如图 4所示。连续降温期间, CF、CM和AF的鳃和肠道中HSP70基因表达水平均呈现先显著升高后显著降低的趋势, 而HSP90基因表达水平呈现显著升高趋势。CF鳃中HSP70基因表达量在12℃、10℃和8℃时均显著低于CM和AF (P<0.05); CM鳃中HSP70基因表达量在10℃和恢复后的12℃时均显著高于AF。AF鳃中HSP90基因表达量在12℃、8℃和6℃时与CF与CM相比无显著差异(P>0.05)。CM和AF肠道中HSP70基因表达量在10℃和8℃时均显著高于CF (P<0.05)。AF肠道中HSP90基因表达量在10℃、6℃和恢复后的12℃时均显著低于CF (P<0.05)。
连续降温期间, CF、CM和AF的鳃和肠道中IL-6和TNF-α基因表达量均显著升高(P<0.05)。CF与CM鳃中IL-6基因表达量在8℃和6℃时均显著高于AF (P<0.05), 而CF与CM间差异不显著(P>0.05)。CF和AF鳃中TNF-α基因表达量在6℃和恢复后的12℃时均显著高于CM (P<0.05)。CF与CM肠道中IL-6基因表达量在8℃和6℃时均显著高于AF (P<0.05)。CM肠道中TNF-α基因表达量在6℃和恢复后的12℃时均显著高于CF和AF (P<0.05); 而CF肠道中TNF-α基因表达量在12℃、10℃、8℃、6℃和恢复后的12℃时与AF相比均无显著差异(P>0.05)。
2.5 低温胁迫对大黄鱼肠道菌群的影响
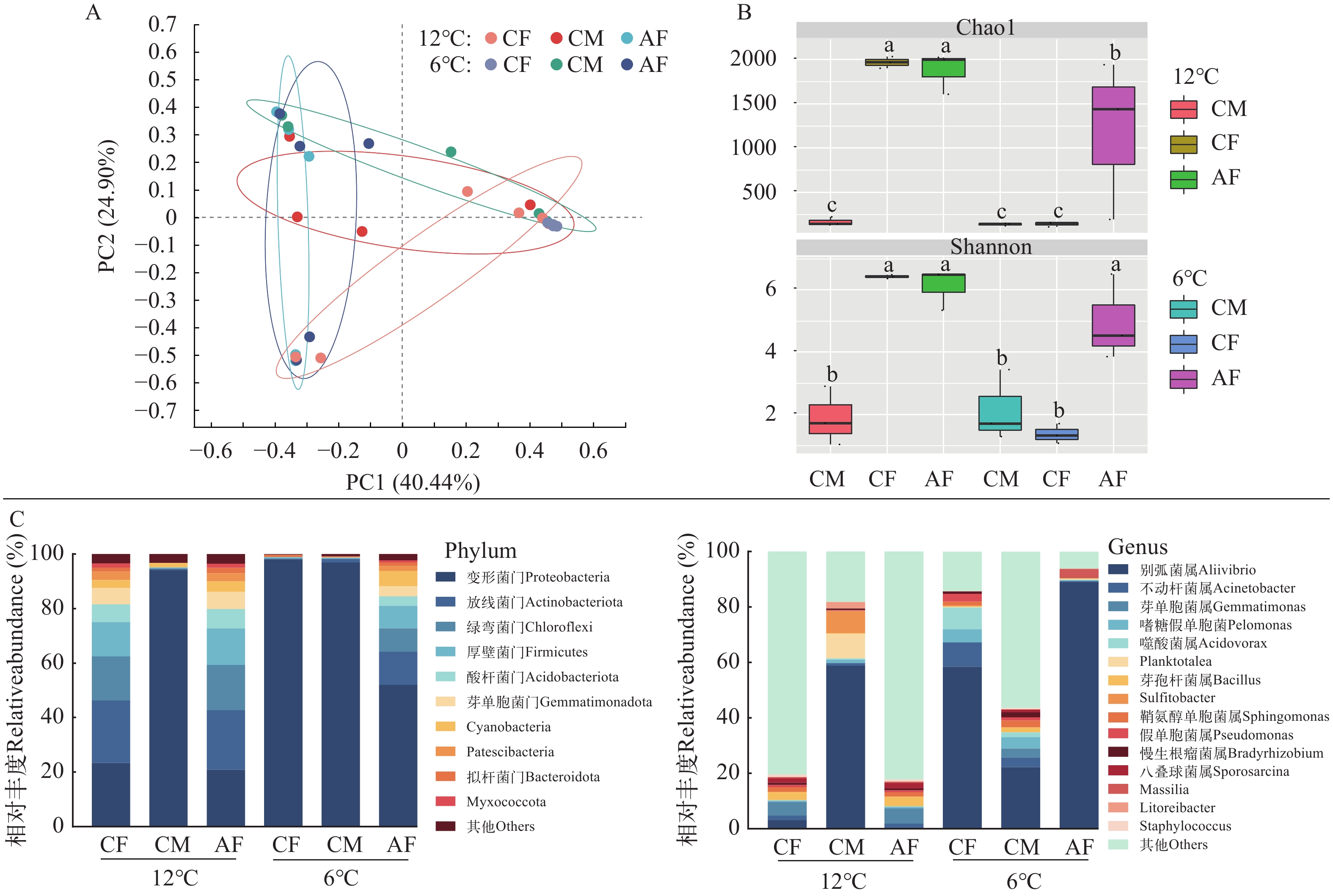
低温胁迫对大黄鱼肠道菌群多样性和组成的影响 低温胁迫对CF、CM和AF肠道菌群的影响如图 5所示。PCoA分析可知(图 5A), 低温胁迫下CF、CM和AF的肠道菌群组成没有明显的分布规律。进一步的PERMANOVA分析和ANOSIM分析表明(表 3), 低温胁迫下CF肠道菌群结构显著改变(P<0.05), 而CM和AF肠道菌群结构没有显著变化(P>0.05)。如图 5B所示, 低温胁迫后, CF肠道菌群中Chao1指数和Shannon指数均显著降低(P<0.05); CM肠道菌群中Chao1指数和Shannon指数均无显著变化(P>0.05); AF肠道菌群中Chao1指数显著降低(P<0.05), 而Shannon指数无显著变化(P>0.05)。此外, 双因素方差分析结果显示(表 4), 大黄鱼肠道菌群中Chao1指数和Shannon指数均存在显著的性别差异(Chao1: F=1.380, P=0.018; Shannon: F=3.912, P=0.001), 而没有显著温度差异(Chao1: F=1.184, P=0.148; Shannon: F=1.523, P=0.170); Chao1指数和Shannon指数在性别和温度上未表现出显著的交互作用(Chao1: F=1.081, P=0.253; Shannon: F=0.809, P=0.594)。
![]() 图 5 低温胁迫对大黄鱼肠道菌群多样性和组成的影响A.肠道菌群主坐标分析(PCoA); B.肠道菌群α-多样性分析; C.肠道菌群在门水平和属水平上的组成Figure 5. Effect of low temperature stress on the diversity and composition of the intestinal microbiota in L. croceaA. The principal co-ordinates analysis of the intestinal microbiota; B. the α-diversity of the intestinal microbiota; C. the composition of the intestinal microbiota at phylum- and genus-level表 3 低温胁迫下对照组雌鱼、对照组雄鱼和全雌鱼肠道菌群差异分析Table 3. Differences in the intestinal microbiota among females, males, and all-females were analyzed under low-temperature stress
图 5 低温胁迫对大黄鱼肠道菌群多样性和组成的影响A.肠道菌群主坐标分析(PCoA); B.肠道菌群α-多样性分析; C.肠道菌群在门水平和属水平上的组成Figure 5. Effect of low temperature stress on the diversity and composition of the intestinal microbiota in L. croceaA. The principal co-ordinates analysis of the intestinal microbiota; B. the α-diversity of the intestinal microbiota; C. the composition of the intestinal microbiota at phylum- and genus-level表 3 低温胁迫下对照组雌鱼、对照组雄鱼和全雌鱼肠道菌群差异分析Table 3. Differences in the intestinal microbiota among females, males, and all-females were analyzed under low-temperature stress性别 温度/℃ Bray-Curtis distance PERMANOVA ANOSIM F P R P 雌鱼 12 vs. 6 1.550 0.010 0.060 0.004 雄鱼 12 vs. 6 1.051 0.268 0.436 0.226 全雌鱼 12 vs. 6 0.771 0.728 0.108 0.628 表 4 基于双因素方差分析比较不同性别和温度的α-多样性指数Table 4. Comparison of α-diversity indexes in sex and temperature based on two-way ANOVA testTwo-way ANOVA test Chao1 Shannon F P F P 性别(雌, 雄, 全雌) 1.380 0.018* 3.912 0.001* 温度(12, 6) 1.184 0.148 1.523 0.170 性别×温度 1.081 0.253 0.809 0.594 注: *代表差异显著Note: * indicate significant differences 低温胁迫对大黄鱼肠道菌群组成的影响如图 5C所示。在门水平上, 在12℃时, CF和AF肠道菌群中优势菌门均为变形菌门(Proteobacteria)[CF: (23.39±0.95)%; AF: (20.91±0.39)%]和放线菌门(Actinobacteriota)[CF: (22.89±0.11)%; AF: (21.79±0.22%)]; 而CM为变形菌门[(94.2±2.75)%]; 在6℃时, CF、CM和AF肠道菌群中优势菌门均为变形菌门[CF: (98.04±0.76)%; CM: (96.88±1.28)%; AF: (52.03±17.05)%]。进一步的统计学分析显示, 低温胁迫后CF和AF肠道菌群中变形菌门的相对丰度均显著增加(P<0.05), 而放线菌门的相对丰度均显著降低(P<0.05); CM肠道菌群中变形菌门的相对丰度无显著变化(P>0.05)。在属水平上, 在12℃时, CF和AF肠道菌群中优势菌属均为芽单胞菌属(Gemmatimonas)[CF: (4.95±0.11)%; AF: (5.49±0.19%)]; 而在CM中为别弧菌属(Aliivibrio)[(58.83±29.67)%]; 在6℃时, CF、CM和AF肠道菌群中优势菌属均为别弧菌属[CF: (89.07±6.55)%; CM: (58.44±29.06)%; AF: (22.24±2.95%)]; 进一步的统计学分析显示, 在低温胁迫后, CF和AF肠道菌群中别弧菌属的相对丰度均显著增加(P<0.05), 而CM无显著变化(P>0.05)。
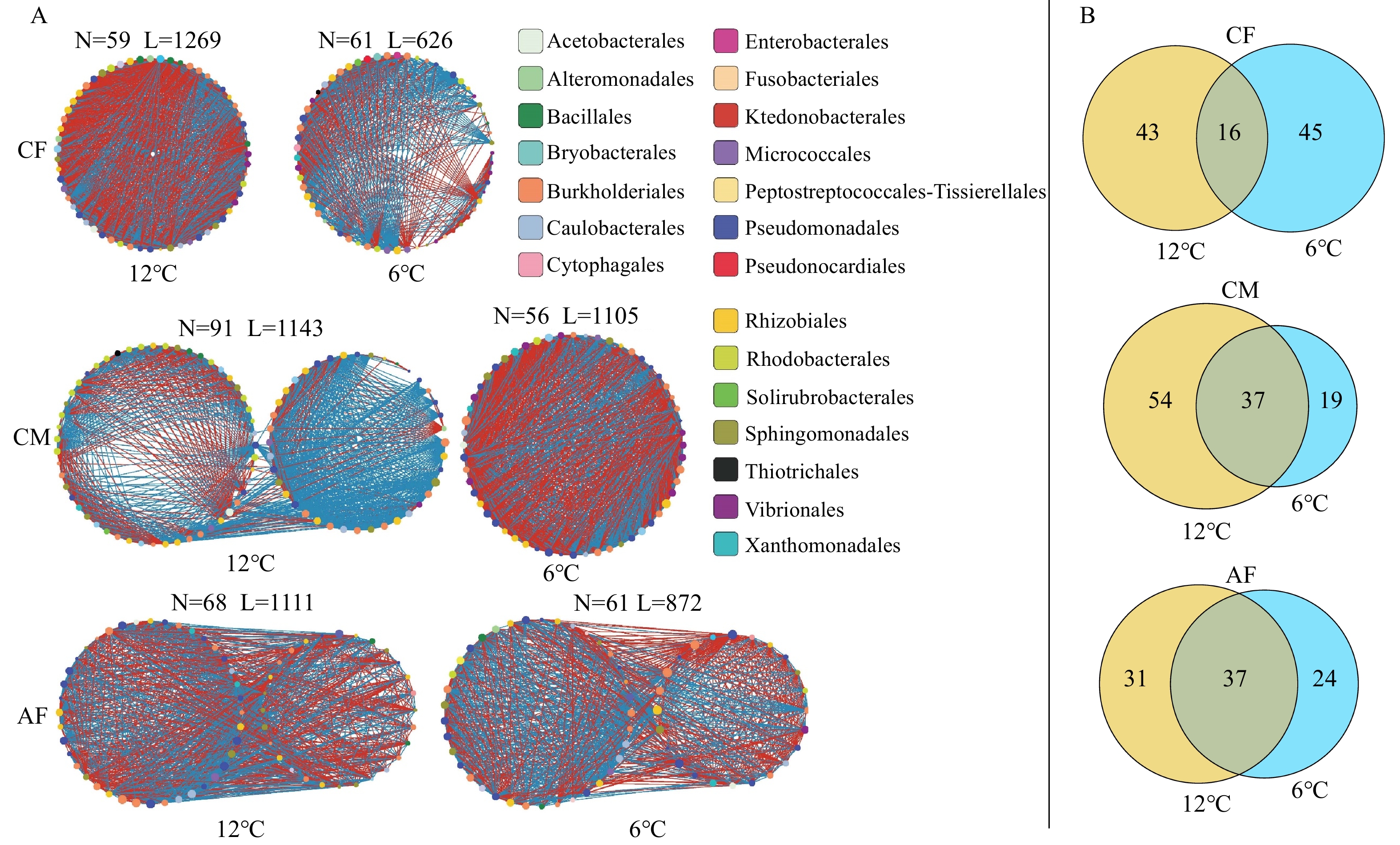
低温胁迫对大黄鱼肠道菌群网络结构的影响 低温胁迫对大黄鱼肠道菌群网络结构的影响如图 6所示。如图 6A所示, 图中每一个节点代表一个ASV, 节点大小代表物种间连接度大小; 红色连线代表两个物种间是消极关系, 如竞争关系等; 蓝色连线代表两个物种间是积极关系, 如互补关系等。在12℃时, CF肠道菌群网络由59个ASVs和1269个连线(红色: 481, 蓝色: 788)组成; CM肠道菌群网络由91个ASVs和1143个连线(红色: 791, 蓝色: 352)组成; AF肠道菌群网络由68个ASVs和1111个连线(红色: 572, 蓝色: 539)组成; 在6℃时, CF肠道菌群网络由61个ASVs和626个连线(红色: 370, 蓝色: 256)组成; CM肠道菌群网络由56个ASVs和1105个连线(红色: 669, 蓝色: 436)组成; AF肠道菌群网络由61个ASVs和872个连线(红色: 402, 蓝色: 470)组成。由图 6B可知, 在12℃和6℃条件下, CF、CM和AF肠道菌群网络中共有ASVs数量分别为37、16和37个, 共有ASVs主要隶属于Pseudomonadales(假单胞菌目)和Burkholderiales(伯克霍尔德氏菌目)。进一步网络结构差异分析如表 5所示, 低温胁迫后, CF、CM和AF肠道菌群网络结构均发生了显著的变化(P<0.05)。综上可知, 在低温胁迫下, CF和AF肠道菌群网络结构出现物种间互作关系减弱, 而CM肠道菌群网络模块出现重组现象; 此外, 低温胁迫诱导CF、CM和AF肠道菌群网络结构显著改变。
表 5 低温胁迫下对照组雌鱼、对照组雄鱼和全雌鱼肠道菌群网络结构差异分析Table 5. The networked community differences among females, males, and all-females were analyzed under low-temperature stress性别 温度/℃ Bray-Curtis distance PERMANOVA ANOSIM F P R P 雌鱼 12 vs. 6 11.134 0.014 1.000 0.011 雄鱼 12 vs. 6 3.886 0.011 0.530 0.004 全雌鱼 12 vs. 6 4.598 0.009 0.820 0.009 3. 讨论
3.1 全雌养殖大黄鱼生长性能分析
基于雄性和雌性之间存在明显的生长速率差异, 单性养殖成为某些鱼类优选的养殖模式[6]; 如, 孔雀鱼[6]、罗非鱼[9]等, 其单性养殖依然保持较快的生长速度。此外, 雌雄鱼分开养殖可有效避免鱼类将能量用于繁殖和竞争, 而对生长产生负面影响[9]。在本研究中, 养殖120d后, AF体重显著高于CM, 而与CF无显著差异; 而CF和CM体重间无显著差异, 全雌养殖大黄鱼保持了较快的生长速度。由此可以推测, 随着养殖时间的延长, 雌雄间将进一步表现出生长差距, 全雌养殖组会表现出更为明显的生长优势。
3.2 连续降温诱导大黄鱼鳃和肠道组织损伤
鳃是鱼类的主要呼吸器官, 同时也具有代谢废物、调节渗透压等功能[18], 而鳃组织对温度变化较为敏感。例如, 军曹鱼(Rachycentron canadum)[19]、黑鲷(Acanthopagrus schlegelii)[18]、四指马鲅(Eleutheronema tetradactylum)[20]等在低温暴露情况下其鳃组织均出现了细胞增生、上皮细胞糜烂及鳃丝变形等现象, 且随着暴露时间的增加和温度的降低鳃组织损伤情况加剧。本研究结果与其类似, 在低温胁迫条件下, CF、CM和AF的鳃组织均出现细胞空泡化、水肿以及鳃丝变形, 且随着温度的降低以及暴露时间的增加其损伤加剧。鳃组织的水肿和变形可能是由低温胁迫导致渗透压平衡的失调从而致使膜的渗透性增加而引起的[19]; 随着低温胁迫时间的延长, 水肿加剧且引起鳃丝收缩, 从而导致鳃丝弯曲[20]。
肠道黏膜是防御病害的一道屏障, 其结构的损伤不但影响肠道的防御功能, 而且影响肠道的免疫和吸收功能[21]; 黏液细胞分泌的黏液具有润滑肠壁、助消化及增加有益菌的定植的功能[22]。研究证实, 低温胁迫可引起肠道组织出现生理损伤, 如上皮细胞损伤、细胞增生、杯状细胞肿胀等[23]。本研究结果显示, 随着水温的连续降低, CF、CM和AF的肠道组织均出现肠细胞融合、杯状细胞肿胀、黏膜细胞坏死和脱落等现象, 破坏了肠道组织结构的完整性, 对肠道功能产生了一定的影响。
3.3 连续降温诱导大黄鱼鳃和肠道氧化应激及免疫反应
低温波动会导致鱼类体内大量活性氧(ROS)的积累, 从而引发氧化应激, 致使机体出现氧化损伤[19, 24, 25]。鱼类可通过提高其鳃和肠道中抗氧化酶活性来降低低温应激给机体带来的损伤。例如, 在低温胁迫军曹鱼和黄姑鱼(Nibea albiflora)的研究中发现, 鳃组织中抗氧化酶(SOD、CAT)活性先显著升高后显著降低[19, 26]。在低温胁迫暗纹东方鲀(Takifugu fasciatus)和大黄鱼的研究中发现, 其肠道中SOD、CAT、GSH-Px活性及MDA含量均显著升高[16, 23]。本研究结果与以上研究结果相似; 无论对照组还是全雌养殖大黄鱼, 在连续降温胁迫后其鳃和肠道中SOD、CAT、GSH-Px活性及MDA含量均呈先显著升高后显著下降。这可能是因为温度降至6℃时鳃和肠道受到严重氧化应激损伤所致[27, 28]。
热休克蛋白常被作为鱼体是否受到应激的反应指标之一[26]。研究表明, 黑鲷和黄姑鱼低温暴露后其肝脏中热休克蛋白含量均显著增加[26, 29]; 大黄鱼在8℃处理3d后肝脏中HSP70和HSP90基因的表达量均显著增加[16]。在本研究中, 在连续低温胁迫条件下, CF、CM和AF的鳃和肠道中HSP70和HSP90含量均显著升高; 但温度恢复后, 其HSP70和HSP90基因的表达量均未恢复到正常水平, 这可能是因为鱼体对外界环境进行自主适应的生理表现。
低温暴露会触发Toll样受体(TLRs)的激活, 如TLR4和TLR5, 随后启动NF-κB信号通路, 导致促炎细胞因子相关基因过度表达, 从而引起组织炎症反应[30, 31]。例如, 在低温胁迫下大西洋鲑皮肤中TNF-α基因表达量显著增加[32]; 在低温胁迫下雌雄大黄鱼肠道中IL-6基因表达量均显著增加[1]。在本研究中, 在连续低温胁迫条件下, CF、CM和AF的鳃和肠道中IL-6和TNF-α基因表达量均显著增加; 而在6℃时, CF和CM的鳃和肠道中IL-6基因的表达量均显著高于AF。此外, 在6℃时, CF鳃中IL-6和TNF-α基因表达量均显著高于CM; 而在CF和AF的肠道中TNF-α基因表达量显著低于CM, CF与CM间IL-6基因表达量无显著差异。综上可知, CF和AF比CM有更高的低温耐受能力, 这可能与雌雄鱼低温胁迫相关应激途径差异有关[31, 33], 具体原因还需进一步的研究。
3.4 低温胁迫对大黄鱼肠道菌群的影响
肠道菌群作为宿主的体外“器官”, 其在宿主体内的动态平衡对宿主的健康至关重要[34, 35]。温度是影响肠道微生物群组成和功能的重要环境因素, 冷刺激可显著影响肠道菌群的组成[36], 可能导致“寒冷微生物群”的形成[37]。在本研究中, 低温胁迫后CF和AF肠道菌群组成显著变化, 而CM没有; 这表明CF和AF肠道菌群组成更易受到低温影响; 此外, 低温胁迫后CF和AF肠道菌群中别弧菌属相对丰度显著增加, CM肠道菌群中别弧菌属相对丰度一直保持较高的丰度; 这一结果与我们之前对大黄鱼网箱越冬的研究相一致[1], 由此表明, 低温时应该加强对大黄鱼肠道菌群中弧菌属细菌的防治。
肠道菌群生态网络分析有助于进一步解析水产动物低温胁迫下其肠道菌群的稳定性。网络中两个节点之间的连接表示物种间的相互作用[38]。红色连接表示竞争关系, 而蓝色连接表示互利或共生关系[39]。在本研究中, 在低温胁迫条件下, CF、CM和AF肠道菌群生态网络结构均发生显著改变; 在低温胁迫后, CF肠道菌群物种间连线数量减少50.67%, 而且主要是代表物种间互利或共生关系的连线数量急剧减少; 这表明CF肠道菌群网络系统稳定性明显降低。在低温胁迫下, CM肠道菌群网络发生重组, 形成一个新的模块; 在生物系统中, 涌现特性是指一种整体特性, 无法由其单个组成部分决定, 而是由整个网络的结构和内部相互作用所产生的结果[40], 在微生物群落中, 这一特性促进了成员间的高效交流, 使其能够快速应对环境变化[39]; 因此, 在低温胁迫后, CM肠道菌群网络通过重组网络模块, 从而可能实现比原始子模块更多或新的功能以应对温度的变化。相较于CF和CM, 低温胁迫后AF肠道菌群网络系统仍有2个模块构成, 这表明低温虽然也显著影响其肠道菌群网络结构, 但其网络系统稳定性优于CF和CM。
4. 结论
在本研究中, 在相同的养殖条件下, 全雌大黄鱼的单性养殖保持了较高的生长速度。低温胁迫可导致对照组雌鱼、对照组雄鱼和全雌养殖大黄鱼的鳃和肠道组织均出现损伤和氧化应激, 影响机体炎症反应; 而在恢复后的12℃时, 对照组雌鱼和对照组雄鱼的鳃和肠道组织中过氧化氢酶活性和丙二醛含量仍显著高于全雌养殖大黄鱼; 同时, 对照组雌鱼和对照组雄鱼的鳃组织中相关炎症基因表达水平仍显著高于全雌养殖大黄鱼; 低温胁迫可改变对照组雌鱼和全雌养殖大黄鱼的肠道菌群优势组成, 而对对照组雄鱼肠道菌群优势组成无显著影响; 显著影响对照组雌鱼、对照组雄鱼和全雌养殖大黄鱼的肠道菌群网络结构, 但全雌大黄鱼的肠道菌群网络结构的稳定性优于对照组雌鱼和对照组雄鱼。
-
图 2 低温胁迫对大黄鱼鳃(A)和肠道(B)组织显微结构的影响(×200, 比例尺=50 μm)
SL. 鳃小片; PL. 鳃丝; 1. 鳃小片末端弯曲; 2. 上皮细胞水肿; 3. 细胞空泡化。C. 柱状细胞; G. 杯状细胞; SG. 杯状细胞肿胀; N. 黏膜层坏死
Figure 2. Effects of low temperature stress on the gill (A) and intestine (B) structure in L. crocea (×200, scale bar=50 μm)
SL. Secondary lamella; PL. Primary lamellae; 1. Curved tips and hyperemia at ending; 2. Epithelial oedema; 3. Cellular vacuolation; C. Columnar cell; G. Goblet cell; SG. Swelling of goblet cell; N. Necrosis in the mucosal layer
图 3 低温胁迫对大黄鱼鳃和肠道组织超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶活性及丙二醛含量的影响
图上不同小写字母表示相同温度下不同组间差异显著(P<0.05); 下同
Figure 3. Effects of low temperature stress on the activities of SOD, CAT, GSH-Px, and MDA content in gill and intestine of L. crocea
Different lowercase letters on the graph indicate significant differences in groups at the same temperature (P<0.05); The same applies below
图 5 低温胁迫对大黄鱼肠道菌群多样性和组成的影响
A.肠道菌群主坐标分析(PCoA); B.肠道菌群α-多样性分析; C.肠道菌群在门水平和属水平上的组成
Figure 5. Effect of low temperature stress on the diversity and composition of the intestinal microbiota in L. crocea
A. The principal co-ordinates analysis of the intestinal microbiota; B. the α-diversity of the intestinal microbiota; C. the composition of the intestinal microbiota at phylum- and genus-level
表 1 荧光定量引物
Table 1 RT-qPCR primers
引物
Primer引物序列
Primer sequence (5′—3′)来源
SourceIL-6-F TGAAGGCTCCGACGAAATG Cen et al.[1] IL-6-R GTCCAGTAGGCTAAACTGCTATC Cen et al.[1] TNF-α-F CGTCGTTCAGAGTCTCCTGC Tan et al.[17] TNF-α-R TGTACCACCCGTGTCCCACT Tan et al.[17] HSP70-F CGCAGTCATCACAGTTCCG Lv et al.[16] HSP70-R TGCCGTCTTCAATGGTCAG Lv et al.[16] HSP90-F CCGCTACGAAAGCCTGACTGA Lv et al.[16] HSP90-R ACGACCACCTTCTCGGCAAC Lv et al.[16] β-actin-F GACCTGACAGACTACCTCATG Tan et al.[17] β-actin-R AGTTGAAGGTGGTCTCGTGGA Tan et al.[17] 表 2 对照组和全雌养殖大黄鱼的生长指标
Table 2 The growth indexes of control group and all-female culture of L. crocea
组别
Group初体重
Initial body
Weight (g)末体重
Final body
Weight (g)增重率
Weight gain
rate (%)特定生长率
Specific growth
rate (%/d)肥满度
Condition factor
(g/cm3)饲料系数
Feed conversion
ratioCF 14.01±2.52 70.04±11.37ab 401.45±24.83ab 1.34±0.04 2.09±0.28a 1.47±0.14a CM 13.87±3.17 66.56±7.00b 390.45±49.50b 1.32±0.09 1.88±0.17b AF 14.09±2.72 74.16±6.39a 438.04±66.52a 1.40±0.23 2.11±0.17a 1.35±0.26b 注: 同列不同小写字母表示差异显著(P<0.05)Note: Different lowercase letters in the same column indicate significant differences (P<0.05) 表 3 低温胁迫下对照组雌鱼、对照组雄鱼和全雌鱼肠道菌群差异分析
Table 3 Differences in the intestinal microbiota among females, males, and all-females were analyzed under low-temperature stress
性别 温度/℃ Bray-Curtis distance PERMANOVA ANOSIM F P R P 雌鱼 12 vs. 6 1.550 0.010 0.060 0.004 雄鱼 12 vs. 6 1.051 0.268 0.436 0.226 全雌鱼 12 vs. 6 0.771 0.728 0.108 0.628 表 4 基于双因素方差分析比较不同性别和温度的α-多样性指数
Table 4 Comparison of α-diversity indexes in sex and temperature based on two-way ANOVA test
Two-way ANOVA test Chao1 Shannon F P F P 性别(雌, 雄, 全雌) 1.380 0.018* 3.912 0.001* 温度(12, 6) 1.184 0.148 1.523 0.170 性别×温度 1.081 0.253 0.809 0.594 注: *代表差异显著Note: * indicate significant differences 表 5 低温胁迫下对照组雌鱼、对照组雄鱼和全雌鱼肠道菌群网络结构差异分析
Table 5 The networked community differences among females, males, and all-females were analyzed under low-temperature stress
性别 温度/℃ Bray-Curtis distance PERMANOVA ANOSIM F P R P 雌鱼 12 vs. 6 11.134 0.014 1.000 0.011 雄鱼 12 vs. 6 3.886 0.011 0.530 0.004 全雌鱼 12 vs. 6 4.598 0.009 0.820 0.009 -
[1] Cen H X, Li H D, Chen R Y, et al. Exploring the sex dimorphism in the expression of intestinal barrier and immune-related genes and intestinal microbiota in cage-cultured large yellow croaker (Larimichthys crocea) during the overwintering period along the Zhoushan coast [J]. Frontiers in Marine Science, 2024(11): 1391035.
[2] Mu J L, Hu W H, Chen R Y, et al. Production of neomale and neofemale large yellow croaker (Larimichthys crocea) and establishment of all-female populations [J]. Aquaculture, 2024(590): 741010.
[3] Kunda M, Pandit D, Harun-Al-Rashid A. Optimization of stocking density for mono-sex nile tilapia (Oreochromis niloticus) production in riverine cage culture in Bangladesh [J]. Heliyon, 2021, 7(11): e08334. doi: 10.1016/j.heliyon.2021.e08334
[4] 潘书慧, 周彤, 袁嘉慧, 等. 金钱鱼下丘脑转录组分析及其对雌激素在体注射的响应 [J]. 水生生物学报, 2023, 47(8): 1195-1210.] doi: 10.7541/2023.2022.0286 Pan S H, Zhou T, Yuan J H, et al. Transcriptome analysis of hypothalamus in male and female spotted scat (Scatophagus argus) and differential gene expression in 17β-estradiol injected males [J]. Acta Hydrobiologica Sinica, 2023, 47(8): 1195-1210. [ doi: 10.7541/2023.2022.0286
[5] 孙宇轩, 张梦倩, 李璐, 等. 半滑舌鳎rimoc1基因在雌雄鱼中的差异表达 [J]. 渔业科学进展, 2024, 45(4): 34-42.] doi: 10.11758/yykxjz.20230307001 Sun Y X, Zhang M Q, Li L, et al. Differential expression of the rimoc1 gene in male and female chinese tongue sole (Cynoglossus semilaevis) [J]. Progress in Fishery Sciences, 2024, 45(4): 34-42. [ doi: 10.11758/yykxjz.20230307001
[6] Görelşahin S, Yanar M, Kumlu M. The effects of stocking density, Tubifex feeding and monosex culture on growth performance of guppy (Poecilia reticulata) in a closed indoor recirculation system [J]. Aquaculture, 2018(493): 153-157.
[7] 王凌宇, 齐飘飘, 陈敏, 等. 性类固醇激素对黄颡鱼雌雄生长二态性的影响 [J]. 水生生物学报, 2020, 44(2): 379-388.] Wang L Y, Qi P P, Chen M, et al. Effects of sex steroid hormones on sexual size dimorphism in yellow catfish (Tachysurus fulvidraco) [J]. Acta Hydrobiologica Sinica, 2020, 44(2): 379-388. [
[8] 张发扬, 李坤, 汪惟超, 等. 牙鲆amhr2基因的分子特征及组织表达 [J]. 水产科学, 2024, 43(4): 509-519.] Zhang F Y, Li K, Wang W C, et al. Molecular characteristics and expression analysis of amhr2 gene in bastard halibut Paralichthys olivaceus [J]. Fisheries Science, 2024, 43(4): 509-519. [
[9] Githukia C M, Ogello E O, Kembenya E M, et al. Comparative growth performance of male monosex and mixed sex nile tilapia (Oreochromis niloticus L.) reared in earthen ponds [J]. Croatian Journal of Fisheries, 2015, 73(1): 20-25. doi: 10.14798/73.1.788
[10] Lavrutich M, Markussen J, Rystad N. The value of mono-gender production in Atlantic salmon farming [J]. Aquaculture, 2024(578): 740089.
[11] 王彤, 陈生熬, 刘一萌, 等. 鱼类低温适应性机制与抗冻蛋白的研究进展 [J]. 海洋渔业, 2024, 46(4): 509-519.] doi: 10.3969/j.issn.1004-2490.2024.04.010 Wang T, Chen S A, Liu Y M, et al. Research progress on the mechanism of low temperature adaptation and antifreeze protein of fish [J]. Marine Fisheries, 2024, 46(4): 509-519. [ doi: 10.3969/j.issn.1004-2490.2024.04.010
[12] Donaldson M R, Cooke S J, Patterson D A, et al. Cold shock and fish [J]. Journal of Fish Biology, 2008, 73(7): 1491-1530. doi: 10.1111/j.1095-8649.2008.02061.x
[13] 王永红, 王武卿, 曾霖, 等. 升温驯化对温度胁迫下大黄鱼幼鱼能量代谢的影响 [J]. 海洋渔业, 2024, 46(5): 599-607.] doi: 10.3969/j.issn.1004-2490.2024.05.008 Wang Y H, Wang W Q, Zeng L, et al. Effects of heat acclimation on energy metabolism of juvenile Larimichthys crocea under temperature stress [J]. Marine Fisheries, 2024, 46(5): 599-607. [ doi: 10.3969/j.issn.1004-2490.2024.05.008
[14] 张东玲, 徐浩, 张震西, 等. 大黄鱼cGPDH和mGPDH基因克隆及低温胁迫下的表达差异分析 [J]. 中国水产科学, 2021, 28(3): 253-264.] Zhang D L, Xu H, Zhang Z X, et al. Molecular cloning of cGPDH and mGPDH and their expression analysis under low-temperature stress in Larimichthys crocea [J]. Journal of Fishery Sciences of China, 2021, 28(3): 253-264. [
[15] Suo N, Wu Y D, Zhou Z X, et al. Genome-wide association and expression analysis revealed the candidate variants and molecular underpinnings of cold-stress response in large yellow croaker [J]. Marine Biotechnology, 2022, 24(5): 927-941. doi: 10.1007/s10126-022-10155-7
[16] Lv H R, Liu Y L, Li H D, et al. Modulation of antioxidant enzymes, heat shock protein, and intestinal microbiota of large yellow croaker (Larimichthys crocea) under acute cold stress [J]. Frontiers in Marine Science, 2021(8): 725889.
[17] Tan P, Dong X J, Mai K S, et al. Vegetable oil induced inflammatory response by altering TLR-NF-κB signalling, macrophages infiltration and polarization in adipose tissue of large yellow croaker (Larimichthys crocea) [J]. Fish & Shellfish Immunology, 2016(59): 398-405.
[18] 卫明亮, 张志伟, 张志勇, 等. 冷应激对黑鲷组织损伤及细胞凋亡基因表达的影响 [J]. 南方水产科学, 2022, 18(5): 110-117.] doi: 10.12131/20210372 Wei M L, Zhang Z W, Zhang Z Y, et al. Effects of cold stress on black porgy tissue injury and apoptosis gene expression [J]. South China Fisheries Science, 2022, 18(5): 110-117. [ doi: 10.12131/20210372
[19] 李豫, 黄建盛, 陈有铭, 等. 低温胁迫对军曹鱼幼鱼鳃组织抗氧化能力、细胞凋亡和组织结构的影响 [J]. 南方水产科学, 2023, 19(3): 68-77.] doi: 10.12131/20220227 Li Y, Huang J S, Chen Y M, et al. Effect of low temperature stress on antioxidant stress, apoptosis and histological structure of gills in cobia (Rachycentron canadum) [J]. South China Fisheries Science, 2023, 19(3): 68-77. [ doi: 10.12131/20220227
[20] 区又君, 刘奇奇, 温久福, 等. 急性低温胁迫对四指马鲅幼鱼肝脏、肌肉以及鳃组织结构的影响 [J]. 生态科学, 2018, 37(5): 53-59.] Ou Y J, Liu Q Q, Wen J F, et al. The effects of acute low temperature stress on liver, muscle and gill tissues of juvenile Eleutheronema tetradactylum [J]. Ecological Science, 2018, 37(5): 53-59. [
[21] 邢潇, 宋如昕, 王兰, 等. 急性冷胁迫对中华鳖幼鳖肠道黏膜组织的影响 [J]. 水生生物学报, 2019, 43(1): 102-108.] Xing X, Song R X, Wang L, et al. The different response of the intestinal mucosal histological features in different sections of juvenile chinese soft-shelled turtle under acute cold stress [J]. Acta Hydrobiologica Sinica, 2019, 43(1): 102-108. [
[22] 李海东, 白雪峰, 孙虎山, 等. 两种海马鳃组织和消化道的黏液细胞类型及分布 [J]. 动物学杂志, 2014, 49(4): 552-559.] Li H D, Bai X F, Sun H S, et al. Types and distribution of mucous cells in the gill tissue and digestive system of Hippocampus trimaculatus and H. japonicus [J]. Chinese Journal of Zoology, 2014, 49(4): 552-559. [
[23] 付东勇, 张艺然, 褚鹏, 等. 低温胁迫对暗纹东方鲀肠道氧化应激、细胞凋亡及肠道微生物组成的影响 [J]. 水产学报, 2024, 48(1): 42-53.] Fu D Y, Zhang Y R, Chu P, et al. Effects of low temperature stress on the oxidative stress, apoptosis and intestinal microbial composition in intestine of Takifugu fasciatus [J]. Journal of Fisheries of China, 2024, 48(1): 42-53. [
[24] Lushchak V I, Bagnyukova T V. Temperature increase results in oxidative stress in goldfish tissues. 1. Indices of oxidative stress [J]. Comparative Biochemistry and Physiology Part C: Toxicology & Pharmacology, 2006, 143(1): 30-35.
[25] Xu Z H, Regenstein J M, Xie D D, et al. The oxidative stress and antioxidant responses of Litopenaeus vannamei to low temperature and air exposure [J]. Fish & Shellfish Immunology, 2018(72): 564-571.
[26] 罗胜玉, 徐冬冬, 楼宝, 等. 低温胁迫对黄姑鱼(Nibea albiflora)抗氧化酶、Na+/-K+-ATP酶及Hsp70蛋白含量的影响 [J]. 海洋通报, 2017, 36(2): 189-194.] Luo S Y, Xu D D, Lou B, et al. Effects of low temperature stress on activities of antioxidant enzymes, Na+/-K+-ATP enzyme and Hsp70 content of Nibea albiflora [J]. Marine Science Bulletin, 2017, 36(2): 189-194. [
[27] 郭美洁, 梅俊, 谢晶. 温度和振动联合胁迫对花鲈有水保活运输中组织损伤及生化指标的影响 [J]. 水产学报, 2024, 48(7): 69-81.] Guo M J, Mei J, Xie J. Effects of temperature and vibration stress on tissue damage and biochemical indices in sea bass (Lateolabrax japonicus) during the process of keeping-alive [J]. Journal of Fisheries of China, 2024, 48(7): 69-81. [
[28] Luo S W, Cai L, Liu Y, et al. Functional analysis of a dietary recombinant Fatty acid binding protein 10 (FABP10) on the Epinephelus coioides in response to acute low temperature challenge [J]. Fish & Shellfish Immunology, 2014, 36(2): 475-484.
[29] 陈自强, 张志勇, 祝斐, 等. 急性低温对黑鲷抗氧化酶活性和热休克蛋白含量的影响 [J]. 动物学杂志, 2020, 55(6): 784-792.] Chen Z Q, Zhang Z Y, Zhu F, et al. The effects of acute low temperature stress on activities of antioxidant enzymes and heat shock protein content in Acanthopagrus schlegelii [J]. Chinese Journal of Zoology, 2020, 55(6): 784-792. [
[30] Chen H, Liang Y, Han Y W, et al. Genome-wide analysis of Toll-like receptors in zebrafish and the effect of rearing temperature on the receptors in response to stimulated pathogen infection [J]. Journal of Fish Diseases, 2021, 44(3): 337-349. doi: 10.1111/jfd.13287
[31] 崔宗斌, 任静, 龙勇. 鱼类低温应激和损伤的信号通路与调控机制 [J]. 河南师范大学学报(自然科学版), 2023, 51(3): 11-21.] Cui Z B, Ren J, Long Y. Signal pathways and regulatory mechanisms of cold stress response and injury in fish [J]. Journal of Henan Normal University (Natural Science Edition), 2023, 51(3): 11-21. [
[32] Jensen L B, Boltana S, Obach A, et al. Investigating the underlying mechanisms of temperature-related skin diseases in Atlantic salmon, Salmo salar L. , as measured by quantitative histology, skin transcriptomics and composition [J]. Journal of Fish Diseases, 2015, 38(11): 977-992.
[33] Hayward S A L, Manso B, Cossins A R. Molecular basis of chill resistance adaptations in poikilothermic animals [J]. The Journal of Experimental Biology, 2014, 217(1): 6-15. doi: 10.1242/jeb.096537
[34] Shortt C, Hasselwander O, Meynier A, et al. Systematic review of the effects of the intestinal microbiota on selected nutrients and non-nutrients [J]. European Journal of Nutrition, 2018, 57(1): 25-49. doi: 10.1007/s00394-017-1546-4
[35] Mackos A R, Varaljay V A, Maltz R, et al. Role of the intestinal microbiota in host responses to stressor exposure [J]. International Review of Neurobiology, 2016(131): 1-19.
[36] Zhou E, Zhang L, He L, et al. Cold exposure, gut microbiota and health implications: a narrative review [J]. The Science of the Total Environment, 2024(916): 170060.
[37] Chevalier C, Stojanović O, Colin D J, et al. Gut microbiota orchestrates energy homeostasis during cold [J]. Cell, 2015, 163(6): 1360-1374. doi: 10.1016/j.cell.2015.11.004
[38] Deng Y, Jiang Y H, Yang Y F, et al. Molecular ecological network analyses [J]. BMC Bioinformatics, 2012(13): 113.
[39] Deng Y, Zhang P, Qin Y J, et al. Network succession reveals the importance of competition in response to emulsified vegetable oil amendment for uranium bioremediation [J]. Environmental Microbiology, 2016, 18(1): 205-218. doi: 10.1111/1462-2920.12981
[40] Bhalla U S, Iyengar R. Emergent properties of networks of biological signaling pathways [J]. Science, 1999, 283(5400): 381-387. doi: 10.1126/science.283.5400.381



 下载:
下载: