EMISSION CHARACTERISTIC AND INFLUENCING FACTOR OF CO2, CH4, AND N2O FROM WATER-AIR INTERFACE OF LARGEMOUTH BASS CULTURE POND
-
摘要:
为探究大口黑鲈(Micropterus salmoides)养殖系统温室气体的排放特征和规律, 于2023年7—10月采用静态箱−气相色谱法对大口黑鲈养殖塘水−气界面CO2、CH4、N2O排放通量进行了测定, 并结合水体表层环境因子和氮磷营养变化分析了其主要影响因素。结果表明: 监测期间大口黑鲈养殖塘水−气界面CO2、CH4、N2O的排放通量均值分别为(241.4±14.5)、(1.38±0.31)和(0.24±0.04) mg/(m2·h), 养殖塘整体上表现为温室气体排放源。皮尔森分析结果表明CO2排放通量与水温(WT)、温度(T)、叶绿素a (Chl.a)、压强(P)和pH呈显著正相关, 与氨氮(${\rm{NH}}^+_4 $-N)呈显著负相关; N2O排放通量与总氮(TN)、亚硝态氮(${\rm{NO}}^-_2 $-N)、硝态氮(${\rm{NO}}^-_3 $-N)和溶解氧(DO)呈显著正相关, 与WT呈显著负相关; CH4排放通量与环境因子无显著相关关系。冗余分析表明WT是影响水−气界面CO2、CH4、N2O排放的关键环境因子。在90d的重要养殖期内, 大口黑鲈养殖塘百年全球增温潜势为7.74×103 kg/hm2, 暗示大口黑鲈池塘养殖或有促进温室效应的潜力。
Abstract:Largemouth bass (Micropterus salmoides) has become one of the important species cultured in ponds across China, yet there are few studies on greenhouse gas fluxes at the water-gas interface in largemouth bass culture ponds. In this study, we investigated the characteristics and patterns of greenhouse gas emissions in largemouth bass culture ponds located in Daye City, Hubei Province. The CO2, CH4, and N2O emission fluxes at the water-air interface were measured by static box-gas chromatography from July to October 2023. Additionally, we analyzed the main influencing factors by examining changes in surface environmental factors and nutrients levels. The results showed that the mean emission fluxes of CO2, CH4, and N2O at the water-air interface of the largemouth bass culture ponds were (241.0±14.5), (1.38±0.31), and (0.24±0.04) mg/m2·h during the monitoring period, respectively, indicating that the largemouth bass culture ponds are a net source of greenhouse gas emission. Pearson correlation analysis showed that CO2 emission fluxes were positively correlated with WT, T, Chl.a, P, and pH, and negatively correlated with ${\rm{NH}}^+_4 $-N. N2O emission flux was positively correlated with TN, ${\rm{NO}}^-_2 $-N, ${\rm{NO}}^-_3 $-N, and DO, and negatively correlated with WT. No significant correlation was found between CH4 emission flux and environmental factors. Redundancy analysis indicated that WT is the key environmental factor affecting the emission of CO2, CH4, and N2O at the water-air interface. During the 90-day growth cycle, the 100-year global warming potential of largemouth bass aquaculture pond was 7.74×103 kg/hm2, suggesting that pond culture of largemouth bass may have the potential to promote the greenhouse effect.
-
Keywords:
- Greenhouse gases /
- Emission flux /
- Global warming potential /
- Largemouth bass /
- Pond aquaculture
-
由温室气体浓度升高导致的全球气候变暖问题是当今世界的主要挑战之一[1]。CO2、CH4、N2O是大气中主要的温室气体(GHGs), 分别占全球气候变暖权重的60%、25%和5%[2]。2023年大气中CO2和CH4浓度分别为420和1.90 μg/L, 比工业化前水平高出约48%和156%[3]。据估算, 全球内陆水体释放2.10 Pg·C/y的CO2[4]、0.65 Pg·C/y的CH4[5]及0.37 Pg·C/y的N2O。现如今如何量化不同生态系统CO2、CH4、N2O来源和估算其排放强度已成为全球温室气体减排的关键问题之一[6]。
水生生态系统是温室气体的重要来源。目前有关水生生态系统温室气体排放的研究大多集中在湖泊[4]、水库[7]、河流[4]等天然水域, 而对水产养殖池塘的研究相对缺乏[8]。水产养殖塘是全球水生生态系统的重要组成部分, 小规模的水产养殖塘在不同地点广泛存在。据估算, 全球约有1.11×105 km2小型池塘[6], 是全球温室气体排放不可忽视的来源之一。与天然水体相比, 水产养殖池塘具有更高的养殖密度、有机物密度[1]、水域浅和混合频繁等特点[9], 这些条件往往导致更高的温室气体产生和排放速率。中国内陆淡水养殖系统每年共排放181.7 Tg CO2-eq (CO2和CH4), 其中池塘养殖系统(74.6 Tg CO2-eq/y)和稻渔综合种养系统(69.4 Tg CO2-eq/y)的排放量占总排放量的79.3%[10]。目前已有一些水产养殖塘CO2、CH4和N2O排放通量的报告[11, 12], 但由于测量的地理分布有限及数据可用性不足[13], 这些水产养殖塘温室气体排放存在较大差异[14]。
中国是世界上最大的水产养殖国, 多年来水产养殖产量占全球水产养殖总产量的60%以上[15]; 其中, 池塘养殖是最主要的养殖模式, 2022年全国淡水池塘养殖面积达2.63×104 km2 [16]。研究表明投进养殖池塘中的饲料不到30%被养殖物种摄食利用, 大部分以固体形式沉积于池塘底部[17], 造成了水体富营养化等环境问题。同时养殖塘具有较高的温室气体排放潜力, 随着中国水产养殖塘规模的逐年扩大, 水产养殖塘池温室气体减排问题日益迫切。水产养殖池塘的温室气体通量和排放特征在不同养殖区域和养殖品种之间存在较大差异[18]。黄河三角洲养虾塘整体上表现为CO2汇和CH4、N2O排放源, 且三者排放均呈现明显的季节差异[11]; 而闽江口鱼虾混合养殖塘CO2、CH4和N2O排放通量平均值分别为21.0、3.15和0.02 mg/(m2·h), 三者均表现为温室气体排放源[12]。近年来, 大口黑鲈(Micropterus salmoides)因具有无肌尖刺、肉质鲜美, 营养和经济价值高等优点成为我国水产养殖的重要品种之一。2022年我国大口黑鲈养殖产量达到8.03×108 kg[16], 主要为池塘养殖(超2万hm2)和工厂化养殖两种方式。目前大口黑鲈的研究主要集中在养殖技术、苗种培育、营养饲料等方面[19, 20], 关于大口黑鲈养殖池塘水−气界面温室气体通量研究鲜有报道。
湖北省是大口黑鲈主要养殖省份之一, 且研究发现湖北省养殖塘拥有最高的全球增温潜势[21]。因此本研究在湖北省大冶市保安湖附近养殖基地选择了三个大口黑鲈养殖塘, 于2023年7—10月监测了养殖塘CO2、CH4、N2O等3种温室气体的排放通量及变化特征, 分析了温室气体排放通量与环境因子的关系, 评估了大口黑鲈池塘养殖系统对温室效应的贡献。研究结果有利于了解池塘养殖系统的温室气体排放特征和规律, 可为池塘养殖系统温室气体减排方案制定提供理论基础。
1. 材料与方法
1.1 实验区域
本实验在湖北省黄石市大冶市保安湖附近养殖基地进行。该区域地处暖风带, 气候温暖潮湿, 雨量充沛, 日平均气温为17℃, 平均降水量为1.42×103 mm, 年光照时间约为2.13×103h, 无霜期261d。在此养殖基地选择3口大口黑鲈养殖塘, 每个塘口面积约为0.012 km2。鱼塘养殖用水均来自附近保安湖, 养殖期间水深控制在1.8—2.0 m。3个塘口均在4月上旬投放大口黑鲈鱼苗(投放鱼苗约30—40 g/尾, 3000 尾/667m2), 10月下旬开始起捕。养殖期间, 每天6:00—7:00和17:00—18:00定时投喂人工配合饲料(粗蛋白48%、粗脂肪≥6.5%、粗纤维≤5.0%、粗灰分18%、总磷1.0%、赖氨酸2.85%、水分12.0%), 具体投喂量视大口黑鲈生长阶段和摄食情况而定。每个鱼塘安装2台增氧机, 保证养殖期间大口黑鲈所需的溶解氧, 溶解氧为3.32—8.96 mg/L。
1.2 样品采集与分析
气体样品采集 本实验于2023年7月29日开始采用静态箱−气相色谱法采集大口黑鲈养殖塘CO2、CH4、N2O气体。在每个养殖塘沿对角线均匀布设3个气体采样点, 每15天采集1次, 共采样7次。采样前箱体于通风处倒置, 使箱内气体混合均匀, 然后将底座凹槽注满水, 在箱子扣入时达到水封的目的, 确保采集过程中不会出现漏气、跑气的现象。箱体密封后0、5min、10min、15min、20min进行气体收集, 采集量为50 mL左右, 气样储存于250 mL铝箔气样袋中, 立即带回实验室, 48h内完成气体检测。使用配备火焰电离检测器(FID)和电子捕获检测器的(ECD)的气相色谱仪Agilent 7890A分析CO2、CH4和N2O气体浓度。在采气过程中第15min读取采样箱和水体中的温度计读数作为采样时的箱温和水温。
气候与水质采集分析 在采集气体样品的同时监测气温(T)、风速(U)和气压(P), 测量高度距离水面1.5m。使用多参数水质检测仪(YSI 6600)监测水温(WT)、溶解氧(DO)、pH和电导率(Cond)。气体样品采集完成后, 在悬浮箱采样点附近使用有机玻璃采水器采集水体表层(水面以下10 cm深)水样装进1 L聚乙烯瓶中, 用4℃冰箱保存并立即运回实验室。水样在24h内完成测定, 水质指标监测参照《水和废水监测分析方法》(第4版)[22]。总氮(TN)采用碱性过硫酸钾消解-紫外分光光度法(HJ 636-2012)、氨氮(${\rm{NH}}^+_4 $-N)采用纳氏试剂光度法(HJ 535-2009)、硝态氮(${\rm{NO}}^-_3 $-N)采用酚二磺酸光度法(GB 7480-87)、亚硝态氮(${\rm{NO}}^-_2 $-N)采用N-(1-萘基)-乙二胺光度法(HJ 634-2016)、总磷(TP)采用钼酸铵分光光度法(GB/T 11893-1989)、磷酸盐(${\rm{PO}}^{3-}_4 $-P)采用磷钼蓝比色法 (GB/T 514-2008)和叶绿素a (Chl.a)采用紫外分光光度法(HJ 897-2017)测定。
气体通量计算 水−气界面CO2、CH4、N2O气体排放通量采用以下计算公式[12]:
$$ F=\rho \times \frac{V}{A}\times \frac{P}{{P}_{0}}\times \frac{{T}_{0}}{T}\times \frac{dc}{dt} $$ 式中, F为气体通量(mg/m2·h); $ \rho $为标准状态下温室气体密度; V为箱内空气体积, 即静态箱体积(m3); A为采样箱覆盖面积(m2); P为采样点处的气压(hPa); $ {T}_{0} $和$ {P}_{0} $分别为标准状态下的空气绝对温度(273.2 K)和气压(1.01×103 hPa); T为采样箱的绝对温度; $ \dfrac{dc}{dt} $为采样箱内CO2、CH4、N2O气体的浓度变化率。所测的数值只有当线性回归方程R2>0.8, 才为有效数据。
温室气体累积排放通量计算公式如下[23]:
$$ M=\sum _{i=1}^{a}\left[\frac{\left({F}_{i+1}+{F}_{i}\right)}{2}\times \left({t}_{i+1}-{t}_{i}\right)\times {10}^{-2}\times 24\right] $$ 式中, M为气体累积排放量(kg/hm2); F为气体通量(mg/m2·h); ti+1–ti为相邻两次采样间隔天数(d); 10–2为单位转化系数; 24为时间转化系数。
全球增温潜势(Global warming potential, GWP)一般用CO2当量(CO2-eq)表示, CH4和N2O其增温潜势在百年尺度上约为CO2的34倍和298倍[24]。
$$ {\mathrm{GWP}}={[{\mathrm{CO}}}_{2}]+34\times {[{\mathrm{CH}}}_{4}]+298\times {[{\mathrm{N}}}_{2}{\mathrm{O}}] $$ 1.3 数据分析
使用R 4.3.2软件“car”包中的Shapiro.test和 Levene.test检验数据正态性和方差齐性。对于满足正态性和方差齐性的数据 (T、U、Chl.a)使用单因素方差分析(One- way ANOVA)并使用Turkey-test进行事后多重比较; 对于不符合正态性和方差齐性的指标(P、WT、Cond、pH、DO、TN、${\rm{NH}}^+_4 $-N、${\rm{NO}}^-_2 $-N、${\rm{NO}}^-_3 $-N、TP、${\rm{PO}}^{3-}_4 $-P、CO2、CH4、N2O)使用Kruskal Wallis检验并使用“FSA”包进行Dunn test多重比较。使用“Meta”包分析环境因子与温室气体排放通量之间的关系; 使用冗余分析(RDA)环境因素对温室气体排放通量的影响程度, 该过程在“Vegan”包中实现, 并使用“rdacca.hp”包计算RDA分析中环境变量的单独解释率。以上统计分析中, 数据均为平均值±标准误(mean±SE), P<0.05视为有显著性差异。
2. 结果
2.1 环境因子变化特征
气候因子 在调查监测期间养殖塘区域的气温变动于20.3—37.6℃, 均值为(29.9±0.9)℃, 总体呈波动下降趋势。风速U的变化范围为0.88—2.82 m/s, 均值为(1.58±0.12) m/s, 10月26日风速最大。气压999.4—1024.7 hPa, 均值为(1010.2±1.1) hPa, 总体呈现为上升趋势。气温、风速和气压在不同监测时间点均存在显著差异(P<0.05; 表 1)。
表 1 不同监测时间点大口黑鲈养殖塘的气候因子变化特征Table 1. Characteristics of climatic factors in ponds of Micropterus salmoides culture at different monitoring times指标Parameter 采样日期Sampling date 7—29 8—12 8—27 9—11 9—27 10—11 10—26 温度T (℃) 31.7±0.8ab 36.8±1.3a 28.0±1.4abc 37.6±1.3a 25.6±0.9bc 25.9±1.7bc 20.3±1.1c 风速U (m/s) 1.41±0.18 ab 1.78±0.31 ab 2.04±0.32 ab 1.57±0.28 ab 0.88±0.15b 1.00±0.20b 2.82±0.30a 压强P (hPa) 999.4±0.1d 1001.6±0.2cd 1009.1.±0.2abc 1006.6±0.4bcd 1005.9±0.2ab 1014.3±3.1ab 1024.7±0.4a 注: 同一行中平均值上标有不同字母表示差异显著(P<0.05); 下同Note: Means with different superscript letters are significantly different from each other in the same row (P<0.05); The same applies below 水体理化因子 在调查监测期间水温变动于19.4—33.6℃, 均值为(27.3±0.6)℃, 总体呈现下降趋势。溶解氧变动于4.02—5.96 mg/L, 均值为(5.42±0.16) mg/L。电导率整体较高, 变动于455.6—677.6 μS/cm, 均值为(565.0±13.3) μS/cm。养殖水体呈碱性条件, pH变化范围介于8.24—9.05, 均值为8.53±0.05, 整体呈先降低后升高再降低的变化趋势(表 2)。水温、溶解氧、电导率和pH在不同监测时间点均有显著性差异(P<0.05)。
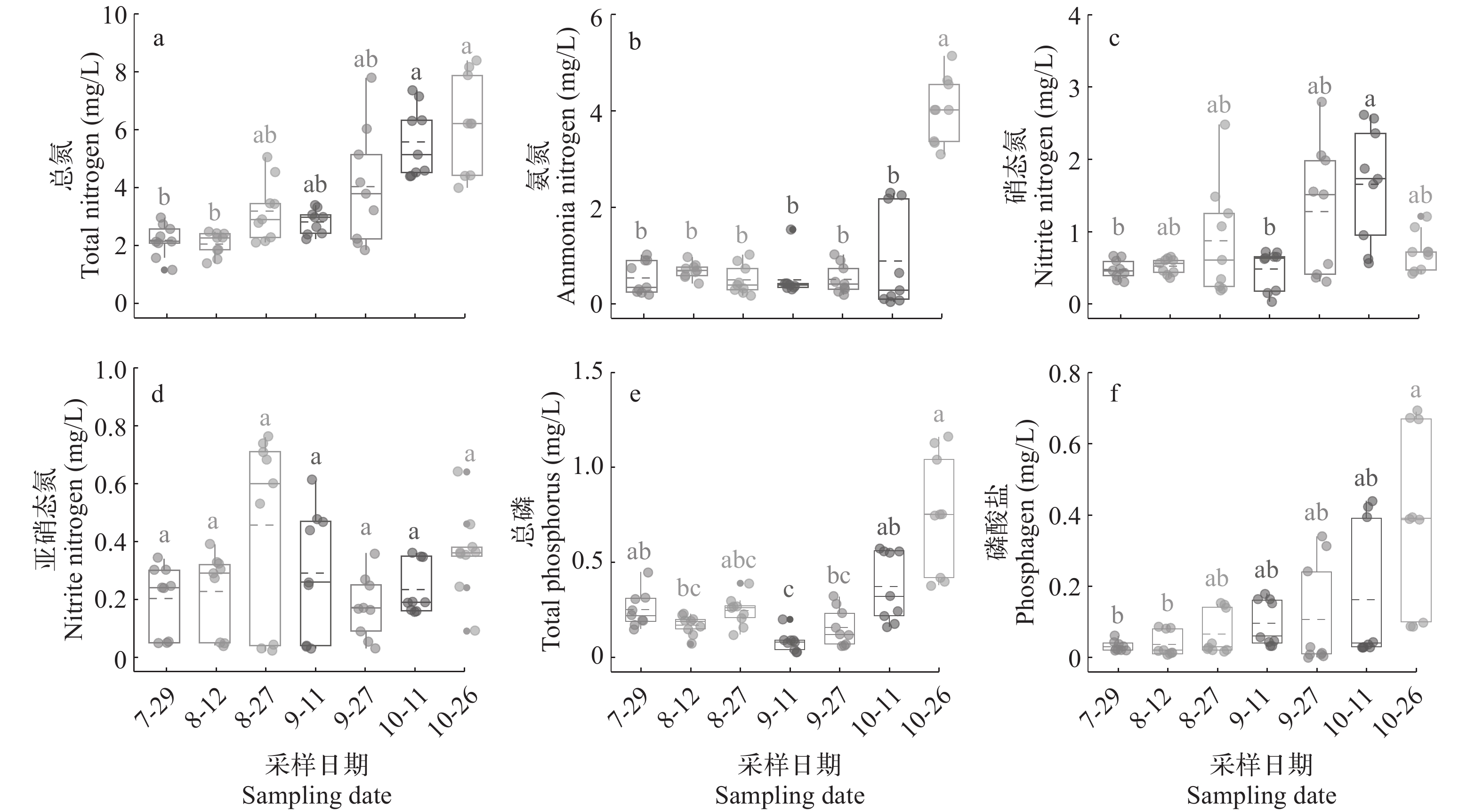
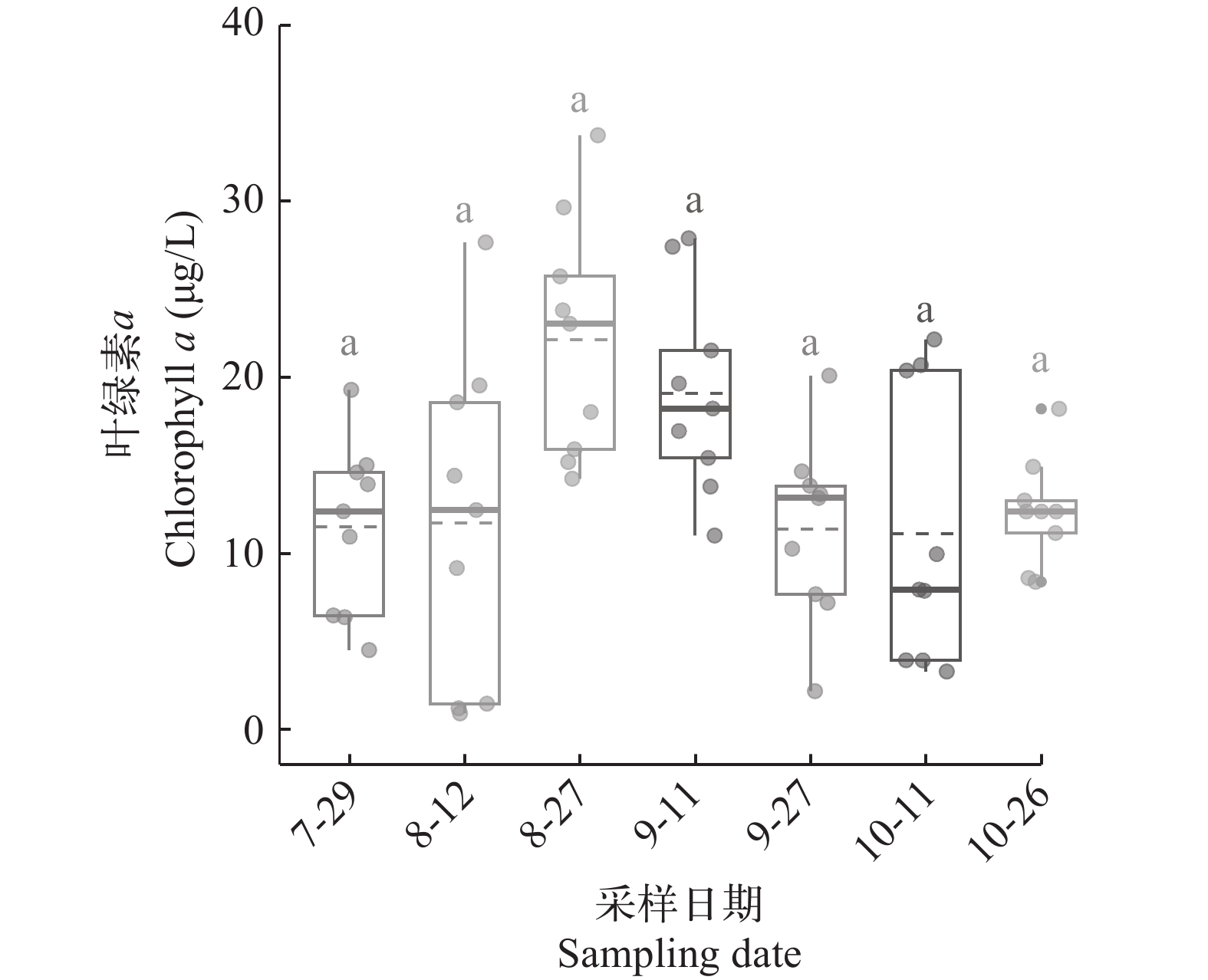
表 2 不同监测时间点大口黑鲈养殖塘的水质理化因子变化特征Table 2. Characteristics of water quality physicochemical factors in ponds of Micropterus salmoides culture at different monitoring times指标Parameter 采样日期Sampling date 7—29 8—12 8—27 9—11 9—27 10—11 10—26 水温WT (℃) 31.3±0.1ab 33.6±0.1a 26.9±0.1bc 31.1±0.2ab 25.3±0.1bcd 22.6±0.2cd 19.4±0.1d 溶解氧DO (mg/L) 4.75±0.36ab 5.79±0.30a 5.94±0.46a 5.89±0.44a 4.02±0.19b 5.58±0.43ab 5.96±0.38a 电导率Cond (μS/cm) 577.2±16.1ab 677.6±27.9a 571.7±20.2abc 482.7±60.6bc 599.2±14.0ab 590.9±11.2ab 455.6±4.4c pH 8.36±0.05ab 8.38±0.06 ab 8.24±0.03b 8.65±0.06a 9.05±0.19a 8.59±0.07a 8.46±0.08ab 氮、磷和叶绿素a含量 养殖塘中的氮磷含量在监测周期内呈波动上升趋势(图 1)。TN、${\rm{NH}}^+_4 $-N、${\rm{NO}}^-_3 $-N、TP和${\rm{PO}}^{3-}_4 $-P含量在不同监测时间点呈现显著性差异(P<0.05)。TN含量变动于2.05—6.21 mg/L, 整体呈现持续上升趋势, 10—11和10—26的TN含量显著高于7—29和8—12 (P<0.05)。${\rm{NH}}^+_4 $-N含量变动于0.50—4.02 mg/L, 最大值出现在10—26, 且显著高于其他监测时间点(P<0.05)。${\rm{NO}}^-_3 $-N含量变动于0.48—1.66 mg/L, 在10—11的${\rm{NO}}^-_3 $-N含量显著高于7—29和9—11 (P<0.05); ${\rm{NO}}^-_2 $-N含量变动于0.17—0.46 mg/L, 不同监测时间点之间均无显著差异(P>0.05); ${\rm{NO}}^-_3 $-N和${\rm{NO}}^-_2 $-N变化趋势基本一致均呈现“先增加-后下降-再增加”的趋势。TP含量变动于0.08—0.75 mg/L, 总体呈上升趋势, 10—26的TP含量显著高于8—12、9—11和9—27 (P<0.05)。${\rm{PO}}^{3-}_4 $-P含量变动于0.03—0.39 mg/L, 总体呈显著上升趋势, 10—26的${\rm{PO}}^{3-}_4 $-P含量显著高于7—29和8—12 (P<0.05; 图 1)。Chl.a变化范围是11.1—22.1 μg/L, 均值是(14.3±1.0) μg/L, 不同监测时间点之间均无显著差异(P>0.05; 图 2)。
2.2 水−气界面CO2、CH4、N2O排放特征
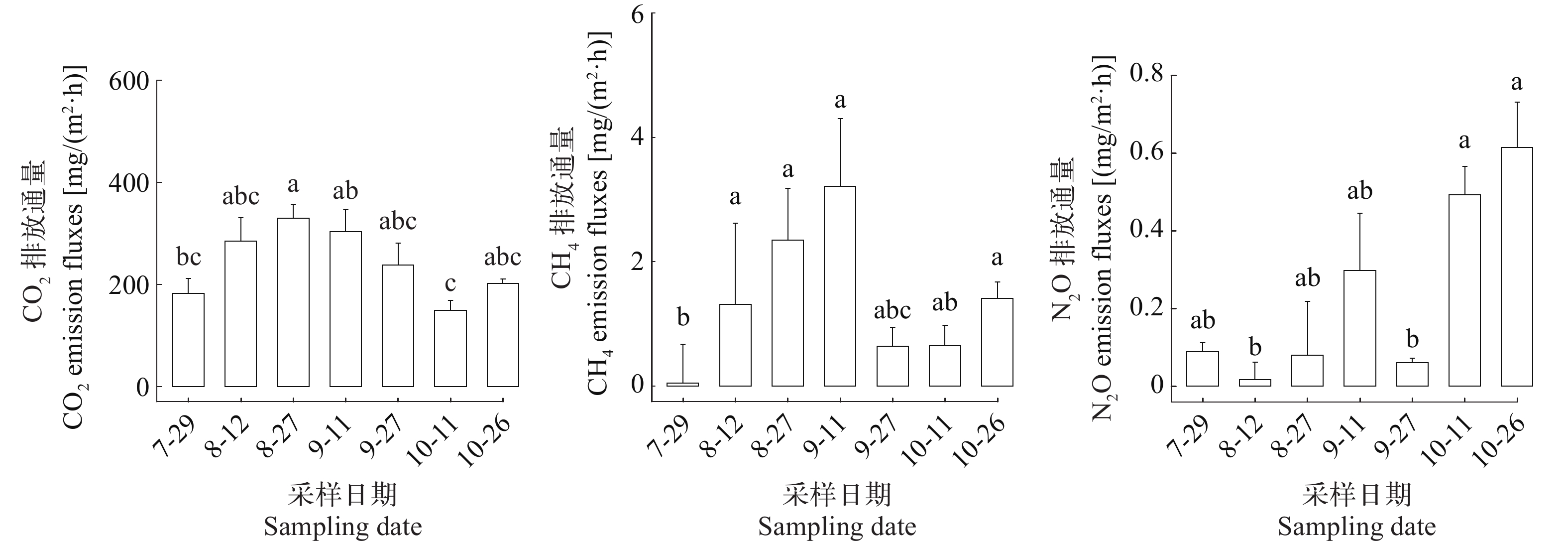
监测期间大口黑鲈养殖塘水−气界面的CO2、CH4和N2O排放通量整体上均表现为排放源, 且在不同监测时间点均呈现显著差异(P<0.05; 图 3)。不同监测时间点CO2通量变动于148.8—328.9 mg/(m2·h), 最大值出现在8—27, 最小值出现在10—11, 均值为(241.0±14.5) mg/(m2·h); 8—27的CO2通量显著高于10—11和7—29 (P<0.05)。CH4通量变动于0.20—2.79 mg/(m2·h), 均值为(1.38±0.31) mg/(m2·h), 9—11的CH4通量显著高于7—29 (P<0.05)。N2O通量变动于0.02—0.61 mg/(m2·h), 均值为(0.24±0.04) mg/(m2·h), 最大值出现在10—26, 最小值出现在8—12, 10—26的N2O通量显著高于8—12和9—27 (P<0.05)。
2.3 养殖塘水−气界面CO2、CH4、N2O排放特征的影响因素分析
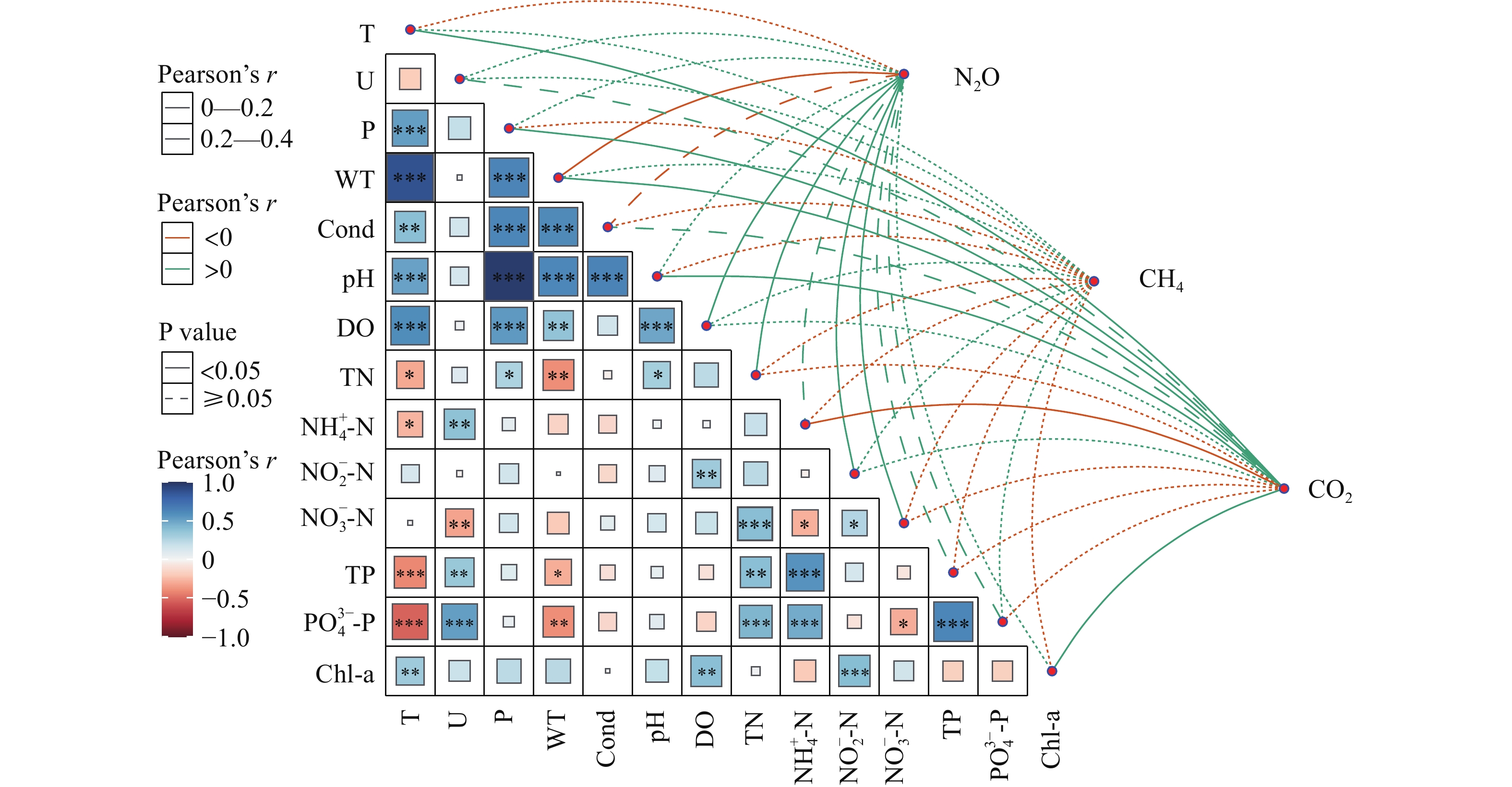
将CO2、CH4、N2O排放通量和14项环境因子进行Pearson相关分析, 结果显示T、P、WT、pH、DO、TN、${\rm{NH}}^+_4 $-N、${\rm{NO}}^-_2 $-N、${\rm{NO}}^-_3 $-N和Chl.a能影响CO2、CH4、N2O排放通量, 其中, CO2排放通量与WT (r=0.36, P<0.01)、T (r=0.27, P<0.05)、Chl.a (r =0.29, P<0.05)、P (r=0.26, P<0.05)和pH (r=0.25, P<0.05)呈显著正相关, 与${\rm{NH}}^+_4 $-N (r= –0.25, P<0.05)呈显著负相关。N2O排放通量与TN (r=0.39, P<0.01)、${\rm{NO}}^-_2 $-N (r=0.25, P<0.05)、${\rm{NO}}^-_3 $-N (r=0.29, P<0.05)和DO (r=0.26, P<0.05)呈显著正相关, 与WT (r= –0.34, P<0.01)呈显著负相关。CH4排放通量与环境因子无显著相关关系(图 4)。
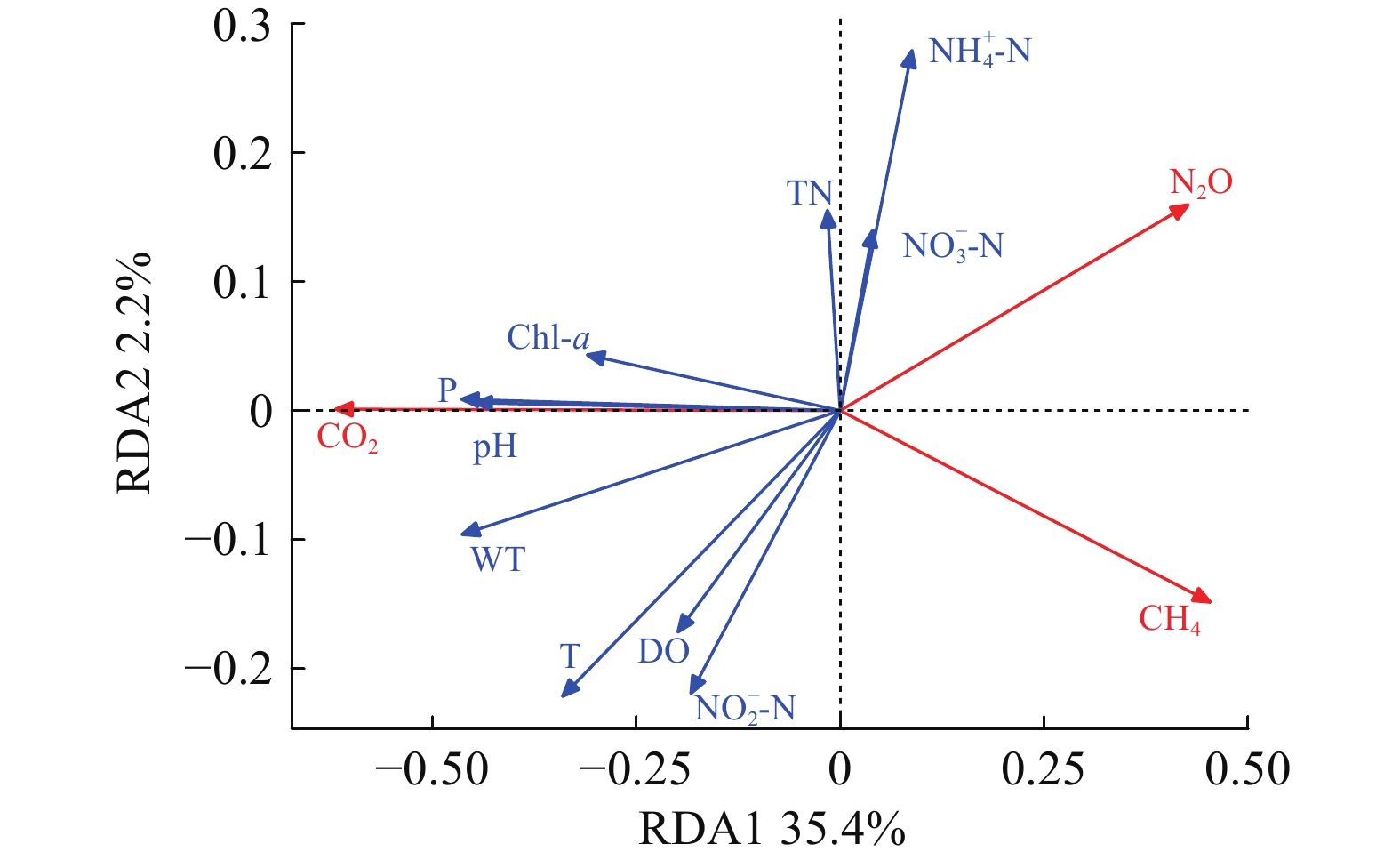
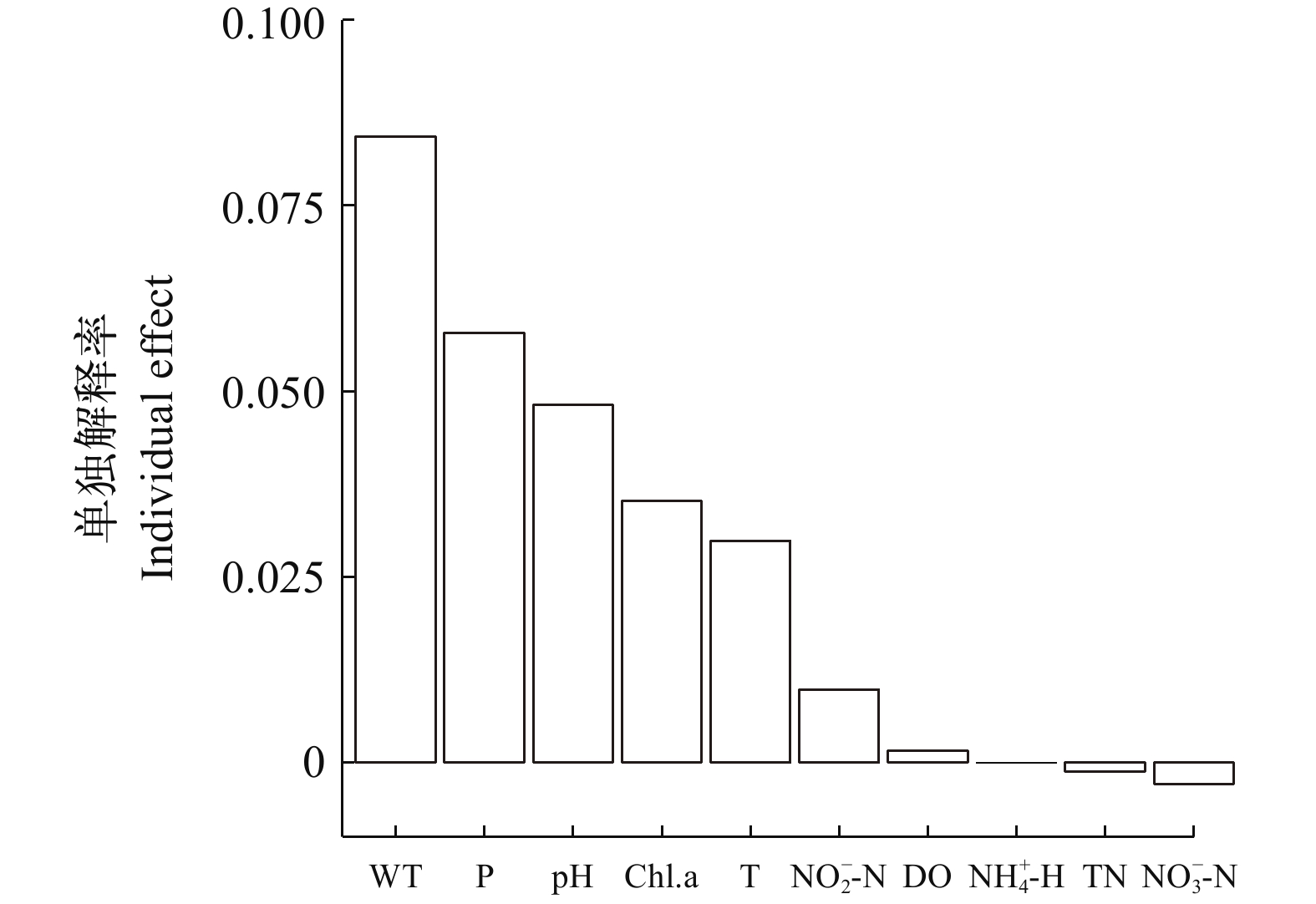
将CO2、CH4、N2O排放通量和影响通量的环境因子(T、P、pH、DO、TN、${\rm{NH}}^+_4 $-N、${\rm{NO}}^-_2 $-N、${\rm{NO}}^-_3 $-N和Chl.a)进行RDA分析, 排序轴一和轴二分别解释了35.4%和2.2%的环境因子变化信息。其中, CO2排放通量与T、WT、P、pH、DO、${\rm{NO}}^-_2 $-N和Chl.a呈正相关, 与TN、${\rm{NH}}^+_4 $-N和${\rm{NO}}^-_3 $-N呈负相关; CH4排放通量与T、WT、P、pH、DO、TN、${\rm{NH}}^+_4 $-N、${\rm{NO}}^-_2 $-N、${\rm{NO}}^-_3 $-N和Chl.a呈负相关; N2O排放通量与TN、${\rm{NH}}^+_4 $-N和${\rm{NO}}^-_3 $-N呈正相关, 与T、WT、P、pH、DO、${\rm{NO}}^-_2 $-N和Chl.a呈负相关(图 5), WT (解释率为32.2%)是水−气界面CO2、CH4、N2O排放通量的主要影响因子(图 6)。
2.4 大口黑鲈养殖塘水−气界面CO2、CH4、N2O全球增温潜势分析
在90d的大口黑鲈养殖生长期期间, 养殖塘水−气界面CO2、CH4和N2O累积排放量分别为5.26×103、32.0和4.68 kg/hm2, 三者对应的CO2排放当量分别为5.26×103、1.09×103和1.39×103 kg/hm2(表 3)。因此在100年的时间里, 大口黑鲈池塘养殖系统的全球增温潜势为7.74×103 kg/hm2, 暗示大口黑鲈池塘养殖或有促进温室效应的潜力。
表 3 大口黑鲈养殖池塘在90d实验期间的CO2、CH4和N2O累积排放量、总二氧化碳当量和增温潜势Table 3. Cumulative emissions of CO2, CH4, and N2O, total CO2 equivalent and global warming potential (GWP) in ponds of Micropterus salmoides culture in 90d experiment时间Time CO2累积排放量
CO2 cumulative emission (kg/hm2)CH4累积排放量
CH4 cumulative emission (kg/hm2)N2O累积排放量
N2O cumulative emission (kg/hm2)7-29—
8-12840.7 2.99 0.20 8-12—
8-271101.2 7.13 0.18 8-27—
9-111138.2 9.25 0.68 9-11—
9-27911.4 6.17 0.65 9-27—
10-11633.0 2.56 0.99 10-11—
10-26630.3 3.94 1.98 监测期间累积排
放量5257.8 32.04 4.68 二氧化碳排放当量(kg/hm2) 5257.8 1089.4 1394.6 全球增温潜势GWP (kg/hm2) 7741.8 注: GWP以CO2当量计Note: GWP is measured in CO2 equivalent 3. 讨论
3.1 大口黑鲈养殖塘水−气界面温室气体通量变化特征
不同的水产养殖系统温室气体排放存在较大差异。本研究监测期间大口黑鲈养殖塘整体上表现为温室气体的排放源, 且3种温室气体的排放通量呈现明显的季节变化。监测期间CO2排放通量最大值出现在温度较高的8月27日, 最低值出现在10月11日, 该结果与杨平等[12]研究结果相似。究其原因, 7月29日至9月11日期间, 水温的上升加速了水体中CO2分解速率和沉积物中CO2产生[25], 使得CO2排放增加。9月11日至10月26日期间, 随着水温的下降, 大口黑鲈觅食、代谢强度和呼吸作用下降, 同时微生物活性下降, 导致CO2产生减少。CH4排放通量表现为先上升后下降的趋势, 其中最大值出现在9月11日。7月29日至9月11日期间, 水温升高会刺激产甲烷菌活性并促进有机物分解, 为产甲烷菌产CH4提供了更多底物[25], 且有机物分解消耗氧气形成了有利于CH4排放的缺氧环境; 监测后期水温下降减弱了产甲烷菌活性, 同时提升了水中CH4的溶解度, 最终导致CH4排放的下降[26]。N2O排放通量整体上呈现上升趋势。研究表明养殖塘中不同的还原-氧化环境会影响N2O产生和排放[27], 且在${\rm{NH}}^+_4 $-N和DO含量高的环境中, 硝化反应可能是N2O产生的主要途径[28]。本研究在监测后期${\rm{NH}}^+_4 $-N含量随着养殖周期增加而增加, 硝化反应底物也随之增加, 使得N2O产生增加。
3.2 水−气界面CO2、CH4、N2O排放与环境因素
利用皮尔森相关系数值排序限制因子的方法在先前研究中得到了广泛应用[29, 30]。本研究发现, 影响大口黑鲈养殖塘CO2排放通量的环境因子依次为TW (r=0.36)、Chl.a (r=0.29)和T (r=0.27)。其中, CO2排放通量与WT和T之间呈显著正相关关系, 表明CO2排放是由养殖塘水热状态驱动。温度对CO2排放通量的正效应可能与水中有机质分解速率和沉积物中CO2产生速率有关[25]。同时温度还可以影响溶解度和水中物质的分解从而影响水中CO2产生和排放[11]。一般来说, 温度降低, 溶解度增加, 气体从大气中进入水体, 使得CO2排放通量减少。水中Chl.a浓度是估计水中浮游植物和藻类数量的重要参数, CO2排放与Chl.a之间呈现显著正相关关系, 表明有机物矿化可能与CO2排放有关[31]。
影响大口黑鲈养殖塘N2O排放通量的环境因子依次为TN (r=0.39)、WT (r= –0.34)、${\rm{NO}}^-_3 $-N (r=0.29)、DO (r=0.26)和${\rm{NO}}^-_2 $-N (r=0.25)。其中, TN与N2O排放通量呈极显著正相关关系, 这与Liu等[32]研究结果一致, 表明增加N负荷促进N2O排放。水体中溶解无机氮(${\rm{NH}}^+_4 $-N、${\rm{NO}}^-_2 $-N和${\rm{NO}}^-_3 $-N)是硝化和反硝化作用的底物, 对N2O产生和排放起着重要作用。一般来说, 较高浓度的${\rm{NO}}^-_2 $-N和${\rm{NO}}^-_3 $-N可以加速硝化和反硝化反应[6], 相对较高的${\rm{NH}}^+_4 $-N浓度可以促进沉积物和水体中硝化作用产生N2O[33]。本研究中N2O排放通量与WT呈显著负相关, 与Paudel等[34]研究结果一致。关于低温下N2O排放量增加的原因尚不明确, 可能的解释是与酶对温度的不同敏感性有关, 即低温条件下N2O还原酶的失活程度大于产生N2O的酶。本研究的CH4排放通量与其他环境因子无显著相关关系, 可能与水深较浅, 水体热分层不明显有关[35]。此外, 综合冗余分析和层次分割分析的研究结果, 表明WT是影响水−气界面CO2、CH4、N2O排放通量变化的关键环境因子, 这与前人的研究结果一致[11, 31]。
3.3 不同养殖塘水−气界面CO2、CH4和N2O排放通量比较
归纳比较我国不同类型养殖塘水−气界面的CO2、CH4和N2O排放通量特征, 发现CO2排放通量可在源和汇之间转化, CH4、N2O排放通量总体上表现为源(表 4)。养殖种类、监测时间和水生植物等因素均可对养殖塘CO2、CH4和N2O等温室气体的排放通量产生影响。Zhang等[10]综述前人的研究发现鱼类养殖、虾类养殖、蟹类养殖及多种类耦合养殖的CO2排放通量没有显著性差异, 但虾类养殖的CH4通量明显高于鱼类和蟹类养殖, 且多种类耦合养殖的CH4排放通量最低。分析认为虾类养殖中较高的放养密度和大量投喂饲料大量消耗了水体溶解氧, 从而增加CH4产量[36, 37]。多种类耦合养殖比单一养殖的CH4排放通量更低, 是因为多种类耦合养殖能更高效地利用水体内的有机物, 减少沉积物中用于产CH4的有机输入[38, 39]。与本研究不同的是, Liu等[40]发现硬壳蛤−凡纳滨对虾混养系统表现为碳汇, 这可能是贝类通过自身生长封存一部分碳酸盐[41], 此外滤食性贝类还可通过摄食利用水体中的有机质, 从而抑制CH4的产生。不同的监测时间会因为温度等环境条件的差异导致温室气体排放通量的不同。本研究的N2O排放通量显著高于杨平等[12]研究结果, 究其原因可能是本研究的监测时间为7—10月, 适宜的温度不仅增强了硝化细菌和反硝化细菌活性, 而且加快水中溶解氧消耗和降低水中N2O溶解度, 从而促进了N2O产生和排放; 同时相对较高的温度促进了大口黑鲈活动, 促使沉积物中更多的${\rm{NO}}^-_2 $-N和${\rm{NO}}^-_3 $-N释放到水中, 促进水体进行反硝化产生N2O。水生植物的有无亦可改变养殖池塘水−气界面温室气体排放强度。研究发现在中华绒螯蟹养殖塘中种植沉水植物能减少甲烷排放量[23, 42], 一方面水生植物生长能影响水体碳、氮输入和积累, 另一方面水生植物通过物理介导或拦截等作用直接影响水体排放过程[43]。
表 4 我国不同类型养殖塘的CO2、CH4、N2O通量比较Table 4. Comparison of CO2, CH4, and N2O fluxes in different types of ponds in China养殖塘类型
Type of aquaculture pond位置
Location观测时间
ObservationCO2排放通量
CO2 emission flux [mg/(m2·h)]CH4排放通量
CH4 emission flux [mg/(m2·h)]N2O排放通量
N2O emission flux [mg/(m2·h)]参考文献
Reference大口黑鲈 湖北省大冶市 2023.7—2023.10 241.0 1.38 0.24 本研究 草鱼−对虾 福建闽江河口 2011.9—2012.2 21.0 3.15 0.02 [12] 南美白对虾 福建闽江河口 2011.9—2011.11 20.8 19.95 0.01 [31] 南美白对虾 福建闽江河口 2016.5—2017.3 18.0 / / [44] 草鱼−鲢 江苏省太湖地区 2016.3—2017.3 / 0.73 / [42] 中华绒螯蟹−无水草 江苏省太湖地区 2016.3—2017.3 / 0.61 / [42] 中华绒螯蟹−有水草 江苏省太湖地区 2016.3—2017.3 / 0.54 / [42] 凡纳滨对虾−硬壳蛤 山东省东营市 2021.5—2021.9 –12.7 / / [40] 水蕹菜−中华绒螯蟹 江苏省苏州市 2018.4—2018.11 / 2.12 0.38 [23] 水稻−中华绒螯蟹 江苏省苏州市 2018.4—2018.11 / 2.08 0.48 [23] 注: “/”表示文献中没有相关数据Note: “/” indicates no relevant data in the literature 4. 结论
在大口黑鲈90d (7月29日—10月26日)的养殖生长周期期间, 大口黑鲈养殖塘整体上表现为大气温室气体排放源, CO2、CH4和N2O排放通量均值分别为(241.0±14.5)、(1.38±0.31)和(0.24±0.04) mg/(m2·h), 且呈现显著的时间变化。大口黑鲈养殖塘温室气体排放通量受T、P、pH、WT、DO、Chl.a、${\rm{NH}}^+_4 $-N、TN、${\rm{NO}}^-_2 $-N和${\rm{NO}}^-_3 $-N的调节, WT是影响水−气界面CO2、CH4和N2O排放的关键环境因子。在此养殖期内大口黑鲈养殖系统百年全球增温潜势为7.74×103 kg/hm2, 暗示大口黑鲈池塘养殖或有促进温室效应的潜力。
-
表 1 不同监测时间点大口黑鲈养殖塘的气候因子变化特征
Table 1 Characteristics of climatic factors in ponds of Micropterus salmoides culture at different monitoring times
指标Parameter 采样日期Sampling date 7—29 8—12 8—27 9—11 9—27 10—11 10—26 温度T (℃) 31.7±0.8ab 36.8±1.3a 28.0±1.4abc 37.6±1.3a 25.6±0.9bc 25.9±1.7bc 20.3±1.1c 风速U (m/s) 1.41±0.18 ab 1.78±0.31 ab 2.04±0.32 ab 1.57±0.28 ab 0.88±0.15b 1.00±0.20b 2.82±0.30a 压强P (hPa) 999.4±0.1d 1001.6±0.2cd 1009.1.±0.2abc 1006.6±0.4bcd 1005.9±0.2ab 1014.3±3.1ab 1024.7±0.4a 注: 同一行中平均值上标有不同字母表示差异显著(P<0.05); 下同Note: Means with different superscript letters are significantly different from each other in the same row (P<0.05); The same applies below 表 2 不同监测时间点大口黑鲈养殖塘的水质理化因子变化特征
Table 2 Characteristics of water quality physicochemical factors in ponds of Micropterus salmoides culture at different monitoring times
指标Parameter 采样日期Sampling date 7—29 8—12 8—27 9—11 9—27 10—11 10—26 水温WT (℃) 31.3±0.1ab 33.6±0.1a 26.9±0.1bc 31.1±0.2ab 25.3±0.1bcd 22.6±0.2cd 19.4±0.1d 溶解氧DO (mg/L) 4.75±0.36ab 5.79±0.30a 5.94±0.46a 5.89±0.44a 4.02±0.19b 5.58±0.43ab 5.96±0.38a 电导率Cond (μS/cm) 577.2±16.1ab 677.6±27.9a 571.7±20.2abc 482.7±60.6bc 599.2±14.0ab 590.9±11.2ab 455.6±4.4c pH 8.36±0.05ab 8.38±0.06 ab 8.24±0.03b 8.65±0.06a 9.05±0.19a 8.59±0.07a 8.46±0.08ab 表 3 大口黑鲈养殖池塘在90d实验期间的CO2、CH4和N2O累积排放量、总二氧化碳当量和增温潜势
Table 3 Cumulative emissions of CO2, CH4, and N2O, total CO2 equivalent and global warming potential (GWP) in ponds of Micropterus salmoides culture in 90d experiment
时间Time CO2累积排放量
CO2 cumulative emission (kg/hm2)CH4累积排放量
CH4 cumulative emission (kg/hm2)N2O累积排放量
N2O cumulative emission (kg/hm2)7-29—
8-12840.7 2.99 0.20 8-12—
8-271101.2 7.13 0.18 8-27—
9-111138.2 9.25 0.68 9-11—
9-27911.4 6.17 0.65 9-27—
10-11633.0 2.56 0.99 10-11—
10-26630.3 3.94 1.98 监测期间累积排
放量5257.8 32.04 4.68 二氧化碳排放当量(kg/hm2) 5257.8 1089.4 1394.6 全球增温潜势GWP (kg/hm2) 7741.8 注: GWP以CO2当量计Note: GWP is measured in CO2 equivalent 表 4 我国不同类型养殖塘的CO2、CH4、N2O通量比较
Table 4 Comparison of CO2, CH4, and N2O fluxes in different types of ponds in China
养殖塘类型
Type of aquaculture pond位置
Location观测时间
ObservationCO2排放通量
CO2 emission flux [mg/(m2·h)]CH4排放通量
CH4 emission flux [mg/(m2·h)]N2O排放通量
N2O emission flux [mg/(m2·h)]参考文献
Reference大口黑鲈 湖北省大冶市 2023.7—2023.10 241.0 1.38 0.24 本研究 草鱼−对虾 福建闽江河口 2011.9—2012.2 21.0 3.15 0.02 [12] 南美白对虾 福建闽江河口 2011.9—2011.11 20.8 19.95 0.01 [31] 南美白对虾 福建闽江河口 2016.5—2017.3 18.0 / / [44] 草鱼−鲢 江苏省太湖地区 2016.3—2017.3 / 0.73 / [42] 中华绒螯蟹−无水草 江苏省太湖地区 2016.3—2017.3 / 0.61 / [42] 中华绒螯蟹−有水草 江苏省太湖地区 2016.3—2017.3 / 0.54 / [42] 凡纳滨对虾−硬壳蛤 山东省东营市 2021.5—2021.9 –12.7 / / [40] 水蕹菜−中华绒螯蟹 江苏省苏州市 2018.4—2018.11 / 2.12 0.38 [23] 水稻−中华绒螯蟹 江苏省苏州市 2018.4—2018.11 / 2.08 0.48 [23] 注: “/”表示文献中没有相关数据Note: “/” indicates no relevant data in the literature -
[1] Waldemer C, Koschorreck M. Spatial and temporal variability of greenhouse gas ebullition from temperate freshwater fish ponds [J]. Aquaculture, 2023(574): 739656. doi: 10.1016/j.aquaculture.2023.739656
[2] Mosier A R. Soil processes and global change [J]. Biology and Fertility of Soils, 1998, 27(3): 221-229. doi: 10.1007/s003740050424
[3] National Oceanic and Atmospheric (NOAA). Carbon cycle greenhouse gases [EB/OL]. 2023. Available in: https://www.esrl.noaa.gov/gmd/ccgg/.
[4] Raymond P A, Hartmann J, Lauerwald R, et al. Global carbon dioxide emissions from inland waters [J]. Nature, 2013, 503(7476): 355-359. doi: 10.1038/nature12760
[5] Peacock M, Audet J, Bastviken D, et al. Small artificial waterbodies are widespread and persistent emitters of methane and carbon dioxide [J]. Global Change Biology, 2021, 27(20): 5109-5123. doi: 10.1111/gcb.15762
[6] Yang P, Yang H, Lai D Y F, et al. Large contribution of non-aquaculture period fluxes to the annual N2O emissions from aquaculture ponds in Southeast China [J]. Journal of Hydrology, 2020(582): 124550. doi: 10.1016/j.jhydrol.2020.124550
[7] 周梅, 叶丽菲, 张超, 等. 广东新丰江水库表层水体CO2分压及其影响因素 [J]. 湖泊科学, 2018, 30(3): 770-781.] doi: 10.18307/2018.0319 Zhou M, Ye L F, Zhang C, et al. Partial pressure of carbon dioxide in the Xinfengjiang Reservoir of Guangdong Province and its influencing factors [J]. Journal of Lake Sciences, 2018, 30(3): 770-781. [ doi: 10.18307/2018.0319
[8] Tong C, Bastviken D, Tang K W, et al. Annual CO2 and CH4 fluxes in coastal earthen ponds with Litopenaeus vannamei in Southeastern China [J]. Aquaculture, 2021(545): 737229. doi: 10.1016/j.aquaculture.2021.737229
[9] Yuan J, Xiang J, Liu D, et al. Rapid growth in greenhouse gas emissions from the adoption of industrial-scale aquaculture [J]. Nature Climate Change, 2019(9): 318-322. doi: 10.1038/s41558-019-0425-9
[10] Zhang Y, Tang K W, Yang P, et al. Assessing carbon greenhouse gas emissions from aquaculture in China based on aquaculture system types, species, environmental conditions and management practices [J]. Agriculture, Ecosystems & Environment, 2022(338): 108110.
[11] 宋红丽, 刘兴土, 文波龙. 黄河三角洲养殖塘水−气界面CO2、CH4和N2O通量特征 [J]. 生态环境学报, 2017, 26(9): 1554-1561.] Song H L, Liu X T, Wen B L. Greenhouse gases fluxes at water-air interface of aquaculture ponds in the Yellow River estuary [J]. Ecology and Environmental Sciences, 2017, 26(9): 1554-1561. [
[12] 杨平, 仝川, 何清华, 等. 闽江口鱼虾混养塘水−气界面温室气体通量及主要影响因子 [J]. 环境科学学报, 2013, 33(5): 1493-1503.] Yang P, Tong C, He Q H, et al. Greenhouse gases fluxes at water-air interface of aquaculture ponds and influencing factors in the Min River estuary [J]. Acta Scientiae Circumstantiae, 2013, 33(5): 1493-1503. [
[13] Fang X, Zhao J, Wu S, et al. A two-year measurement of methane and nitrous oxide emissions from freshwater aquaculture ponds: Affected by aquaculture species, stocking and water management [J]. Science of the Total Environment, 2022(813): 151863. doi: 10.1016/j.scitotenv.2021.151863
[14] Yang P, Wang D Q, Lai D, et al. Spatial variations of N2O fluxes across the water-air interface of mariculture ponds in a subtropical estuary in Southeast China [J]. Journal of Geophysical Research: Biogeosciences, 2020, 125(9): e2019JG005605. doi: 10.1029/2019JG005605
[15] Stankus A. State of world aquaculture 2020 and regional reviews: FAO webinar series [J]. FAO Aquaculture Newsletter, 2021(63): 17-18.
[16] 农业农村部渔业渔政管理局. 2023中国渔业统计年鉴 [R]. 北京: 中国农业出版社, 2023: 21-25.] Fishery Administration of Ministry of Agriculture and Rural Affairs. China Fishery Statistical Yearbook [R]. Beijing: China Agriculture Press, 2023: 21-25. [
[17] Zhu L, Che X, Liu H, et al. Greenhouse gas emissions and comprehensive greenhouse effect potential of Megalobrama amblycephala culture pond ecosystems in a 3-month growing season [J]. Aquaculture International, 2016, 24(4): 893-902. doi: 10.1007/s10499-015-9959-7
[18] 安桐彤, 许潇方, 高强, 等. 我国养殖水体N2O排放特征及其影响因素研究进展 [J]. 生态学杂志, 2021, 40(1): 266-277.] An T T, Xu X F, Gao Q, et al. Spatiotemporal distribution and the influencing factors of nitrous oxide emissions from aquaculture water in China: a review [J]. Chinese Journal of Ecology, 2021, 40(1): 266-277. [
[19] Tidwell J H, Coyle S D, Bright L A, et al. Effect of water temperature on growth, survival, and biochemical composition of largemouth bass Micropterus salmoides [J]. Journal of the World Aquaculture Society, 2003, 34(2): 175-183. doi: 10.1111/j.1749-7345.2003.tb00054.x
[20] Park J, Renukdas N, Luna T, et al. The effects of biomass density on size variability and growth performance of juvenile largemouth bass, Micropterus salmoides, in a semi-closed recirculating system [J]. Journal of the World Aquaculture Society, 2015, 46(3): 283-291. doi: 10.1111/jwas.12194
[21] 张政, 刘梅, 周聃, 等. 我国淡水增养殖系统温室气体排放的时空特征研究进展 [J]. 广东海洋大学学报, 2023, 43(6): 153-162.] Zhang Z, Liu M, Zhou D, et al. Spatial and temporal characteristics of greenhouse gas emissions from freshwater aquaculture systems in China [J]. Journal of Guangdong Ocean University, 2023, 43(6): 153-162. [
[22] 国家环境保护总局水和废水监测分析方法(第四版) [M]. 北京: 中国环境出版社, 2002: 243-670.] State Environmental Protection Administration. Monitoring and Analysis Method of Water and Wastewater (4th edition) [M]. Beijing: China Environment Science Press, 2002: 243-670. [
[23] 刘永茂, 付为国, 金梅娟, 等. 高温季节蟹塘不同水生植物对水质净化和温室气体排放的影响 [J]. 生态与农村环境学报, 2020, 36(8): 1072-1079.] Liu Y M, Fu W G, Jin M J, et al. Effects of different aquatic plants on water purification and greenhouse gas emission in crab pond in high temperature season [J]. Journal of Ecology and Rural Environment, 2020, 36(8): 1072-1079. [
[24] Intergovernmental Panel on Climate Change. Climate Change 2013 - the Physical Science Basis Working Group I Contribution to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change [M]. Cambridge University Press, 2014.
[25] Yang P, Zhang Y, Lai D Y F, et al. Fluxes of carbon dioxide and methane across the water–atmosphere interface of aquaculture shrimp ponds in two subtropical estuaries: The effect of temperature, substrate, salinity and nitrate [J]. Science of the Total Environment, 2018(635): 1025-1035. doi: 10.1016/j.scitotenv.2018.04.102
[26] Odinga S A, Sifuna A, Lungayia H, et al. Greenhouse gas emissions associated with nile tilapia (Oreochromis niloticus) pond fertilization in western Kenya [J]. The Scientific World Journal, 2023(2023): 1712985.
[27] 胡博文, 潘萌, 石彭兰, 等. 气候变暖与富营养化交互作用对浅水湖泊水−气界面N2O通量的影响 [J]. 水生生物学报, 2021, 45(3): 625-635.] Hu B W, Pan M, Shi P L, et al. Effect of climate warming and eutrophication on N2O flux at water-air interface of shallow lakes [J]. Acta Hydrobiologica Sinica, 2021, 45(3): 625-635. [
[28] Barnard R, Leadley P W, Hungate B A. Global change, nitrification, and denitrification: a review [J]. Global Biogeochemical Cycles, 2005, 19(1): GB1007.
[29] 张晓晶, 李畅游, 贾克力, 等. 乌梁素海水体透明度分布及影响因子相关分析 [J]. 湖泊科学, 2009, 21(6): 879-884.] doi: 10.18307/2009.0619 Zhang X J, Li C Y, Jia K L, et al. Spatial-temporal changes in water transparency and its impact factors in Lake Wuliangsuhai [J]. Journal of Lake Sciences, 2009, 21(6): 879-884. [ doi: 10.18307/2009.0619
[30] 郭超, 李为, 李诗琦, 等. 盐龙湖沉水植物群落变化规律及其驱动因子研究 [J]. 水生态学杂志, 2021, 42(6): 34-40.] Guo C, Li W, Li S Q, et al. Succession and driving factors of submerged macrophytes in Yanlong Lake [J]. Journal of Hydroecology, 2021, 42(6): 34-40. [
[31] Yang P, He Q, Huang J, et al. Fluxes of greenhouse gases at two different aquaculture ponds in the coastal zone of Southeastern China [J]. Atmospheric Environment, 2015, 115: 269-277. doi: 10.1016/j.atmosenv.2015.05.067
[32] Liu X L, Liu C Q, Li S L, et al. Spatiotemporal variations of nitrous oxide (N2O) emissions from two reservoirs in SW China [J]. Atmospheric Environment, 2011, 45(31): 5458-5468. doi: 10.1016/j.atmosenv.2011.06.074
[33] Wang J, Chen N, Yan W, et al. Effect of dissolved oxygen and nitrogen on emission of N2O from rivers in China [J]. Atmospheric Environment, 2015, 103: 347-356. doi: 10.1016/j.atmosenv.2014.12.054
[34] Paudel S R, Choi O, Khanal S K, et al. Effects of temperature on nitrous oxide (N2O) emission from intensive aquaculture system [J]. Science of the Total Environment, 2015(518): 16-23.
[35] Webb J R, Leavitt P R, Simpson G L, et al. Regulation of carbon dioxide and methane in small agricultural reservoirs: optimizing potential for greenhouse gas uptake [J]. Biogeosciences, 2019, 16(21): 4211-4227. doi: 10.5194/bg-16-4211-2019
[36] van Bergen T J H M, Barros N, Mendonça R, et al. Seasonal and diel variation in greenhouse gas emissions from an urban pond and its major drivers [J]. Limnology and Oceanography, 2019, 64(5): 2129-2139. doi: 10.1002/lno.11173
[37] Chen Y, Dong S, Wang F, et al. Carbon dioxide and methane fluxes from feeding and no-feeding mariculture ponds [J]. Environmental Pollution, 2016(212): 489-497. doi: 10.1016/j.envpol.2016.02.039
[38] Zhang D, Xu W, Wang F, et al. Carbon dioxide fluxes from mariculture ponds with swimming crabs and shrimps in Eastern China: The effect of adding razor clams [J]. Aquaculture Reports, 2022(22): 100917. doi: 10.1016/j.aqrep.2021.100917
[39] Zhang D, Tian X, Dong S, et al. Carbon budgets of two typical polyculture pond systems in coastal China and their potential roles in the global carbon cycle [J]. Aquaculture Environment Interactions, 2020(12): 105-115. doi: 10.3354/aei00349
[40] 刘旭博, 董世鹏, 于力业, 等. 凡纳滨对虾-硬壳蛤池塘综合养殖系统水−气界面 CO2 通量及其与环境因子的关系 [J]. 中国海洋大学学报 (自然科学版), 2023, 53(8): 26-34.] Liu X B, Dong S P, Yu L Y, et al. CO2 flux on water-air interface of integrated pond culture system of Litopenaeus vannamei and Mercenaria mercenaria and Its relationships with environmental factors [J]. Periodical of Ocean University of China, 2023, 53(8): 26-34. [
[41] Morris J P, Humphreys M P. Modelling seawater carbonate chemistry in shellfish aquaculture regions: Insights into CO2 release associated with shell formation and growth [J]. Aquaculture, 2019(501): 338-344. doi: 10.1016/j.aquaculture.2018.11.028
[42] 马煜春, 孙丽英, 刘翠英, 等. 太湖地区两种典型水产养殖系统CH4排放研究 [J]. 生态环境学报, 2018, 27(7): 1269-1275.] Ma Y C, Sun L Y, Liu C Y, et al. Methane emission from two typical aquaculture ponds in Taihu Lake [J]. Ecology and Environmental Sciences, 2018, 27(7): 1269-1275. [
[43] 龚小杰, 袁兴中, 刘婷婷, 等. 水生植物对淡水生态系统温室气体排放的影响研究进展 [J]. 地球与环境, 2020, 48(4): 496-509.] Gong X J, Yuan X Z, Liu T T, et al. Review on Effects of aquatic plants on the greenhouse gas emission from freshwater ecosystems [J]. Earth and Environment, 2020, 48(4): 496-509. [
[44] 赵光辉, 杨平, 谭立山, 等. 闽江河口养虾塘养殖期和非养殖期CO2通量变化特征 [J]. 环境科学研究, 2020, 33(4): 949-957.] Zhao G H, Yang P, Tan L S, et al. Temporal variation of carbon dioxide flux between farming and non-farming stages in the land-based shrimp pond in the Min River estuary [J]. Research of Environmental Sciences, 2020, 33(4): 949-957. [



 下载:
下载: